Adenoid hypertrophy is a condition that presents itself as the chronic enlargement of adenoid tissues; it is frequently observed in the pediatric population. The Ugrp2 gene, a member of the secretoglobin superfamily, encodes a low‐molecular weight protein that functions in the differentiation of upper airway epithelial cells. However, little is known about the association of Ugrp2 genetic variations with adenoid hypertrophy.
ObjectiveThe aim of this study is to investigate the association of single nucleotide polymorphisms in the Ugrp2 gene with adenoid hypertrophy and its related phenotypes.
MethodsA total of 219 children, comprising 114 patients suffering from adenoid hypertrophy and 105 healthy patients without adenoid hypertrophy, were enrolled in this study. Genotypes of the Ugrp2 gene were determined by DNA sequencing.
ResultsWe identified four single nucleotide polymorphisms (IVS1‐189G>A, IVS1‐89T>G, c.201delC, and IVS2‐15G>A) in the Ugrp2 gene. Our genotype analysis showed that the Ugrp2 (IVS1‐89T>G) TG and (c.201delC) CdelC genotypes and their minor alleles were associated with a considerable increase in the risk of adenoid hypertrophy compared with the controls (p=0.012, p=0.009, p=0.013, and p=0.037, respectively). Furthermore, Ugrp2 (GTdelCG, GTdelCA) haplotypes were significantly associated with adenoid hypertrophy (four single nucleotide polymorphisms ordered from 5′ to 3′; p=0.0001). Polymorfism‐Polymorfism interaction analysis indicated a strong interaction between combined genotypes of the Ugrp2 gene contributing to adenoid hypertrophy, as well as an increased chance of its diagnosis (p<0.0001). In addition, diplotypes carrying the mutant Ugrp2 (c.201delC) allele were strongly associated with an increased risk of adenoid hypertrophy with asthma and with allergies (p=0.003 and p=0.0007, respectively).
ConclusionSome single nucleotide polymorphisms and their combinations in the Ugrp2 gene are associated with an increased risk of developing adenoid hypertrophy. Therefore, we tried to underline the importance of genetic factors associated with adenoid hypertrophy and its related clinical phenotypes.
A adenoide ou hipertrofia de tonsila faríngea é uma condição que se apresenta como o aumento crônico de tecidos linfoides na rinofaringe e é frequentemente observada na população pediátrica. O gene Ugrp2, um membro da superfamília da secretoglobina, codifica uma proteína de baixo peso molecular que funciona na diferenciação das células epiteliais das vias aéreas superiores. No entanto, pouco se sabe sobre a associação de variações genéticas do Ugrp2 com hipertrofia de tonsila faríngea.
ObjetivoInvestigar a associação de polimorfismos de nucleotídeos únicos no gene Ugrp2 com hipertrofia de tonsila faríngea e seus fenótipos relacionados.
MétodoForam incluídos no estudo 219 crianças, 114 pacientes com hipertrofia de tonsila faríngea e 105 saudáveis. Os genótipos do gene Ugrp2 foram determinados por sequenciamento de DNA.
ResultadosIdentificamos quatro polimorfismos de nucleotídeo único (IVS1‐189G>A, IVS1‐89T>G, c.201delC, e IVS2‐15G>A) no gene Ugrp2. Nossa análise genotípica mostrou que os genótipos Ugrp2 (IVS1‐89T>G) TG e (c.201delC) CdelC e seus alelos menores foram associados a um aumento considerável no risco de HA em comparação com os controles (p=0,012, p=0,009, p=0,013 e p=0,037, respectivamente). Além disso, os haplótipos Ugrp2 (GTdelCG, GTdelCA) foram significativamente associados com hipertrofia de tonsila faríngea (quatro polimorfismos de nucleot’ ordenados de 5’ a 3’; p=0,0001). A análise de interação polimorfismo‐polimorfismo indicou uma forte interação entre genótipos combinados do gene Ugrp2 que contribuiu para hipertrofia de tonsila faríngea, bem como uma chance maior de seu diagnóstico (p<0,0001). Além disso, os diplótipos que transportam o alelo mutante Ugrp2 (c.201delC) foram fortemente associados a um risco aumentado de hipertrofia de tonsila faríngea com asma e com alergias (p=0,003 e p=0,0007, respectivamente).
ConclusãoAlguns polimorfismos de nucleotídeo único e suas combinações no gene Ugrp2 estão associados a um risco aumentado de desenvolver hipertrofia de tonsila faríngea. Portanto, tentamos enfatizar a importância dos fatores genéticos e fenótipos clínicos associados a essa hipertrofia.
A adenoide, também conhecida como hipertrofia de tonsila faríngea (HTF) ou nasofaríngea, é um componente importante do anel de Waldeyer e parece desempenhar um papel importante no desenvolvimento da “memória imunológica”.1 A hipertrofia de tonsila faríngea é uma condição muito comum em crianças.2 Os sintomas associados à HTF incluem congestão nasal, rinorreia, fala hiponasal, respiração com boca aberta, apneia do sono testemunhada, ronco e uma estrutura facial conhecida como “facies adenoideana”, causada pela obstrução crônica das vias aéreas.2,3 Os mecanismos exatos subjacentes à proliferação linfoide folicular e à hiperplasia das tonsila faríngeas são mal compreendidos. No entanto, atualmente, considera‐se que a inflamação recorrente ou crônica da tonsila faríngea contribui para a ativação crônica de respostas imunes mediadas por células e humorais e leva à HTF.4
As citocinas, que atuam em respostas imunológicas, podem afetar o processo de inflamação. Além disso, acredita‐se que certos polimorfismos de nucleotídeos únicos (PNU) em citocinas contribuem para uma predisposição à HTF.5 Definir os fatores que afetam respostas imunes associadas à HTF forneceria dados importantes para determinar a patogênese da HTF. Vários fatores genéticos podem afetar certos fenótipos da doença e alterar a gravidade das doenças inflamatórias crônicas e os níveis de expressão gênica.6
As secretoglobinas (SCGBs) constituem uma recém‐descoberta superfamília fisiologicamente e fisiopatologicamente ativa e de rápida expansão de proteínas secretoras semelhantes a citocinas com pequenas estruturas diméricas. Elas são candidatas a uma nova família de citocinas, pois têm funções anti‐inflamatórias e imunomoduladoras. Onze genes SCGB e cinco pseudogenes foram descritos no genoma humano.7 Foi relatado que o gene Ugrp2 (Scgb3a1) desempenha um papel na patogênese de alguns tipos de câncer, bem como nas doenças inflamatórias das vias aéreas superiores e inferiores, inclusive asma, alergias e polipose nasal.8–10 Também foi relatado que o UGRP2 é um potente inibidor do crescimento, migração e invasão celular através da via de sinalização AKT.9
O gene Ugrp2 foi identificado em 2002; no entanto, muito poucos estudos foram feitos nesse gene.7 Portanto, no presente estudo, buscamos identificar PNU no gene Ugrp2 e analisar as associações desses PNU com HTF em crianças.
MétodoPopulação do estudoA coorte do estudo nesta investigação consistiu em 114 crianças internadas na clínicas de otorrinolaringologia e pediatria com sintomas de dormir de boca aberta, ronco, apneia do sono testemunhada, fala hiponasal, desnutrição e distúrbios de desenvolvimento médio‐facial e foram diagnosticados com HTF. O diagnóstico de HTF foi baseado no histórico do paciente, bem como em exames físicos e endoscópicos.11 A HTF foi classificada de acordo com a classificação de Parikh: o Grau 1 indica inflamação da tonsila faríngea e ausência de contato com estruturas adjacentes; o Grau 2 indica inflamação da tonsila faríngea em contato com o toro tubário; o Grau 3 indica inflamação da tonsila faríngea em contato com o vômer; e o Grau 4 indica inflamação da tonsila faríngea em contato com o palato mole.12 Em nosso estudo, os pacientes classificados com os graus 2, 3 ou 4 de Parikh foram considerados como tendo HTF e incluídos no estudo.
O grupo controle consistiu em 105 crianças saudáveis admitidas no ambulatório do mesmo hospital para seguimentos regulares ou traumas menores. Os exames endoscópicos nasais foram feitos para confirmar que elas não apresentavam HTF.
A confirmação da apneia do sono testemunhada, do ronco e do ato de dormir de boca aberta foi obtida dos pais das crianças.13 O diagnóstico de asma foi baseado no histórico do paciente ou no exame das crianças no departamento de pneumologia.14 Testes cutâneos foram usados para identificar alergias e foram feitos de acordo com as recomendações da European Academy of Allergology and Clinical Immunology (EAACI).15 As crianças cujos resultados foram positivos para pelo menos um dos alérgenos testados foram consideradas alérgicas.
Os pais das crianças foram informados sobre o estudo e o consentimento informado foi obtido verbalmente e por escrito. O comitê de ética local aprovou os protocolos do estudo e o estudo foi feito de acordo com os direitos humanos e a ética experimental (número de registro 2012‐898).
Foram excluídas deste estudo crianças com anormalidades craniofaciais, defeitos congênitos, retardo mental ou imunodeficiência, bem como doenças cardiovasculares, pulmonares, metabólicas, genéticas ou neuromusculares.16
Sequenciamento do DNAAs amostras de sangue foram incubadas em EDTA. O DNA genômico foi extraído de leucócitos de sangue periférico com o kit NucleoSpin DNA (Macherey‐Nagel, Alemanha). A reação em cadeia de polimerase (PCR) foi feita para amplificar a região relevante do gene (SuperHot Master Mix, Bioron, Alemanha). O gene Ugrp2 tem três exons; portanto, três pares de primers foram usados para a reação de PCR. Para o primeiro exon, 5′‐GGTCAGACCGCAAAGCGAAGG‐3′ foi usado como o primer forward e 5′‐GACCTGGGATCCACGATCGG‐3′ foi usado como o primer reverse; um fragmento de 465‐pb foi amplificado. Para o segundo exon, 5′‐TGCACAGAGTTCACCGGTCCTTC‐3′ foi usado como o primer forward e 5′‐AGGGGCAGGACGGGAAACAG‐3′ como o primer reverse; um fragmento de 611‐pb foi amplificado. Para o terceiro exon, 5′‐CCGCTCCCGCTCCCCACAGA‐3′ foi usado como o primer forward e 5′‐TCTCTCCCTCTCTCACGCAGCAC‐3′ como o primer reverse; um fragmento de 349‐pb foi amplificado. O kit NucleoFast 96 PCR foi usado para a purificação dos produtos amplificados (Macherey‐Nagel). O sequenciamento foi feito para o gene Ugrp2. A reação de sequenciamento foi feita com produtos de PCR purificados. Os produtos obtidos do sequenciamento foram purificados com o kit ZR Sequencing Clean‐up D4051 (Zymo Research, EUA) e preparados para análise de arrays. Os polimorfismos no gene Ugrp2 foram identificados com o equipamento de sequenciamento automático capilar ABI PRISM 3130 Genetic Analyzer.
Análise estatísticaO programa Statistical Package for Social Sciences (SPSS) (versão 22.0, SSPS Inc., EUA) foi usado para análise estatística. A média de idade entre os grupos foi comparada com o teste U de Mann‐Whitney. O teste χ2 ou o teste exato de Fisher foi usado para analisar a associação entre PNU do Ugrp2 e fenótipos clínicos. A frequência de cada genótipo foi testada com o χ2 para concordância com Equilíbrio de Hardy‐Weinberg (EHW).17
Um estudo de Aydin et al. em 1.132 indivíduos na Turquia obteve uma frequência de HTF de 27% para crianças de cinco a sete anos e 19,5% para crianças de oito a 10 anos.18 Levando a prevalência de HTF em consideração, o menor tamanho de amostra necessário para alcançar 78% de confiança foi determinado como de 90 casos.19 Portanto, incluímos 114 pacientes com HTF e 105 crianças saudáveis em nosso estudo.
O software SNPstats foi usado para determinar o grau de desequilíbrio de ligação (DL), bem como na análise de genótipos e haplótipos (http://bioinfo.iconcologia.net/index.php?module=SNPstats).20 Esse software fornece a razão de chances ou odds ratio (OR) e o intervalo de confiança de 95% (IC 95%). Usamos o pacote de software Multifactor Dimensionality Reduction (MDR) (versão 1.0.0, disponível em www.epistasis.org) para abordar possíveis interações PNU‐PNU e PNU ‐fenótipo. O MDR é uma abordagem inovadora descrita por Hahn et al.21 É uma ferramenta computacional e um método não paramétrico (ou seja, parâmetros não são estimados) capazes de detectar interações PNU‐PNU e PNU‐fenótipo em estudos de associação genética. Esse método reduz a dimensionalidade dos dados ao juntar genótipos de múltiplos PNU em grupos de alto risco ou de baixo risco para uma doença, dessa forma contorna o problema de analisar combinações de genótipos de alta ordem com um baixo número de observações. O software identificou com sucesso as combinações de genótipos multilócus associados a doenças e fatores ambientais discretos.22,23 Um valor de p < 0,05 foi considerado significativo em todas as análises estatísticas.
ResultadosCaracterísticas dos participantes do estudoForam incluídas no estudo 219 crianças (114 pacientes com HÁ, dos quais 54 do sexo feminino e 60 do masculino, com média de 5,38 anos [3‐9] e 105 crianças saudáveis, das quais 46 eram do sexo feminino e 59 do masculino, com média de 5,23 anos [2‐10]). As médias das idades (p = 0,570) e as distribuições por sexo (p = 0,709) entre os grupos de estudo e controle não foram estatisticamente significantes. Outras características relevantes da população estudada estão resumidas na tabela 1.
Características da população do estudo
| Pacientes com HTF (n = 114) | Crianças‐controle saudáveis (n = 105) | p‐valor | |
|---|---|---|---|
| Idade (anos) (media ± DP) | 5,38 (1.532) | 5,23 (1.712) | 0,570a |
| Sexo, n (%) | |||
| Masculino | 60 (53) | 59 (56) | 0,709b |
| Feminino | 54 (47) | 46 (44) | |
| Asma (+), n (%) | 30 (26) | 14 (13) | 0,042b |
| Alergia (+), n (%) | 33 (29) | 15 (14) | 0,032c |
Os valores são apresentados como mediana ± DP ou números (%), a menos que especificado de outra forma.
DP, desvio padrão; HTF, hipertrofia de tonsila faríngea; n (%), frequência.
A prevalência de asma e alergias foi maior em crianças com HTF do que no grupo controle (p = 0,047 e p = 0,032, respectivamente). No grupo HTF, 76 (67%) crianças tinham um histórico de dormir com a boca aberta, 80 (70%) tinham histórico de ronco e 81 (71%) tinham histórico de apneia do sono testemunhada.
Relação entre o gene Ugrp2 e HTFNo presente estudo, detectamos quatro PNU dentro do gene Ugrp2. Os PNU IVS1‐189G>A, IVS1‐89T>G, c.201delC, e IVS2‐15G>A foram observados dentro do intron 1, intron 1, exon 2 e intron 2 do gene, respectivamente. Os PNU foram relatados anteriormente e foram registrados no banco de dados de PNU (dbSNP; Short Genetic Variations Database em http://www.ncbi.nlm.nih.gov/snp; números de acesso rs549066053, rs117170752, rs200868132, e rs529004193, respectivamente). As distribuições genotípicas das crianças saudáveis foram consistentes com aquelas esperadas de acordo com os cálculos de EHW (p ¿ 0,05 para todos).
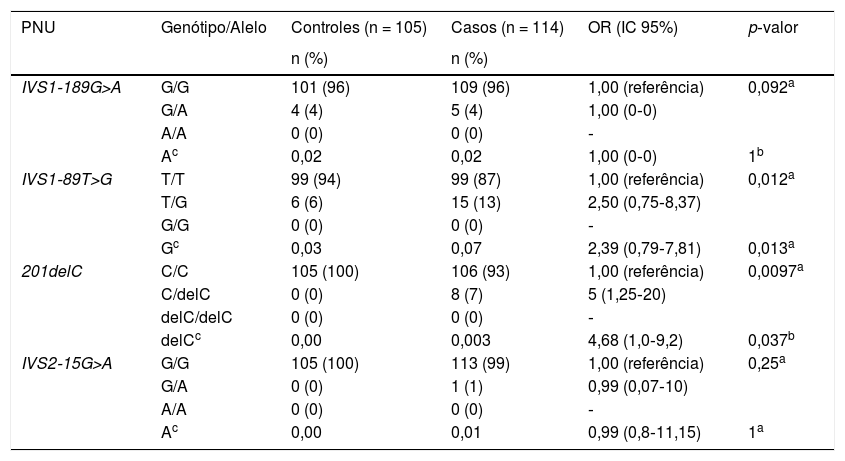
Como mostrado na tabela 2, as análises dos genótipos demonstraram que as frequências do genótipo do Ugrp2 (IVS1‐189G>A) GG, GA e alelo menor foram semelhantes entre os grupos de estudo e controle (0,02 vs. 0,02; p = 0,092 e p = 1, respectivamente). Esse PNU não mostrou correlação com um risco aumentado de HTF. Além disso, observamos que as frequências do genótipo do Ugrp2 (IVS1‐89T>G) TT, TG e o alelo G eram diferentes entre os grupos de estudo e controle (0,07 vs. 0,03; p = 0,012 e p = 0,013, respectivamente). Além disso, indivíduos com o genótipo do Ugrp2 (IVS1‐89T>G) TG e o alelo G eram 2,5 ou 2,3 vezes mais propensos a apresentar HTF do que aqueles com o genótipo TT e o alelo T. Também verificamos que as frequências do genótipo do Ugrp2 (c.201delC) CC, CdelC e alelo delC foram significativamente diferentes entre os grupos de estudo e controle (0,003 vs. 0; p = 0,0009 e p = 0,037, respectivamente). Os indivíduos com o genótipo do Ugrp2 (c.201delC) CC, CdelC e o alelo delC também apresentaram 5 e 4,6 vezes mais probabilidades de apresentar HTF do que aqueles com o genótipo homozigótico do tipo selvagem e o alelo principal. As frequências do genótipo do Ugrp2 (IVS2‐15G> A) GG, GA e o alelo menor não foram significativamente diferentes entre os grupos de estudo e controle (0,001 vs. 0; p = 0,25, p = 1, respectivamente).
Frequências dos genótipos de UGRP2 PNU e alelos
| PNU | Genótipo/Alelo | Controles (n = 105) | Casos (n = 114) | OR (IC 95%) | p‐valor |
|---|---|---|---|---|---|
| n (%) | n (%) | ||||
| IVS1‐189G>A | G/G | 101 (96) | 109 (96) | 1,00 (referência) | 0,092a |
| G/A | 4 (4) | 5 (4) | 1,00 (0‐0) | ||
| A/A | 0 (0) | 0 (0) | ‐ | ||
| Ac | 0,02 | 0,02 | 1,00 (0‐0) | 1b | |
| IVS1‐89T>G | T/T | 99 (94) | 99 (87) | 1,00 (referência) | 0,012a |
| T/G | 6 (6) | 15 (13) | 2,50 (0,75‐8,37) | ||
| G/G | 0 (0) | 0 (0) | ‐ | ||
| Gc | 0,03 | 0,07 | 2,39 (0,79‐7,81) | 0,013a | |
| 201delC | C/C | 105 (100) | 106 (93) | 1,00 (referência) | 0,0097a |
| C/delC | 0 (0) | 8 (7) | 5 (1,25‐20) | ||
| delC/delC | 0 (0) | 0 (0) | ‐ | ||
| delCc | 0,00 | 0,003 | 4,68 (1,0‐9,2) | 0,037b | |
| IVS2‐15G>A | G/G | 105 (100) | 113 (99) | 1,00 (referência) | 0,25a |
| G/A | 0 (0) | 1 (1) | 0,99 (0,07‐10) | ||
| A/A | 0 (0) | 0 (0) | ‐ | ||
| Ac | 0,00 | 0,01 | 0,99 (0,8‐11,15) | 1a |
Del, deleção; IC 95%, intervalo de confiança de 95%; n (%), frequência; OR, odds ratio; PNU, polimorfismo de nucleotídeo único.
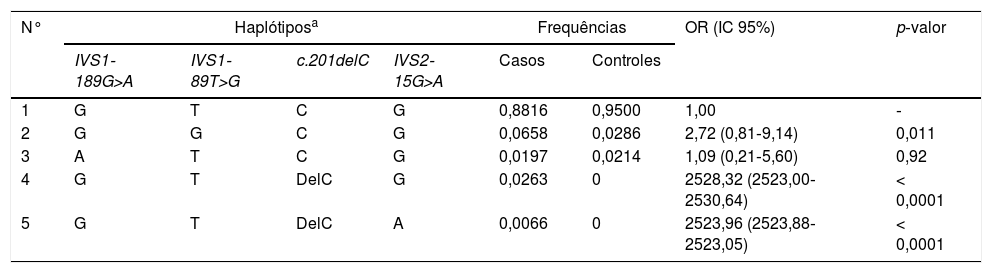
Em nosso estudo, verificamos que os PNU do Ugrp2 (c.201delC) e (IVS2‐15G>A) apresentavam o maior DL (r’= 0.434511). A análise de haplótipos dos quatro PNU foi feita e verificou‐se que alguns haplótipos apresentavam forte correlação com HTF (p = 0,049) (tabela 3). Observamos que os haplótipos GTdelCG e GTdelCA eram um fator de risco potencial para HTF (p = 0,0001 e p = 0,0001, respectivamente), enquanto o haplótipo GTCG foi encontrado em ambos os grupos.
Associações de risco de HTF e frequências de haplótipos com base nos PNU observados em UGRP2 no grupo HTF e controles
| N° | Haplótiposa | Frequências | OR (IC 95%) | p‐valor | ||||
|---|---|---|---|---|---|---|---|---|
| IVS1‐189G>A | IVS1‐89T>G | c.201delC | IVS2‐15G>A | Casos | Controles | |||
| 1 | G | T | C | G | 0,8816 | 0,9500 | 1,00 | ‐ |
| 2 | G | G | C | G | 0,0658 | 0,0286 | 2,72 (0,81‐9,14) | 0,011 |
| 3 | A | T | C | G | 0,0197 | 0,0214 | 1,09 (0,21‐5,60) | 0,92 |
| 4 | G | T | DelC | G | 0,0263 | 0 | 2528,32 (2523,00‐2530,64) | < 0,0001 |
| 5 | G | T | DelC | A | 0,0066 | 0 | 2523,96 (2523,88‐2523,05) | < 0,0001 |
HTF, hipertrofia de tonsila faríngea; IC 95%, intervalo de confiança de 95%; OR, odds ratio.
A análise dos genótipos mostrou uma forte correlação com fenótipos de HTF para alguns genótipos. Os PNU do Ugrp2 (c.201delC) CdelC e Ugrp2 (IVS1‐89T>G) TG foram mais comumente encontrados em crianças com HTF‐alérgicas e HTF‐asmáticas do que nos controles (OR = 2,1, IC 95% = 1,33‐7,24, p = 0,006 e OR = 2,85, IC 95% = 1,34‐6,10, p = 0,005, respectivamente). Além disso, os genótipos do Ugrp2 (IVS1‐189G>A) GG e (IVS1‐89T>G) TG foram mais comumente encontrados em pacientes com HTF que dormiam de boca aberta do que em crianças saudáveis (OR = 7,08, IC 95% = 3,33‐15,04, p = 0,28 e OR = 15,91, IC 95% = 1,84‐137,19, p = 0,94, respectivamente). As frequências dos genótipos do Ugrp2 (IVS1‐189G> A) GG e (IVS1‐89T>G) TT, TG foram mais comuns nos pacientes com HTF e apneia do sono testemunhada do que nos controles (OR = 7,54, IC 95% = 3,53‐16,07, p = 0,56, OR = 9,01, IC 95% = 4,10‐19,81, p = 0,31 e OR = 11,76, IC 95% = 1,23‐112,67, p = 0,30, respectivamente). O modelo da regressão logística mostrou que as frequências dos genótipos do Ugrp2 (IVS1‐189G>A) GG e (IVS1‐89T>G) TG eram maiores em pacientes com ronco do que no grupo controle (OR = 6,74, IC 95% = 3,21‐ 14,14, p = 0,043 e OR = 16,95, IC 95% = 1,95‐147,31, p = 0,88, respectivamente).
A análise dos haplótipos mostrou uma relação significativa entre o haplótipo GGCG e asma (OR = 7,16, IC 95% = 2,23‐22,98, p = 0,0012). Além disso, os haplótipos GTdelCG e GTdelCA foram encontrados em frequências significativamente mais altas em pacientes com HTF com ronco e apneia do sono testemunhada do que em controles (para ronco: OR = 2787,87, IC 95% = 2786,45‐2789,29, p = 0,0001 e OR = 2887,47, IC 95% = 27881,41‐2790,32, p = 0,000, respectivamente). Para apneia do sono testemunhada: OR = 2608,55, IC 95% = 2600,16‐2670,05, p = 0,0001 e OR = 2618,84, IC 95% = 2601,16‐26,45, p = 0,0001, respectivamente.
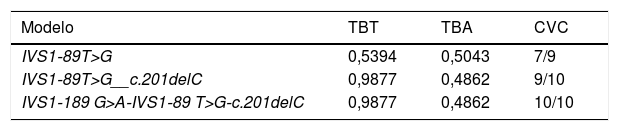
Interações PNU‐PNUA análise por MDR dos PNU no gene Ugrp2 revelou interações estatisticamente significativas (tabela 4). Cada modelo aprimorado em todas as combinações possíveis foi avaliado através de TBA, Teste de Precisão Equilibrada; CVC, Consistência de Validação Cruzada e nível de significância. Encontramos três modelos preditivos para HTF. O modelo de locus único para Ugrp2 (IVS1‐89T>G) foi identificado como um fator de risco confiável para a predição de HTF. Esse modelo de locus único demonstrou os efeitos do polimorfismo do gene Ugrp2 (IVS1‐89T>G) TG. A presença dessa mutação aumentou o risco de HTF 2,5 vezes e seu alelo menor foi colocado no grupo de alto risco para HTF (OR = 2,50, IC 95% = 0,7465‐8,3729). O modelo de dois locus para Ugrp2 (IVS1‐89T>G_c.201delC) mostrou uma associação um pouco menos convincente com o diagnóstico de HTF. Os genótipos homozigotos do tipo selvagem, bem como esses PNU, foram colocados no grupo de baixo risco, enquanto os diplótipos TG + CC e TT + CdelC foram colocados no grupo de alto risco para HTF (OR = 4,0574, IC 95% = 1,2763‐ 12.8986). O modelo de três locus para o gene Ugrp2 (IVS1‐189G>A_IVS1‐89T>G_c.201delC) foi identificado como o terceiro melhor preditor do risco de HTF. Portanto, os genótipos homozigotos do tipo selvagem, juntamente com esses PNU, também foram colocados no grupo de baixo risco. No entanto, os triplótipos GG + TT + CdelC e GG + TG + CC foram colocados no grupo de alto risco para HTF (OR = 3,9375, IC 95% = 1,1936‐12,9881).
Análise da redução da dimensionalidade multifatorial dos PNU no UGRP2
| Modelo | TBT | TBA | CVC |
|---|---|---|---|
| IVS1‐89T>G | 0,5394 | 0,5043 | 7/9 |
| IVS1‐89T>G__c.201delC | 0,9877 | 0,4862 | 9/10 |
| IVS1‐189 G>A‐IVS1‐89 T>G‐c.201delC | 0,9877 | 0,4862 | 10/10 |
CVC, consistência de validação cruzada; TBA, teste de precisão equilibrada; TBT, teste de treinamento equilibrado.
p‐valor < 0,0001.
Outro modelo de interação, determinado empiricamente pelo teste de permutação, foi o modelo de dois fatores que analisou a combinação dos alelos do gene Ugrp2 (IVS1‐189G>A) e (c.201delC) com asma. Foi observado que essas combinações estão associadas a um alto e baixo risco para HTF com um TBA de 60,6% e um CVC de 10/10 (p = 0,003). No entanto, a combinação GG + CdelC + asma foi colocada no grupo de alto risco para HTF (OR = 3,3973, IC 95% = 1,4172‐8,1440). Além disso, foi observado que as combinações dos alelos do gene Ugrp2 (IVS1‐89T>G) e (c.201delC) com alergias estavam associadas a um alto e baixo risco para HTF, com um TBA de 63,2% e um CVC de 9/10 (p = 0,0007). No entanto, a combinação TT + CdelC + alergia foi colocada no grupo de alto risco para HTF (OR = 2,4681, IC 95% = 0,2329‐26,1529).
DiscussãoNeste estudo, analisamos as associações entre polimorfismos do gene Ugrp2 e certos fenótipos, rastreamos uma população pediátrica com HTF e sem HTF. A UGRP2 (também chamada de High In Normal‐1 [HIN‐1]) é uma nova citocina que induz a diferenciação de células epiteliais e funções no crescimento celular negativo.9,24 Que seja de nosso conhecimento, nosso estudo é o primeiro a avaliar as relações entre PNU do Ugrp2 e risco de HTF na população pediátrica turca. Os resultados do nosso estudo indicaram associação significativa entre certos genótipos, haplótipos, diplótipos e triplótipos do gene Ugrp2 e a patogênese de HTF, alergias e asma.
O gene Ugrp2 está localizado no cromossomo 5q35 do genoma humano. O cromossoma 5q31‐36 contém um locus de susceptibilidade à asma, consiste em vários genes associados à inflamação, a certas citocinas e ao fator estimulador de colônias de granulócitos‐macrófagos‐2 (GM‐CSF2).8,25 A expressão do gene Ugrp2 é de regulação descendente na polipose nasal através da diferenciação de células epiteliais das vias aéreas superiores humanas, sugere que esse gene tem um papel na diferenciação de células epiteliais mucinosas, como os tecidos tonsila faríngeas.8,26
A proteína UGRP1 é um membro da superfamília SCGB. A UGRP1 e a UGRP2 têm certas semelhanças entre suas sequências de aminoácidos, especialmente no domínio antiflamina, responsável pelas atividades anti‐inflamatórias e imunomoduladoras da UGRP2, que tem funções anti‐inflamatórias.27,28 Estudos recentes demonstraram que a UGRP1 está fortemente associada à asma e à inflamação das vias aéreas alérgicas (http://omim.org/entry/606531).29,30 Portanto, considerando a literatura atual, sugerimos que a UGRP2 também pode estar associada à patogênese da HTF e seus fenótipos relacionados, como asma e alergias.
No presente estudo, identificamos quatro PNU no gene Ugrp2 (IVS1‐189G>A, IVS1‐89T>G, c.201delC e IVS2‐15G>A). Observamos também que crianças com HTF apresentavam mutação heterozigota no gene Ugrp2 (IVS1‐189G>A). No entanto, a frequência desse alelo foi baixa (4%) e era semelhante à frequência observada no grupo controle saudável. Além disso, observamos que a frequência de HTF em pacientes com o genótipo Ugrp2 (IVS2‐15G>A) GA foi menor do que em pacientes com o genótipo GG; entretanto, essa diferença não foi estatisticamente significante.
Os resultados deste estudo também indicaram um aumento de 2,3 vezes no risco de HTF na presença do alelo G para o genótipo Ugrp2 (IVS1‐89T>G) quando comparado com o alelo T. O genótipo TG foi significativamente mais comum em crianças com HTF do que nos controles e pareceu estar associado a um aumento de 2,5 vezes no risco de desenvolver HTF em comparação com o genótipo TT do tipo selvagem. Também determinamos que a mutação Ugrp2 (c.201delC) foi associada a um aumento de 4,6 vezes no risco de desenvolver HTF. Além disso, havia mais crianças no grupo HTF com o genótipo Ugrp2 (c.201delC) CdelC do que no grupo controle; essas crianças eram cinco vezes mais propensas a desenvolver HTF do que as crianças com o genótipo CC.
A HTF pode causar várias condições de comorbidade, como apneia do sono, doenças atópicas, otite crônica com efusão e sinusite.2,3 Asma e alergias são as doenças atópicas mais comuns em crianças com HTF, pois compartilham um quadro genético comum, bem como uma via imunológica similar.3,31 Não surpreendentemente, a frequência de alergias e asma foi maior em crianças com HTF do que em crianças sem HTF neste estudo. No entanto, a presença de asma e alergias no grupo controle pode refletir etiologias multifatoriais genéticas e ambientais para esses distúrbios.32,33 Também verificamos que os genótipos Ugrp2 (c.201delC) CdelC e (IVS1‐89T>G) TG eram os mais comuns em crianças com HTF alérgica e HTF asmática. Além disso, a combinação de Ugrp2 (IVS1‐189G>A_c.201delC) GG + CdelC + asma e (IVS1‐89T>G_c.201delC) TT + CdelC + alergias foram associadas com um aumento de 3,3 e 2,4 vezes no risco de HTF, respectivamente. A UGRP2 é uma pequena proteína secretória altamente expressa nos tecidos epiteliais das vias aéreas.8–10 A expressão da UGRP2 está associada a citocinas e citocinas pró‐inflamatórias que desempenham um papel crítico na HTF.5,6,26 Nossos resultados sugerem que alguns PNU e combinações de PNU podem afetar a expressão de Ugrp2, induzir mudanças na expressão de citocinas, levar a uma resposta imune local e inflamação das vias aéreas superiores; isso aumenta o risco de asma e reações alérgicas em crianças com HTF. Nossos achados são consistentes com os relatados anteriormente e demonstraram os efeitos do Ugrp2 sobre a inflamação.29,30 No entanto, outras análises funcionais in vitro devem ser feitas nessas crianças para investigar o desenvolvimento de HA no futuro.
Determinamos que os genótipos heterozigotos Ugrp2 (IVS1‐189G>A)/tipo selvagem e (IVS1‐89T>G)/tipo selvagem foram os mais comuns em pacientes que dormem de boca aberta, apneia do sono e ronco. Por outro lado, um estudo anterior descobriu que a mutação UGRP2 (IVS1‐89) estava presente em pacientes com polipose nasal e no grupo controle com frequências semelhantes.10 É possível que os PNU em questão, juntamente com alguns fatores ambientais, possam contribuir para uma predisposição hereditária à HTF e a alguns dos seus fenótipos.
Os resultados do sequenciamento indicaram que a mutação Ugrp2 (c.201delC) está localizada em um exon, enquanto os outros três PNU estão localizados em introns. PNU em regiões de não codificação afetam o splicing pré‐mRNA; PNU nas áreas de codificação afetam a sequência de aminoácidos e desempenham papéis significativos em doenças genéticas humanas.34 Nesse contexto, a mutação Ugrp2 (c.201delC) (p.Val68fs) é uma mutação do tipo frameshift resultante da exclusão de uma das três bases de citosina (CCC) geralmente presentes na posição 226da sequência do mRNA, leva a um frameshift após o códon 68 [Valina (Val)] do gene Ugrp2. A mutação Ugrp2 (c.201delC) altera o quadro de leitura translacional do mRNA traduzido putativamente, bem como a expressão de Ugrp2’; a proteína mutante resultante provavelmente altera a atividade proteica da UGRP2 (Q96QR1).35 Esses resultados sugerem que as mutações do gene Ugrp2 (IVS1‐89T>G) e (c.201delC) podem desempenhar um papel na fisiopatologia da HTF, alergias e asma. No entanto, estudos adicionais são necessários para elucidar a importância desses PNU em HTF e seus fenótipos relacionados.
As análises de associação baseadas em haplótipos, diplótipos e triplótipos foram mais efetivas e informativas do que as análises baseadas em alelos e genótipos.36 Em nosso estudo, a análise da associação de haplótipos revelou que os haplótipos GTdelCG ou GTdelCA portadores do alelo delC do gene Ugrp2 (c.201delC) estavam associados com um risco significativamente maior de HTF, ronco e apneia do sono testemunhada. Isso foi possivelmente devido ao fato de que as mutações do Ugrp2 (c.201delC) e (IVS2‐15G>A) estavam fortemente ligadas uma à outra (r2 ≥ 0,33), indica que essa região pode ser herdada em conjunto.37
O MDR é um método livre de modelo (ou seja, um método sem modelo genético presumido) projetado para detectar interações PNU‐PNU ou PNU‐fenótipo em estudos de caso‐controles na ausência de efeitos significativos. O MDR tornou‐se um dos programas mais eficazes para estudos de associação genética e para a compreensão de traços complexos.21–23 Para as interações PNU‐PNU e seus efeitos, as análises de associação baseadas em genótipos, diplótipos ou triplótipos provavelmente serão mais informativas do que análises de associação baseadas em haplótipos, genótipos ou alelos. No presente estudo, os resultados do MDR sugeriram que o genótipo Ugrp2 (IVS1‐89T>G) TG, os diplótipos (IVS1‐89T>G_c.201delC) TG + CC, TT + CdelC e os triplótipos (IVS1‐189G>A_IVS1‐89T>G_c.201delC) GG + TT + CdelC, GG + TG + CC estavam associados com um risco 2,5, 2,5, ∞‐, ∞‐ e 2,5 vezes maior de HTF em crianças, respectivamente. Os resultados anteriormente mencionados apoiam um modelo que mostra que fortes interações entre esses polimorfismos e alguns fenótipos podem levar a uma maior susceptibilidade à HTF.
Frequências de PNU relacionados ao gene Ugrp2 em diferentes populações saudáveis em todo o mundo estão disponíveis em bancos de dados online (www.hapmap.org e www.ncbi.nlm.nih.gov/snp), mas sua aplicabilidade é limitada. No entanto, as frequências dos alelos e as taxas de polimorfismos para esse gene em controles saudáveis em nosso estudo foram diferentes das frequências relatadas nesses bancos de dados, mas eram similares a um estudo anterior feito em uma população turca.10 Essas inconsistências nas frequências de alelos menores dos polimorfismos do gene Ugrp2 em indivíduos saudáveis demonstram a importância da distribuição geográfica, da etnia e do tamanho da amostra em estudos de associação.36 As crianças incluídas neste estudo viviam em uma localização geográfica similar. No entanto, uma potencial limitação de nosso estudo é que necessitávamos de uma coorte hospitalar e, portanto, nos faltaram dados sobre disparidades étnicas e estratificação populacional.
Outra limitação do nosso estudo foi o tamanho de amostra relativamente pequeno. Isto é particularmente importante porque as classificações fenotípicas com vários critérios de seleção foram aplicadas à seleção de controles neste estudo. Uma limitação adicional pode ser a inclusão de indivíduos clinicamente diagnosticados apenas com o grau 2, 3, ou 4 de HTF de Parikh, o que leva à ausência de análises genéticas em pacientes com tonsila faríngeas menores. Considerando as limitações acima, outros estudos funcionais são necessários com um grupo de estudo maior, composto por amostras independentes e coortes com base familiar para elucidar a relação entre polimorfismos do gene Ugrp2 e HTF.
ConclusãoEste estudo identificou vários PNU no gene Ugrp2 associados ao aumento da suscetibilidade para HTF e fenótipos clínicos relacionados com a HTF. Nossos resultados demonstraram o papel potencial de Ugrp2 na patogênese da HTF e servem como dados preliminares para estudos futuros.
Conflitos de interesseOs autores declaram não haver conflitos de interesse.
Esse trabalho foi aprovado pelo Comitê de Ética da Universidade de Hacettepe e recebeu apoio financeiro pela Unidade de Coordenação do Projeto de Pesquisa Científica da Universidade Hacettepe (Projeto n° 2012‐898). Não houve envolvimento no desenho ou na condução do estudo; coleta, gestão, análise ou interpretação dos dados; ou na preparação, revisão ou aprovação do manuscrito.
Como citar este artigo: Atilla MH, Özdaş S, Özdaş T, Baştimur S, Muz SE, Öz I, et al. Association of Ugrp2 gene polymorphisms with adenoid hypertrophy in the pediatric population. Braz J Otorhinolaryngol. 2018;84:599–607.
A revisão por pares é da responsabilidade da Associação Brasileira de Otorrinolaringologia e Cirurgia Cérvico‐Facial.