A epistaxe recorrente é uma doença comumente vista por especialistas em otorrinolaringologia, médicos de emergência e pediatras. O fato de que muitas modalidades de tratamento estejam sendo pesquisadas e nenhum método único de tratamento seja universalmente aceito apoiam ainda mais essa informação.
ObjetivoComparar a eficácia clínica do uso de pomada antisséptica tópica, pomada descongestionante tópica e tratamentos de cauterização química, que são frequentemente usados em epistaxe anterior recorrente, tanto isoladamente como em combinação.
MétodoEntre agosto de 2017 e fevereiro de 2018, 137 pacientes diagnosticados com epistaxe anterior recorrente foram divididos aleatoriamente em 5 grupos. O grupo I foi tratado com pomada antisséptica tópica, o grupo II com pomada descongestionante tópica, o grupo III foi submetido a cauterização química, o grupo IV foi tratado com pomada antisséptica tópica+cauterização química e o grupo V com pomada descongestionante tópica+tratamento de cauterização química. Todos os pacientes foram contatados por telefone 2 semanas e um mês após o tratamento e perguntados sobre a presença (falha) ou ausência (sucesso) de pelo menos um episódio de epistaxe. Pacientes com comorbidades foram excluídos. O sucesso do tratamento foi analisado estatisticamente.
ResultadosNão houve diferença significante (p> 0,05) entre os grupos em relação à taxa de sucesso no 15° dia após o tratamento. Os grupos IV e V tiveram maiores taxas de sucesso no 30° dia após o tratamento em comparação com os grupo I e II (p<0,05). No grupo III, o sucesso do tratamento no 30° dia não foi diferente dos outros 4 grupos (p> 0,05).
ConclusãoEmbora o número de pacientes que melhoraram com a cauterização química (grupo III) tenha sido maior em nosso estudo, nenhuma diferença significante foi observada nas modalidades de tratamento único (grupos I – III) no 14° dia e no 30° dia após o tratamento. Embora não tenha sido observada diferença estatisticamente significante entre os tratamentos combinados (grupos IV – V) e os tratamentos simples (grupos I – III) na 2ª semana após o tratamento, os tratamentos combinados foram significantemente mais eficazes no 1° mês.
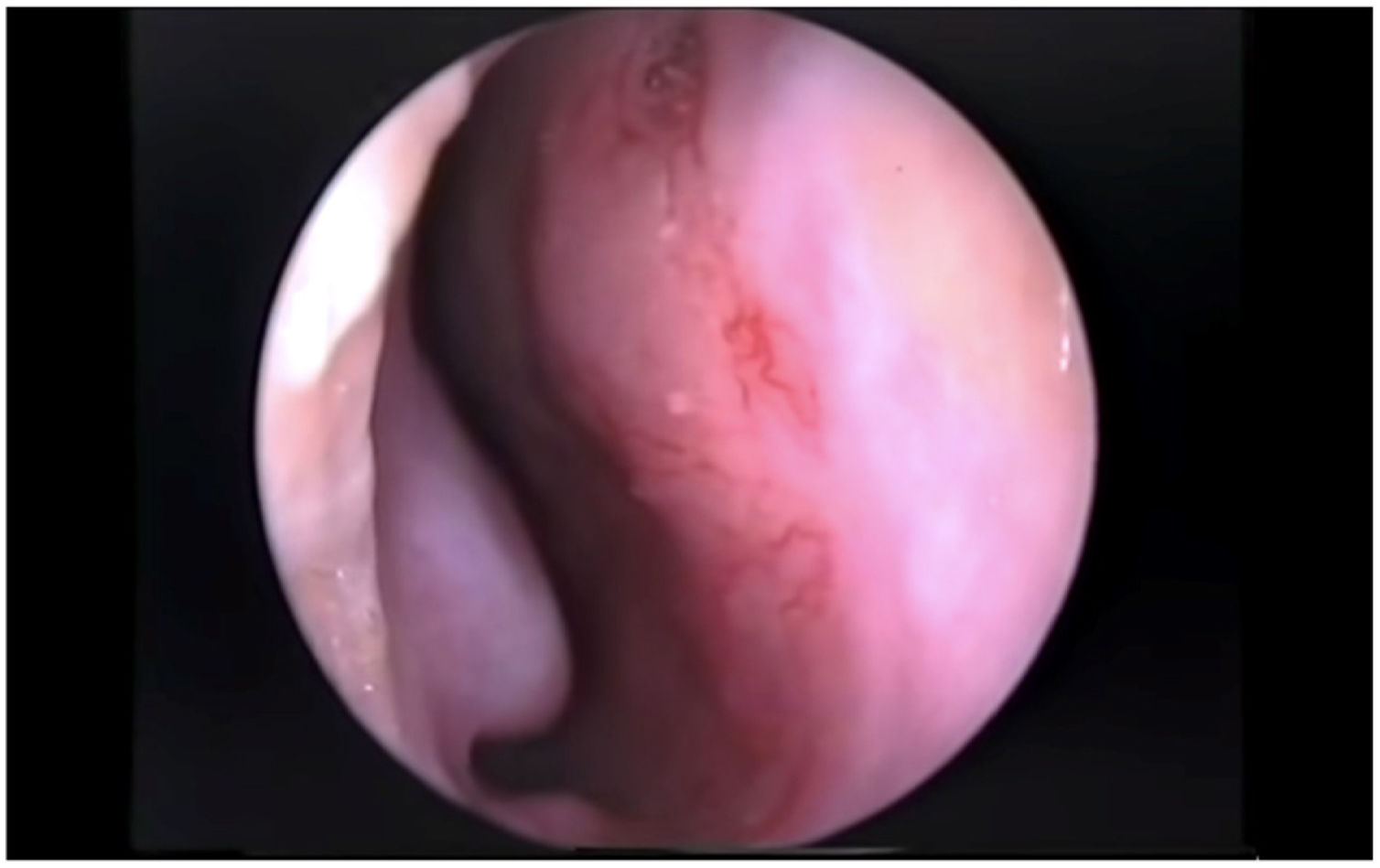
A epistaxe, ou sangramento nasal, é observada em 60% da população. Oitenta por cento desses casos têm origem na área de Little (plexo de Kiesselbach), região anterior do septo nasal, e são chamados de epistaxe anterior (fig. 1).1 São casos comumente vistos por otorrinolaringologistas, pediatras e médicos de pronto‐socorro.2 A epistaxe anterior que se origina da área de Little pode ser recorrente, desenvolver‐se espontaneamente e ser interrompida facilmente pela pressão digital nas laterais do nariz. Não apresenta risco de morte, mas causa grande ansiedade nos pacientes e seus parentes.3 A epistaxe recorrente geralmente está associada à presença de crostas, vestibulite nasal, rinossinusite, trauma digital (fungar, cutucar o nariz), mas geralmente uma causa direta não é encontrada.4 Portanto, pomadas tópicas que incluem óleo e descongestionantes e que hidratam as cavidades nasais têm um papel no tratamento.5 A colonização nasal por Staphylococcus aureus também é considerada como tendo um papel e, portanto, o tratamento com uma pomada antisséptica também pode ser importante.6 O tratamento da telangiectasia vascular, detectado pelo exame rinoscópico anterior, por cauterização química, é um método opcional de tratamento que pode ser aplicado em ambientes clínicos.7 É um fato conhecido que nenhum método único de tratamento foi aceito universalmente para o tratamento da epistaxe recorrente.8 Nosso objetivo neste estudo foi comparar a eficácia clínica de tratamentos frequentemente usados para epistaxe anterior recorrente, tanto isoladamente quanto combinados (figura 1).
MétodoComitê de ÉticaEste estudo foi feito após aprovação do comitê de ética local (Comitê de Ética Número: 2017‐230) como um ensaio clínico prospectivo randomizado.
Seleção dos pacientesEste estudo incluiu 137 pacientes com epistaxe recorrente tratados em nossa clínica, portadores de telangiectasias vasculares localizadas na área de Little segundo a avaliação rinoscópica anterior e com diagnóstico de epistaxe recorrente anterior entre agosto de 2017 e fevereiro de 2018. Pacientes nos quais se pensava a telangiectasia anterior do septo nasal ser a causa da hemorragia foram aleatoriamente agrupados para receber tratamentos diferentes.
Planejamento do tratamentoPomada antisséptica local que incluiu cloridrato de oxitetraciclina‐sulfato de polimixina B (Terramicina, Pfizer Corp., Istambul, Turquia) e pomada descongestionante local que incluiu efedrina‐nafazolina (Sulfarhin‐Santa Farma Corp. Istambul, Turquia) foram prescritos aos pacientes para tratamento tópico. Os pacientes foram instruídos a aplicá‐las na narina, no lado da lesão, duas vezes ao dia, seguido de compressão local, por duas semanas.
A cauterização química foi feita com bastões de nitrato de prata. A anestesia local antes do procedimento foi feita com chumaços de algodão embebidos em 2mL de lidocaína a 10% (Xilocaína 10% Spray, Astra Zeneca Corp. Istambul, Turquia). Após colocá‐los nas narinas por 10 minutos, o lado cauterizador do bastão de nitrato de prata (75% de nitrato de prata, 25% de nitrato de potássio, Selam Medical Corp., Istambul, Turquia) foi aplicado por alguns segundos na área de telangiectasia até formação de uma área esbranquiçada. Foram tomadas precauções para evitar danos por cauterização na mucosa nasal saudável.
AgrupamentoOs pacientes foram divididos em cinco grupos através de randomização simples. No contexto dos critérios do estudo, os pacientes foram alocados nos grupos com a ajuda de um programa de computador que os dividiu de forma completamente aleatória, igual e independente, a despeito de participação anterior. O grupo I foi tratado com pomada antisséptica tópica, o grupo II com pomada descongestionante tópica, o grupo III foi submetido a cauterização química, o grupo IV foi tratado com pomada antisséptica tópica+cauterização química e o grupo V com pomada descongestionante tópica+cauterização química. Todos os pacientes foram contatados por telefone 2 semanas e um mês após o tratamento e perguntados sobre a presença (falha) ou ausência (sucesso) de pelo menos um episódio de epistaxe. Apenas um médico fez os contatos telefônicos e não sabia a que grupo os pacientes pertenciam.
Critérios de inclusãoPacientes com queixa de sangramento nasal unilateral que havia se repetido pelo menos 4 vezes no último mês, com telangiectasias localizadas na área de Little na avaliação rinoscópica anterior e que aceitaram o tratamento foram incluídos.
Critérios de exclusãoFumantes e pacientes que apresentavam comorbidades como doença cardiovascular crônica, microvascular, hipertensão primária crônica, diabetes mellitus tipo 1 ou 2, doença pulmonar obstrutiva crônica, asma, hiperlipidemia, hipercolesterolemia, obesidade, síndrome metabólica, uso de drogas causadoras de coagulopatia, pacientes com distúrbios hemorrágicos, rinossinusite aguda e crônica foram excluídos.
Análise estatísticaOs valores de média, desvio‐padrão, mediana, menor, maior frequência e proporção foram usados como estatística descritiva dos dados. A distribuição das variáveis foi avaliada com o teste de Kolmogorov‐Smirnov. O teste de Kruskal‐Wallis foi usado na análise de dados quantitativos independentes. O teste qui‐quadrado foi usado para analisar dados qualitativos independentes. O software SPSS 22.0 foi usado para fazer as análises estatísticas.
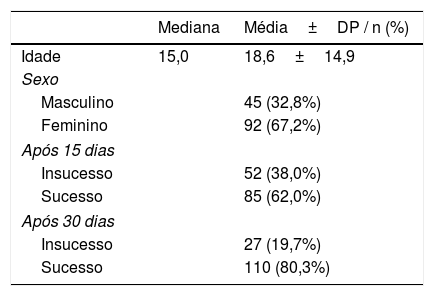
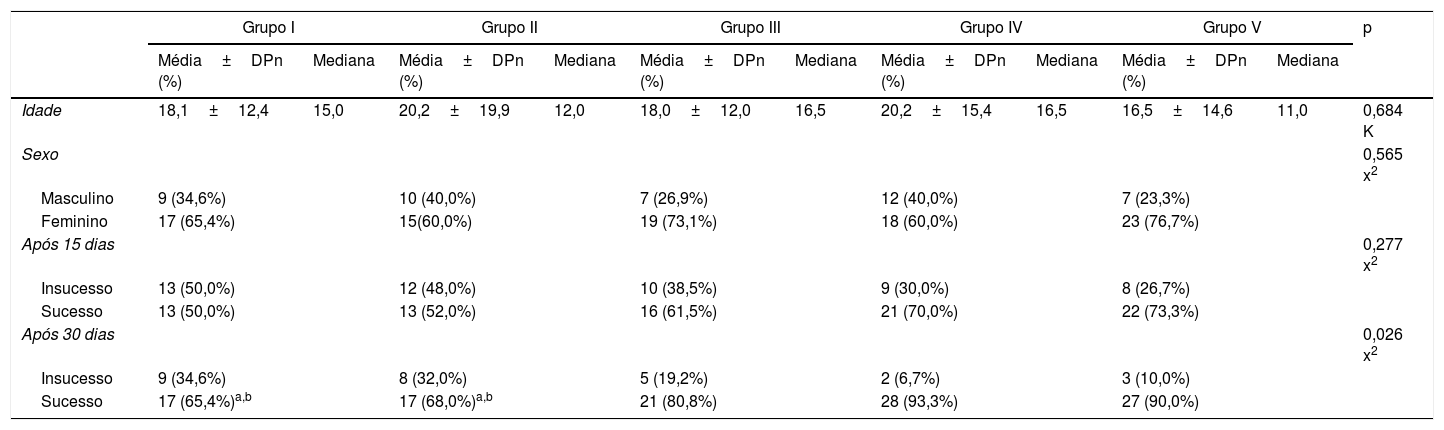
ResultadosA média de idade dos pacientes participantes do estudo foi de 18,6± 14,9 (tabela 1). A média de idade dos grupos foi de 18,1±12,4, 20,2±19,9, 18,0±12,0, 20,2±15,4 e 16,5±14,6, respectivamente. Nenhuma diferença significante foi encontrada entre as idades dos grupos (p> 0,05) (tabela 2). Havia 45 pacientes do sexo masculino e 92 do feminino no estudo e a distribuição por sexo não diferiu significantemente (p> 0,05) (tabela 2). Não houve diferença significante (p> 0,05) entre os grupos de tratamento de acordo com o sucesso no 15° dia após o tratamento (tabela 2). Os grupos IV e V apresentaram maiores taxas de sucesso no 30° dia após o tratamento em comparação com os grupos I e II (p <0,05). No grupo III, o sucesso no 30° dia de tratamento não foi diferente dos outros 4 grupos (p> 0,05) (tabela 2). Não houve diferença significante (p> 0,05) entre os grupos IV e V no 30° dia de tratamento (tabela 2).
Análise estatística dos grupos: idade, sexo e sucesso no tratamento aos 15 e 30 dias entre os grupos
| Grupo I | Grupo II | Grupo III | Grupo IV | Grupo V | p | ||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| Média±DPn (%) | Mediana | Média±DPn (%) | Mediana | Média±DPn (%) | Mediana | Média±DPn (%) | Mediana | Média±DPn (%) | Mediana | ||
| Idade | 18,1±12,4 | 15,0 | 20,2±19,9 | 12,0 | 18,0±12,0 | 16,5 | 20,2±15,4 | 16,5 | 16,5±14,6 | 11,0 | 0,684 K |
| Sexo | 0,565 x2 | ||||||||||
| Masculino | 9 (34,6%) | 10 (40,0%) | 7 (26,9%) | 12 (40,0%) | 7 (23,3%) | ||||||
| Feminino | 17 (65,4%) | 15(60,0%) | 19 (73,1%) | 18 (60,0%) | 23 (76,7%) | ||||||
| Após 15 dias | 0,277 x2 | ||||||||||
| Insucesso | 13 (50,0%) | 12 (48,0%) | 10 (38,5%) | 9 (30,0%) | 8 (26,7%) | ||||||
| Sucesso | 13 (50,0%) | 13 (52,0%) | 16 (61,5%) | 21 (70,0%) | 22 (73,3%) | ||||||
| Após 30 dias | 0,026 x2 | ||||||||||
| Insucesso | 9 (34,6%) | 8 (32,0%) | 5 (19,2%) | 2 (6,7%) | 3 (10,0%) | ||||||
| Sucesso | 17 (65,4%)a,b | 17 (68,0%)a,b | 21 (80,8%) | 28 (93,3%) | 27 (90,0%) | ||||||
K, Kruskal‐Wallis; X2, teste do qui‐quadrado,
A epistaxe recorrente é uma doença comum tratada por otorrinolaringologistas, médicos de pronto‐socorro e pediatras. O exame direto (com ou sem endoscópio flexível ou rígido) para excluir sangramento secundário à doença sistêmica geralmente revela um vaso propenso a sangramento no septo nasal anterior.9 Avaliamos prospectivamente estratégias de tratamento que foram aceitas como eficazes na literatura isoladamente ou em combinação, aleatoriamente formamos grupos de tratamento.
O tratamento da epistaxe anterior é um pouco mais fácil porque na maioria dos casos o sangramento se origina do septo anterior.10 Se não houver condição incomum, como coagulopatia, tumor, perfuração ou telangiectasia hemorrágica hereditária, o sangramento geralmente se origina do plexo de Kiesselbach. Nenhum equipamento especial é necessário para seu diagnóstico e tratamento e a maioria dos pacientes pode ser tratada como pacientes ambulatoriais, a menos que ocorra sangramento abundante.11 Para esse propósito, o uso da cauterização com nitrato de prata, que é fácil de usar, ganhou popularidade entre os otorrinolaringologistas. Entretanto, seu uso requer instruções e não é livre de complicações. A anestesia tópica é necessária para todos os casos e a maioria dos anestésicos pode apresentar efeitos adversos. Recomenda‐se precaução especial durante a cauterização bilateral do septo, devido ao risco de perfuração septal. A cauterização causa esclerose nos vasos e espessamento da mucosa.12 O uso de óleos ou pomadas no manejo da epistaxe já foi sugerido.11 Devido à hipótese de que a mucosa septal em uma região específica pode estar localmente traumatizada e resultar em sangramento recorrente, alguns autores sugeriram hidratação e uso de gotas de óleo e soro fisiológico nasal para evitar ressecamento excessivo e formação de crostas.5 Foi demonstrado por alguns autores que a vasoconstrição que a aplicação de descongestionante tópico causa na área de Little tem um papel no tratamento da epistaxe.13 A colonização nasal com Staphylococcus aureus também é considerada como tendo um papel na etiopatogênese da epistaxe e a eficácia do tratamento com pomadas antissépticas já foi demonstrada em estudos randomizados prospectivos.14
Cinco grupos foram criados aleatoriamente em nosso estudo. Os três primeiros grupos receberam pomada antisséptica, pomada descongestionante ou nitrato de prata, que são usados no tratamento de epistaxe em ambientes clínicos, e os outros dois grupos receberam combinações desses tratamentos. Embora a taxa de sucesso do tratamento tenha sido numericamente maior no grupo que recebeu nitrato de prata, nenhuma diferença estatisticamente significante pôde ser observada na taxa de sucesso no 14° dia e 30° dia nas modalidades de tratamento único. O sucesso dos tratamentos combinados não foi estatisticamente significante no 14° dia, mas foi estatisticamente significante no 30° dia.
Existem várias comparações de opções de tratamento para epistaxe na literatura. Ruddy et al. compararam tratamento antisséptico e cauterização e relataram que ambos os tratamentos foram eficazes após 4 semanas de acompanhamento no tratamento de 48 pacientes com epistaxe.15 Murthy et al. encontraram a mesma eficácia para o tratamento antisséptico e cauterização em 8 semanas de seguimento de 64 pacientes com epistaxe.16 Ao contrário, Calder et al. observaram que a combinação de pomada antisséptica e cauterização com nitrato de prata foi mais eficaz do que pomada antisséptica isoladamente no tratamento de 109 casos de epistaxe com um acompanhamento de 4 semanas.17 Kubba et al. compararam pacientes não tratados e aqueles tratados com pomada antisséptica em seu estudo prospectivo randomizado, que incluiu 103 pacientes, e relataram um melhor resultado no grupo de tratamento.18 Loughan et al. verificaram em 105 pacientes com epistaxe que o uso isolado de vaselina não era útil.19 Pomada antisséptica tópica, pomada descongestionante tópica e cauterização com nitrato de prata são comumente usados por otorrinolaringologistas em contextos clínicos. Este é o primeiro estudo na literatura que fez uma comparação prospectiva e randomizada desses tratamentos isoladamente e em combinação.
Em nosso estudo, a cessação dos episódios de sangramento foi considerada como o único parâmetro de desfecho e a taxa de sangramento e a quantidade não foram usadas para esse fim. Um motivo para essa preferência é que a quantidade de sangramento autorreferida pelos pacientes geralmente é exagerada e, portanto, não confiável. Queixas de sangramento nasal que se repetiram pelo menos 4 vezes no último mês foram levadas em consideração como um critério para questionar a quantidade de sangramento no período pré‐tratamento. Embora o uso da cessação do sangramento como único critério de sucesso tenha diminuído a taxa de sucesso neste estudo, é um desfecho importante, pois é o único fator que afeta o tratamento.
ConclusãoPomada antisséptica local, pomada descongestionante local e cauterização química apresentam resultados semelhantes para o tratamento da epistaxe. Embora não tenha sido observada diferença estatisticamente significante entre os tratamentos combinados e os tratamentos únicos na 2ª semana após o tratamento, os tratamentos combinados foram significantemente mais eficazes no 1° mês.
Aprovação éticaTodos os procedimentos feitos em estudos que envolvem participantes humanos estavam de acordo com os padrões éticos do comitê de pesquisa institucional e/ou nacional e com a Declaração de Helsinque de 1964 e suas alterações posteriores ou padrões éticos comparáveis.
Conflitos de interesseOs autores declaram não haver conflitos de interesse.
Como citar este artigo: Koçak HE, Bilece ZT, Keskin M, Ulusoy HA, Koç AK, Kaya KH. Comparison of topical treatment methods used in recurrent anterior epistaxis: a randomized clinical trial. Braz J Otorhinolaryngol. 2021;87:132–6.
A revisão por pares é da responsabilidade da Associação Brasileira de Otorrinolaringologia e Cirurgia Cérvico‐Facial.