As substâncias tóxicas presentes na fumaça do cigarro podem danificar as células ciliadas da cóclea. Esse efeito foi investigado pela mensuração das emissões otoacústicas.
ObjetivoInvestigar o impacto de estímulos nas emissões otoacústicas, comparar neonatos com e sem exposição à fumaça de cigarro durante a gestação.
MétodoTestes de emissões otoacústicas evocadas transientes, evocadas por estímulo tipo clique e emissões otoacústicas por produto de distorção, evocadas por dois tons, foram feitos em ambas as orelhas, com um aparelho Interacoustic TITAN. O estudo incluiu 105 neonatos divididos em dois grupos: um grupo de estudo, que compreendeu 47 neonatos expostos à fumaça durante a gravidez; e um grupo controle constituído por 58 neonatos que não foram expostos. Todos os participantes apresentaram triagem auditiva neonatal normal.
ResultadosNão foram encontradas diferenças estatísticas nos níveis de resposta das emissões otoacústicas por produto de distorção entre os grupos. Nos testes de emissões otoacústicas evocadas transientes, foram observados menores níveis de resposta no grupo de estudo do que no grupo controle na análise de bandas de frequências da orelha direita, com diferenças estatisticamente significantes nos sinais e relação sinal‐ruído (exceto a 1kHz).
ConclusãoO impacto da exposição ao fumo pôde ser analisado por meio das emissões otoacústicas evocadas transientes em neonatos. O efeito da exposição à fumaça durante a gravidez foi evidenciado por uma redução nos níveis das emissões otoacústicas evocadas transientes no grupo exposto. Esse mesmo efeito não foi observado para as análises feitas nos níveis das emissões otoacústicas por produto de distorção.
O fumo passivo é definido como inalação de fumaça de cigarro presente no ar. Na maioria dos países, estima‐se que 4,4% a 8,4% da população, inclusive crianças, está exposta ao tabagismo passivo no ambiente doméstico. Estima‐se que 600.000 pessoas morrem todos os anos de doenças secundárias à exposição passiva à fumaça do tabaco.1
O tabagismo passivo é especialmente prejudicial durante a gravidez, afeta negativamente o crescimento fetal. As substâncias tóxicas presentes na composição dos cigarros, como arsênico, chumbo e mercúrio, passam facilmente através da placenta e afetam o feto. Esses elementos tóxicos provocam mudanças no metabolismo, reduzem o suprimento de nutrientes e oxigênio ao feto e, no sistema auditivo, podem danificar as células ciliadas da cóclea.1–4
O impacto de substâncias tóxicas nas células ciliadas externas da cóclea pode ser medido com emissões otoacústicas (EOA). Essas emissões são sons de baixa intensidade produzidos espontaneamente a partir de vibrações geradas pela cóclea, mas também podem ser evocadas por estímulos acústicos, que refletem a saúde da orelha interna e podem ser medidos de maneira objetiva, rápida e não invasiva. Fumantes e indivíduos expostos passivamente à fumaça de cigarro exibem menores níveis de respostas de emissões otoacústicas.5–9 A exposição simultânea a ruído e monóxido de carbono induziu grandes alterações nos limiares de tons puros em todas as frequências estudadas em ratos Long‐Evans.10 A perda generalizada de células ciliadas também foi observada, as células ciliadas externas aparentam ser particularmente vulneráveis. Esses dados contribuem para um crescente conjunto de evidências que mostram que a perda auditiva após a exposição à fumaça do tabaco pode estar correlacionada com insuficiência metabólica.11
Além desses métodos tradicionais para classificação das EOA com base no estímulo usado, 12 outra abordagem classifica as EOA com base nos mecanismos de geração: distorção e/ou reflexão.13 Nas emissões otoacústicas evocadas transientes (EOAET), o mecanismo principal parece ser a reflexão, enquanto nas emissões otoacústicas por produto de distorção (EOAPD) o mecanismo é reconhecido como uma soma vetorial dos dois componentes principais, a distorção e a reflexão.14–17
Diversos estudos investigaram a influência da exposição à fumaça nas EOAs. No entanto, o impacto do tabagismo nos níveis de EOAs, de acordo com o tipo de estímulo, ainda não é conhecido. O objetivo do presente estudo é medir o impacto dos estímulos nas EOAs, comparar neonatos com e sem exposição à fumaça de cigarro durante a gestação.
MétodoUm estudo transversal foi feito na ala de alojamento conjunto da Santa Casa de Misericórdia de São Paulo, de junho de 2015 a agosto de 2016, após aprovação do Comitê de Ética em Pesquisa (parecer 771.404).
AmostraCompreendeu 105 neonatos selecionados aleatoriamente de 24 a 72 horas após o nascimento. Os neonatos foram divididos em dois grupos. O Grupo de Estudo (GE), com 47 neonatos expostos à fumaça durante a gestação, foi composto por 21 meninos e 26 meninas. O Grupo Controle (GC), com 58 neonatos sem exposição ao tabagismo durante a gestação, foi composto por 35 meninos e 23 meninas. A divisão dos grupos foi baseada nas informações relatadas pelas mães sobre seus hábitos de tabagismo.
Os critérios de inclusão e exclusão são descritos na tabela 1.
Critérios de inclusão e exclusão para o estudo
| Critério | Grupo Controle | Grupo de Estudo | |
|---|---|---|---|
| Inclusão | Mães sem histórico de uso de álcool e/ou drogas durante o período gestacional e neonatos sem fatores de risco para perda auditiva e com resultados normais na triagem auditiva neonatal, ou seja, presença de emissões otoacústicas evocadas transientes medidas em uma análise de resposta automatizada. | + | + |
| Neonatos expostos à fumaça de tabaco porque suas mães eram fumantes ativas durante a gravidez. | ‐ | + | |
| Neonatos cujas mães não foram expostas ao tabagismo passivo durante a gravidez. | + | ‐ | |
| Exclusão | Não ter condições ideais para a plena aplicação do protocolo de estudo pós‐parto. | + | + |
Todos os procedimentos (seleção dos participantes, feitura dos testes e encaminhamento dos participantes para as intervenções) foram feitos pelo mesmo fonoaudiólogo.
EquipamentoFoi usado um dispositivo Titan (Interacoustics) com módulos:
EOEPD: Dois estímulos tonais primários, f1 e f2, foram produzidos nas frequências f2 de 2, 3, 4, 5, 6 e 8kHz, relação f1/f2 = 1,22, nas intensidades de 65 e 55dB NPS para f1 e f2, respectivamente. O produto de distorção registrado e analisado foi 2f1‐f2.
EOAET: Foi produzido um estímulo tipo clique (banda de frequência 500‐5000Hz) de banda larga, não linear, com intensidade de 80dB pe NPS. As respostas foram analisadas quanto à resposta total e também pelas bandas de frequência 1, 2, 3, 4 e 5kHz (Transformada rápida de Fourier).
Protocolo de estudoA anamnese foi feita com as mães para investigar os hábitos tabagistas: uso de cigarros; primeiro uso; número de cigarros por dia nos trimestres da gravidez e no dia do parto e exposição passiva.
As EOAPD e EOAET foram registradas em sala silenciosa, à prova de som, durante o período pós‐parto (24‐72 horas). Os testes foram feitos apenas quando os neonatos estavam em sono natural e o ambiente estava silencioso.
Análise de dadosAs diferenças nas EOAPD e EOAET obtidas nas duas orelhas foram comparadas entre os grupos controle e estudo, em cada frequência, pelo teste t de Student. O nível de significância estatística adotado foi p ≤ 0,05. Posteriormente, foi feito o teste de normalidade de D’Agostino‐Pearson. Todos os dados passaram no teste de normalidade (α > 0,05, dados não mostrados).
Todas as análises foram feitas com o software GraphPad Prism 5.0.
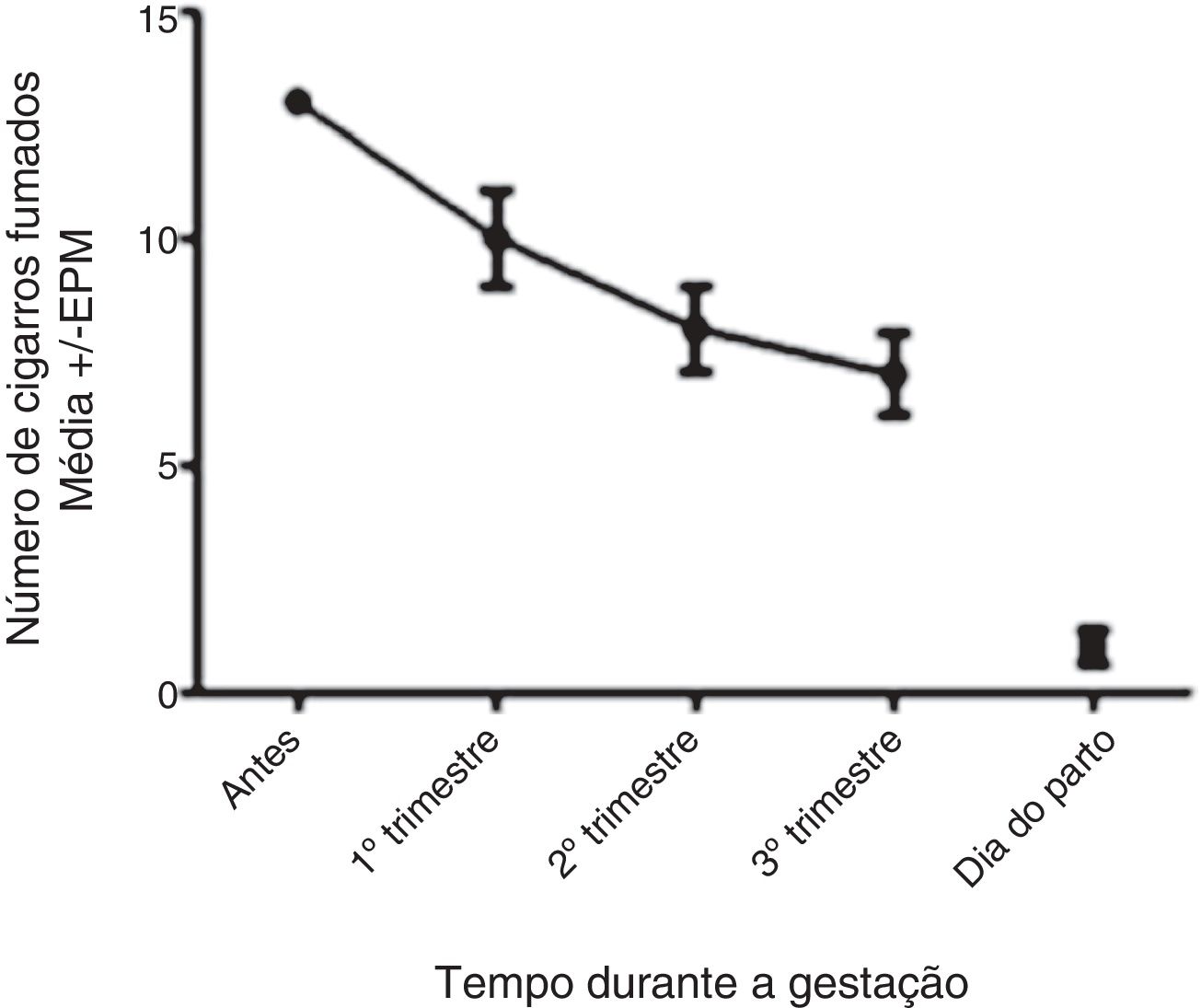
ResultadosO número de cigarros fumados pelas mães antes e durante a gravidez é apresentado na figura 1. Neste estudo, as mães fumantes reduziram o número de cigarros consumidos durante o curso da gravidez para quase zero no dia do parto.
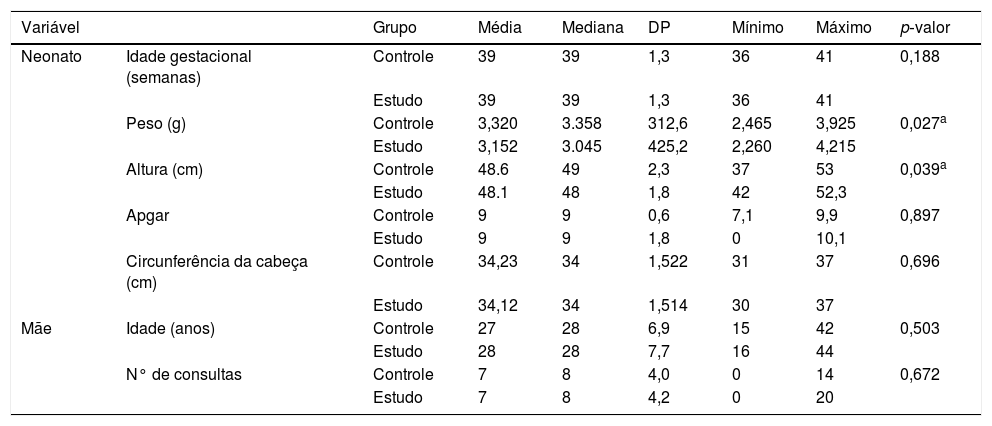
As características perinatais dos neonatos e das mães podem ser encontradas nos dados descritivos apresentados na tabela 2. Todas as variáveis estudadas foram semelhantes nos dois grupos avaliados, exceto pelo menor peso e altura dos neonatos com exposição ao tabagismo durante a gestação.
Características perinatais dos neonatos e mães nos grupos de mães fumantes e não fumantes
| Variável | Grupo | Média | Mediana | DP | Mínimo | Máximo | p‐valor | |
|---|---|---|---|---|---|---|---|---|
| Neonato | Idade gestacional (semanas) | Controle | 39 | 39 | 1,3 | 36 | 41 | 0,188 |
| Estudo | 39 | 39 | 1,3 | 36 | 41 | |||
| Peso (g) | Controle | 3,320 | 3.358 | 312,6 | 2,465 | 3,925 | 0,027a | |
| Estudo | 3,152 | 3.045 | 425,2 | 2,260 | 4,215 | |||
| Altura (cm) | Controle | 48.6 | 49 | 2,3 | 37 | 53 | 0,039a | |
| Estudo | 48.1 | 48 | 1,8 | 42 | 52,3 | |||
| Apgar | Controle | 9 | 9 | 0,6 | 7,1 | 9,9 | 0,897 | |
| Estudo | 9 | 9 | 1,8 | 0 | 10,1 | |||
| Circunferência da cabeça (cm) | Controle | 34,23 | 34 | 1,522 | 31 | 37 | 0,696 | |
| Estudo | 34,12 | 34 | 1,514 | 30 | 37 | |||
| Mãe | Idade (anos) | Controle | 27 | 28 | 6,9 | 15 | 42 | 0,503 |
| Estudo | 28 | 28 | 7,7 | 16 | 44 | |||
| N° de consultas | Controle | 7 | 8 | 4,0 | 0 | 14 | 0,672 | |
| Estudo | 7 | 8 | 4,2 | 0 | 20 | |||
As avaliações da fisiologia coclear com EOAPD e EOAET foram feitas em neonatos expostos (Grupo de Estudo) e em neonatos não expostos (Grupo Controle) ao fumo.
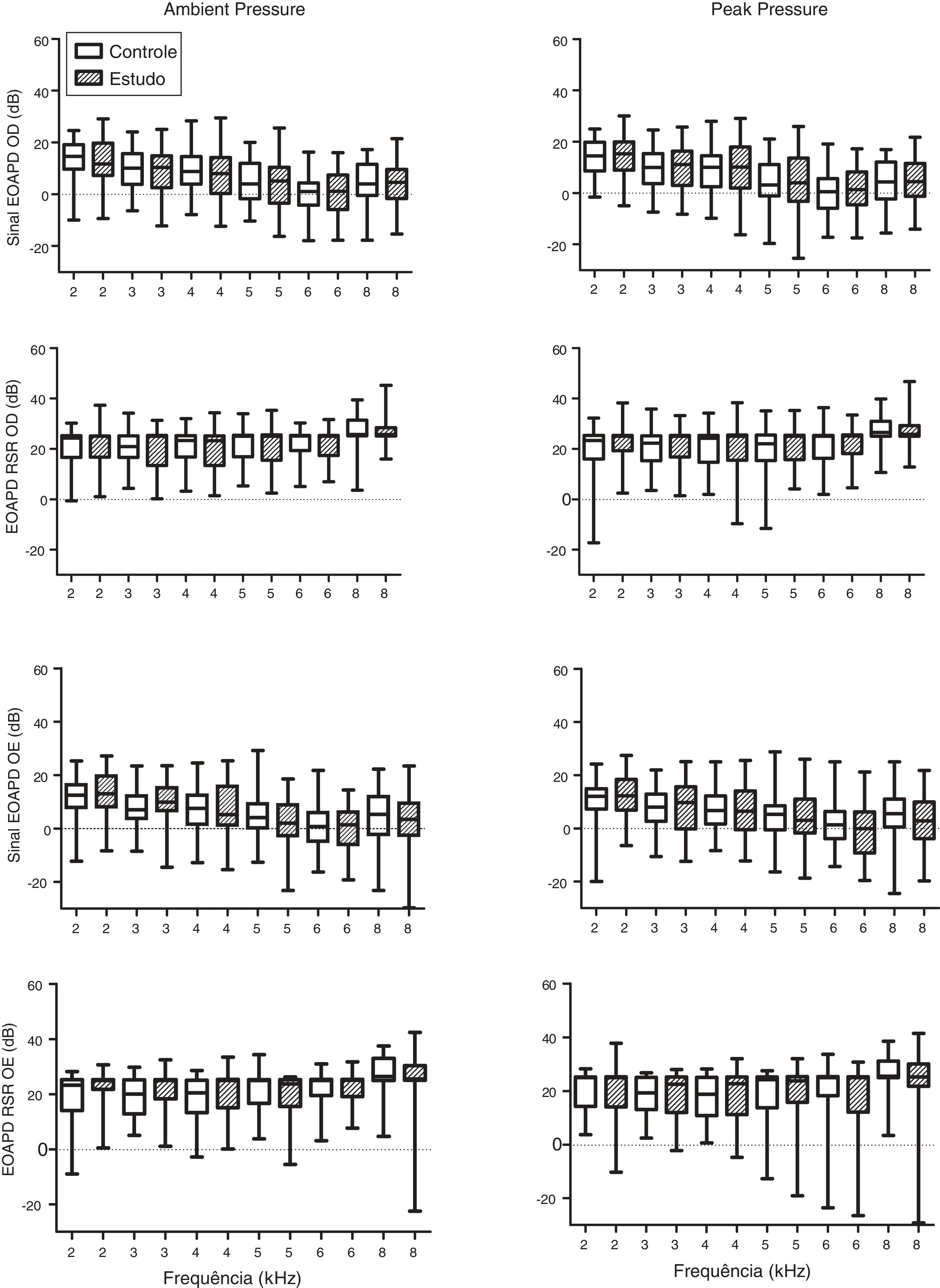
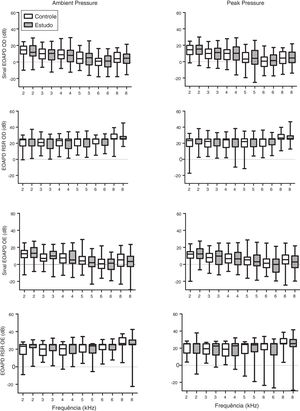
Os níveis médios de resposta do sinal das EOAPD e da relação sinal/ruído (RSR) para as frequências 2, 3, 4, 5, 6 e 8kHz para as orelhas direita e esquerda estão representados na figura 2. Não houve diferenças estatísticas nos níveis de resposta das EOAPD entre os grupos. Entretanto, níveis mais baixos para o sinal das EOAPD medidos na orelha direita foram evidentes no grupo de estudo em todas as frequências testadas.
Gráfico do tipo Box plot do sinal das EOAPD e dos níveis da relação sinal/ruído (RSR) medidos por grupo para a orelha direita (OD) e a orelha esquerda (OE). Grupo controle representado por retângulos ocos e grupo de estudo por retângulos hachurados. Não houve diferença estatística entre os grupos.
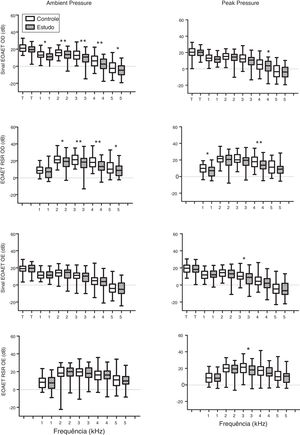
A figura 3 mostra os níveis médios de resposta ao sinal das EOAET e da relação sinal/ruído para a resposta total e as bandas de frequência 1, 2, 3, 4 e 5kHz para os grupos controle e de estudo na orelha direita (OD) e orelha esquerda (OE).
Gráfico do tipo Box plot do sinal das EOAET e dos níveis da relação sinal/ruído (RSR) medidos por grupo para a orelha direita (OD) e orelha esquerda (OE). Grupo controle representado por retângulos ocos e grupo de estudo por retângulos hachurados. Os asteriscos indicam comparação estatística entre os grupos controle e estudo por frequência. Um asterisco para p < 0,05 e dois para p < 0,01.
Níveis mais baixos de resposta foram observados no grupo de estudo do que no grupo controle na análise da banda de frequência das EOAET da orelha direita, com diferenças estatisticamente significantes nos sinais e relação sinal‐ruído (exceto a 1kHz).
DiscussãoEstudos em recém‐nascidos demonstraram o efeito prejudicial da exposição à fumaça durante a gravidez no sistema auditivo de neonatos, mostraram que essa exposição leva a uma redução nos níveis de resposta das EOAET em indivíduos sujeitos à fumaça comparados com indivíduos não expostos, independentemente do grau de exposição.5,7
A importância do estudo dos neonatos expostos ao tabagismo está na alta taxa de mães fumantes e no impacto dessa exposição na saúde. Estima‐se que, entre 2005 e 2015, mais da metade da população mundial (2,8 bilhões de pessoas) foi exposta a pelo menos uma medida de proteção contra o tabagismo.18 Com exceção das regiões africanas e do Mediterrâneo Oriental, a prevalência do tabagismo tem diminuído globalmente. No entanto, o número de fumantes na população continua alto. Cerca de 21% da população mundial com 15 anos ou mais de idade (cerca de 1,1 bilhão de pessoas) são fumantes – aproximadamente 35% de homens e 6% de mulheres. O tabaco é uma substância altamente viciante e a grande maioria dos usuários fuma diariamente.1
Na amostra de mães fumantes avaliada (grupo de estudo), observou‐se redução do hábito de fumar durante o curso da gestação (fig. 1), achado consistente com dados da literatura.1 Uma redução acentuada no consumo de cigarros foi evidente no dia do parto, próximo de zero, provavelmente devido à restrição de fumo imposta pelo ambiente hospitalar. O sangue coletado dos cordões umbilicais das mães mostrou concentrações semelhantes de cotinina (um marcador de uso de nicotina nas últimas 8 a 24 horas) em ambos os grupos, expostos e não expostos. Dado que todas as mães tiveram seus bebês por parto vaginal, com trabalho de parto de várias horas de duração, esse resultado está de acordo com o número de cigarros fumados no dia do parto, mas não mostra a exposição crônica do feto à nicotina durante o período gestacional. Portanto, a divisão dos grupos foi baseada apenas nas informações relatadas pelas mães sobre o hábito de fumar, usou‐se o método validado por Caraballo et al.19
A associação entre tabagismo e seus efeitos prejudiciais à saúde de mulheres, mães grávidas e fetos já foi claramente estabelecida.2–4 A associação entre o tabagismo durante a gravidez e o baixo peso e comprimento do feto ao nascimento também foi descrita.3 Em nosso estudo, os recém‐nascidos de mães fumantes apresentaram massa corporal e estatura, em média, de 168g e 0,5cm menor, respectivamente (p = 0,03 para ambos).
O impacto do tabagismo nas respostas audiológicas tem sido explorado na literatura na população de adultos fumantes20–24 adolescentes25 e crianças passivamente expostos,5,6,8,25 revelou alterações das respostas em baterias de avaliação audiológica como resultado da exposição ao tabagismo ativo e passivo.
Os agentes contidos no tabaco podem reduzir e/ou esgotar os níveis de oxigênio para a cóclea, explicam a redução da amplitude das EOA,25 mensurável pela avaliação das células ciliadas externas, um método objetivo, não invasivo, sensível e rápido.
Os principais resultados do presente estudo revelaram que as diferenças nos níveis de resposta das EOAET foram encontradas para várias frequências nas orelhas direita e esquerda entre os grupos controle e de estudo, com diferenças estatisticamente significantes nos sinais e relação sinal/ruído (exceto a 1kHz). Esses achados são consistentes com os do estudo de Durante et al.5 e diferentes daqueles apresentados por Korres et al.,7 que encontraram diferenças significantes nas EOAET somente a 4kHz.
As grandes variações intersubjetivas nos níveis das EOAET do presente estudo não permitem a identificação dos efeitos do tabagismo em um neonato específico, mas enfatizam o valor das medidas das EOAET na pesquisa sobre o efeito do fumo passivo.
Em contraste, os resultados obtidos com as EOAPD não revelaram efeito da exposição ao fumo durante a gestação (fig. 2). No entanto, o primeiro gráfico da figura 2 mostra níveis de resposta do sinal das EOAPD consistentemente mais baixos na orelha direita no grupo de estudo em comparação com o grupo controle.
Apenas um nível de intensidade foi usado com cada método, EOAET e EOAPD. Aplicar diferentes intensidades e configurações de estimulação afeta a sensibilidade do teste à patologia coclear e, provavelmente, ao tabagismo. Além disso, o mecanismo de geração das EOA por distorção e/ou reflexão pode ser um fator relevante.13 As emissões obtidas clinicamente são possivelmente uma mistura de dois tipos de emissões, nos quais o mecanismo de distorção é maior nas EOAPD e o de reflexão é maior nas EOAET.14–17 Um estudo recente sugere que o componente de reflexão é mais vulnerável à exposição a ototóxicos26, o que pode explicar os resultados na literatura que mostram que o efeito do tabagismo passivo nas emissões otoacústicas de neonatos é mais evidente nas EOAET, independentemente do grau de exposição.6,7 Os estudos que encontraram níveis reduzidos de respostas das EOAPD foram feitos em fumantes ativos.24–26 Os resultados do presente estudo mostraram o efeito da exposição à fumaça durante a gravidez nas medidas das EOAET em neonatos e corroboraram esses achados (fig. 3).
A contribuição deste estudo foi investigar as EOAET e as EOAPD nos mesmos neonatos, revelar a possibilidade de uma relação diferente entre os mecanismos de geração na cóclea humana e o impacto da exposição ao fumo. Estudos futuros de EOA devem ser feitos para investigar as magnitudes relativas dos dois componentes das EOAPD, a fim de proporcionar uma melhor compreensão dos mecanismos subjacentes à produção de EOAPD, após a exposição ao fumo.
ConclusãoO impacto da exposição ao fumo na cóclea pode ser detectado em neonatos com dados de triagem auditiva das EOAET. Em contraste, os dados de triagem das EOAPD da mesma população não demonstraram uma redução significante.
FinanciamentoEste trabalho recebeu apoio financeiro da Fundação de Amparo à Pesquisa do Estado de São Paulo (Fapesp) [concessão n° 014/15229‐6].
Conflitos de interesseOs autores declaram não haver conflitos de interesse.
Como citar este artigo: Durante AS, Nascimento CM, Lopes C. Otoacoustic emissions in neonates exposed to smoke during pregnancy. Braz J Otorhinolaryngol. 2021;87:193–9.
A revisão por pares é da responsabilidade da Associação Brasileira de Otorrinolaringologia e Cirurgia Cérvico‐Facial.