A apneia obstrutiva do sono é o tipo mais comum de apneia do sono, causada por obstrução completa ou parcial da via aérea superior. A obstrução nasal também é considerada como um dos fatores de risco independentes da apneia obstrutiva do sono.
ObjetivoAvaliar pacientes com apneia obstrutiva do sono.
MétodoPacientes com apneia obstrutiva do sono foram incluídos no estudo de junho a dezembro de 2015, tratados com spray de corticosteroide intranasal por quatro semanas. Vários parâmetros foram obtidos antes e após o tratamento, inclusive os escores da escala Nasal Obstruction Symptom Evaluation, do Pittsburgh Sleep Quality Index e do questionário Escala de Sonolência de Epworth.
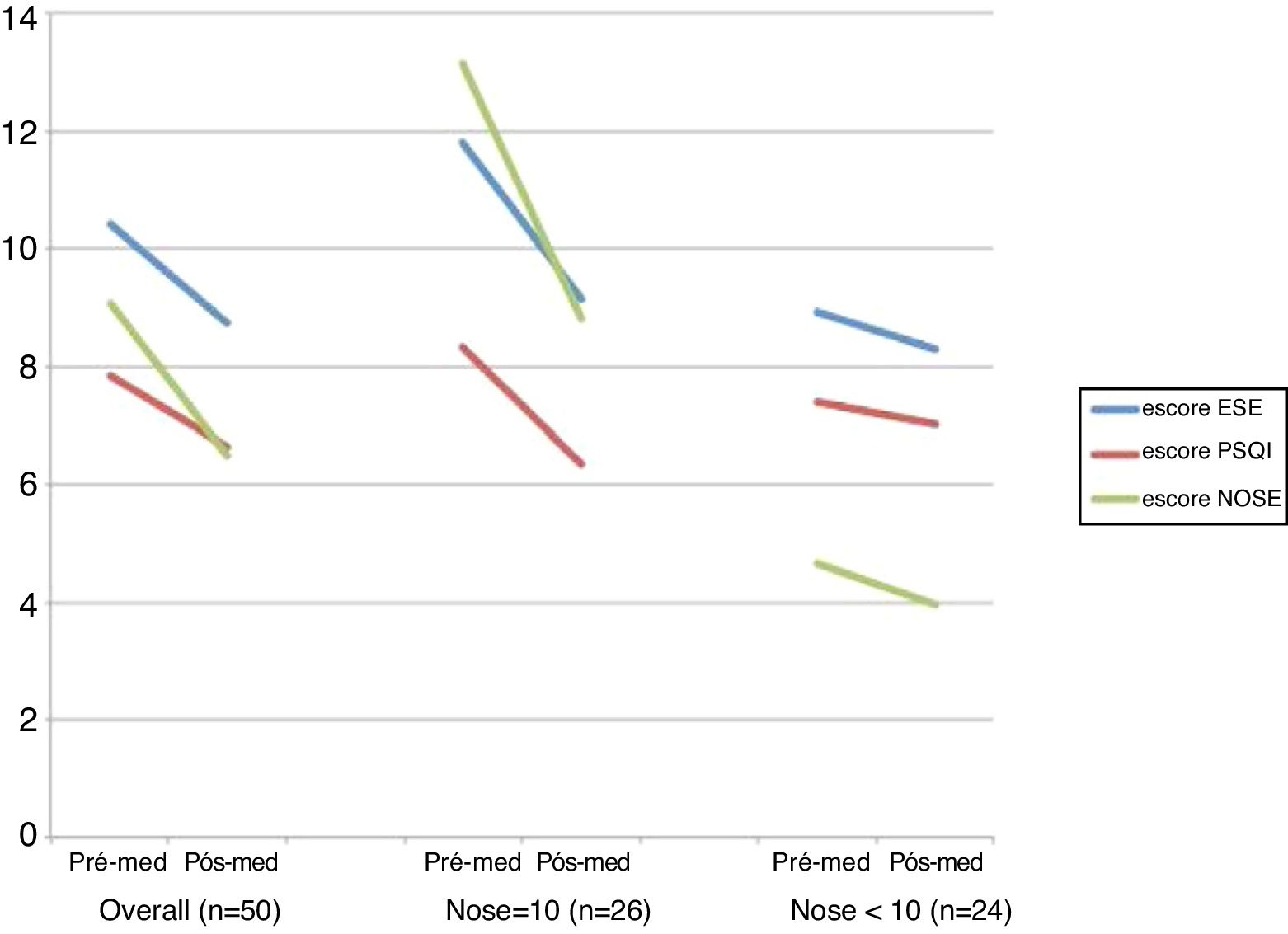
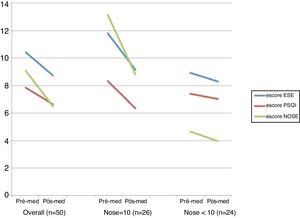
ResultadosCinquenta pacientes completaram os questionários antes e após o tratamento intranasal com fluticasona. A média de idade era de 39,7 ± 15,6 anos, com uma proporção de homens para mulheres de 3:2. Os escores pós‐tratamento da Escala de Sonolência de Epworth, do Pittsburgh Sleep Quality Index e do Nasal Obstruction Symptom Evaluation indicaram uma diminuição em comparação aos escores pré‐tratamento, de 10,4 para 8,74, 7,86 para 6,66 e 9,08 para 6,48, respectivamente. Uma diminuição significativa foi observada no grupo Nasal Obstruction Symptom Evaluation ≥ 10 em todas as três categorias, mas não no grupo Nasal Obstruction Symptom Evaluation <10.
ConclusõesOs autores concluíram que o tratamento com fluticasona intranasal pode ser útil em pacientes com apneia obstrutiva do sono relacionada a obstrução nasal para melhorar a qualidade do sono e limitar a disfunção diurna.
A apneia obstrutiva do sono (AOS) é o tipo mais comum de apneia do sono. É causada por obstrução completa ou parcial da via aérea superior. Aproximadamente 2%–4% a 32,8% dos adultos são portadores de AOS, mais comumente diagnosticada em homens de meia‐idade.1–3 A taxa de prevalência vara de acordo com as diferentes populações. A AOS é caracterizada por episódios repetitivos de respiração superficial ou pausada durante o sono, apesar do esforço para respirar. Redução na saturação de oxigênio no sangue durante o sono é tipicamente observada em pacientes com AOS.
Normalmente a AOS está relacionada ao envelhecimento, à diminuição do tônus muscular, ao aumento dos tecidos moles ao redor das vias aéreas (algumas vezes devido à obesidade) e às características estruturais.2 Os pacientes podem apresentar mais de uma dessas características. A obstrução nasal também é considerada um fator de risco independente para AOS.3 Pacientes com doenças nasais, como a rinite alérgica, podem apresentar aumento da resistência ao fluxo aéreo nasal (NAR, do inglês Nasal Airflow Resistance), o que pode contribuir para o desenvolvimento de obstrução das vias aéreas superiores durante o sono.4
Vários estudos relatam uma relação entre o ronco e AOS em pacientes com obstrução nasal por várias doenças.3,5,6 No entanto, ainda não está claro se o tratamento da obstrução nasal pode melhorar o desfecho de pacientes com AOS.
Modalidades de tratamento para AOS incluem modificações no estilo de vida, como evitar álcool e tabagismo,1 perda de peso em pacientes com sobrepeso, evitar medicações que relaxam o sistema nervoso central, pressão positiva contínua nas vias aéreas (CPAP, do inglês Continuous Positive Airway Pressure) e o uso de dispositivos de avanço mandibular.7,8 Até o momento, não há muitas evidências para apoiar o uso de medicação ou cirurgia,7,9 especialmente com base no aspecto subjetivo.
Como a obstrução nasal pode afetar substancialmente a AOS, os tratamentos para esse problema devem beneficiar alguns dos pacientes com AOS. Neste estudo, usamos a escala Nasal Obstruction Symptom Evaluation (NOSE) para comparar os resultados do tratamento com o uso de fluticasona intranasal em pacientes com diferentes graus de gravidade da obstrução nasal.
MétodoParticipantesEste estudo prospectivo foi aprovado pelo comitê de ética sob o registro CGH‐LP104003. Entre junho e dezembro de 2015, pacientes avaliados em nosso departamento de otorrinolaringologia apresentando ronco e suspeita de AOS foram solicitados a fazer um estudo de polissonografia (PSG) antes que qualquer medicamento fosse prescrito. Uma vez confirmada a AOS, definida por um índice de distúrbio respiratório ≥ 5, os pacientes foram recrutados para este estudo para ser avaliados. O consentimento informado foi obtido dos participantes. Pacientes foram excluídos do estudo caso recusassem o tratamento ou a participação no estudo. Os pacientes que haviam recebido tratamento com esteroides intranasais ou cirurgias nasais ou orais foram excluídos.
Coleta de dados e protocolo do estudoFizemos avaliações em pessoa com base em três questionários internacionalmente validados, confiáveis e amplamente usados, a saber, a escala NOSE,10 o questionário Pittsburgh Sleep Quality Index (PSQI) 11,12 e o questionário Escala de Sonolência de Epworth (ESE).13,14 Após a obtenção do consentimento informado por escrito, os pacientes foram instruídos a preencher os questionários durante a sua primeira consulta. O único medicamento prescrito foi a fluticasona intranasal (27,5 mcg de furoato de fluticasona por pulverização), borrifado uma vez ao dia em cada narina (dose diária total, 110 mcg). Cada entrevista teve a duração de 10 a 20 minutos, aproximadamente. Após quatro semanas de tratamento com corticosteroide intranasal, os questionários PSQI e ESE foram novamente respondidos, quando os pacientes retornaram à clínica.
Ferramentas de avaliaçãoA escala NOSE10 é um instrumento específico da doença validado para medir a obstrução nasal. É amplamente usado na prática otorrinolaringológica para fornecer uma medida objetiva da obstrução nasal.
O questionário PSQI foi usado para avaliar a qualidade e os distúrbios do sono durante o mês anterior. Ele consiste em duas partes. Uma parte contém 19 itens referentes à qualidade subjetiva do sono. Os quatro primeiros itens são questões abertas e os itens 5 a 19 são classificados em uma escala de 4 pontos. Os escores dos itens geram sete subescores, variam de 0 a 3: qualidade do sono, latência do sono, duração do sono, eficiência do sono, distúrbio do sono, uso de medicamentos para dormir e disfunção diurna causada pela sonolência. Os escores totais, que variam de 0 a 21, são obtidos somando‐se os sete subescores. Inúmeros estudos indicam que um escore total no PSQI ≤ 5 indica uma boa qualidade do sono, enquanto um escore total > 5 indica má qualidade do sono.11,15,16 A outra parte do PSQI contém cinco itens referentes à qualidade objetiva do sono. Esses cinco itens foram classificados em uma escala de 4 pontos e somados para obter um escore total que varia de 0 a 15.
O questionário ESE consiste em 8 perguntas classificadas em uma escala de 4 pontos, varia de 0 a 3. Um escore total entre 0 e 24 foi usado para avaliar o nível geral de sonolência diurna dos participantes e a propensão média ao sono em relação ao mês anterior. Um escore no ESE >10 indica sonolência significativa.15,16
Os participantes foram submetidos a polissonografia (PSG) diagnóstica em laboratório em nosso hospital. Todos os indivíduos incluídos foram monitorados com oximetria transcutânea de pulso. O fluxo respiratório foi medido por um termistor externo, monitor de CO2 e cânula de pressão nasal. O esforço respiratório foi registrado por meio de pletismografia respiratória por indutância. O Índice de Apneia e Hipopneia (IAH) representa o número de apneias e hipopneias por hora de sono. A apneia foi definida como uma diminuição de 90% ou mais do fluxo de ar da linha basal anterior, conforme medido por um termistor oronasal por pelo menos 10 segundos. A hipopneia foi definida como um evento obstrutivo parcial, com diminuição do fluxo de ar em mais de 30% em relação ao valor basal por pelo menos 10 segundos, de acordo com a medida feita através de uma cânula de pressão nasal. Os eventos de despertar foram registrados como Índice de Despertares (ID), que representa o número de despertares por hora.
Análise estatísticaTodos os resultados do questionário foram analisados por um teste t para amostras pareadas para determinar as alterações causadas pelo uso de corticosteroides intranasais durante quatro semanas. Analisamos também os parâmetros de pré‐medicação e pós‐medicação em grupos divididos de acordo com os escores da escala NOSE (≥ 10 e <10). Uma análise univariada foi feita com uma correlação de Pearson para comparar a relação entre todos os parâmetros. Os parâmetros gerais foram os seguintes: sexo, idade, altura, peso, índice de massa corporal, frequência de noctúria e circunferência do pescoço. Os parâmetros da PSG incluíram o IAH e o ID. Os parâmetros dos questionários incluíram os métodos de avaliação acima mencionados: ESE, NOSE e PSQI. Os parâmetros de desfecho dos pacientes avaliaram os seguintes sintomas: noctúria, qualidade do sono, disfunção diurna e obstrução nasal. Uma análise multivariada para os mesmos parâmetros foi feita em seguida através de regressão linear. Todas as análises estatísticas foram feitas em um computador pessoal com o pacote estatístico SPSS for Windows (versão 17.0, SPSS).
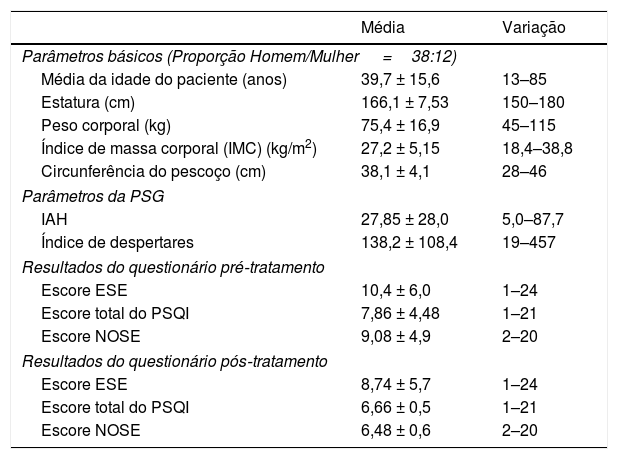
ResultadosCinquenta pacientes preencheram os questionários antes e após os tratamentos intranasais de fluticasona. A média de idade foi de 39,7 ± 15,6 anos, com uma proporção de homens para mulheres de 3:2. As características dos pacientes são mostradas na tabela 1. Todos os pacientes completaram a PSG, que revelou um IAH médio de 27,9 e ID de 138,2, respectivamente. Os escores pós‐tratamento do ESE, PSQI e NOSE indicaram uma diminuição em relação aos escores pré‐tratamento, de 10,4 para 8,74 (p < 0,001), 7,86 para 6,66 (p < 0,001) e 9,08 para 6,48 (p < 0,001), respectivamente.
Dados demográficos e clínicos dos pacientes com distúrbios do sono relacionados à respiração tratados com corticosteroide intranasal em spray
| Média | Variação | |
|---|---|---|
| Parâmetros básicos (Proporção Homem/Mulher =38:12) | ||
| Média da idade do paciente (anos) | 39,7 ± 15,6 | 13–85 |
| Estatura (cm) | 166,1 ± 7,53 | 150–180 |
| Peso corporal (kg) | 75,4 ± 16,9 | 45–115 |
| Índice de massa corporal (IMC) (kg/m2) | 27,2 ± 5,15 | 18,4–38,8 |
| Circunferência do pescoço (cm) | 38,1 ± 4,1 | 28–46 |
| Parâmetros da PSG | ||
| IAH | 27,85 ± 28,0 | 5,0–87,7 |
| Índice de despertares | 138,2 ± 108,4 | 19–457 |
| Resultados do questionário pré‐tratamento | ||
| Escore ESE | 10,4 ± 6,0 | 1–24 |
| Escore total do PSQI | 7,86 ± 4,48 | 1–21 |
| Escore NOSE | 9,08 ± 4,9 | 2–20 |
| Resultados do questionário pós‐tratamento | ||
| Escore ESE | 8,74 ± 5,7 | 1–24 |
| Escore total do PSQI | 6,66 ± 0,5 | 1–21 |
| Escore NOSE | 6,48 ± 0,6 | 2–20 |
ESE, Escala de Sonolência de Epworth; IAH, Índice de apneia‐hipopneia; NOSE, Nasal Obstruction Symptom Evaluation; PSG, polissonografia; PSQI, Pittsburgh Sleep Quality Index.
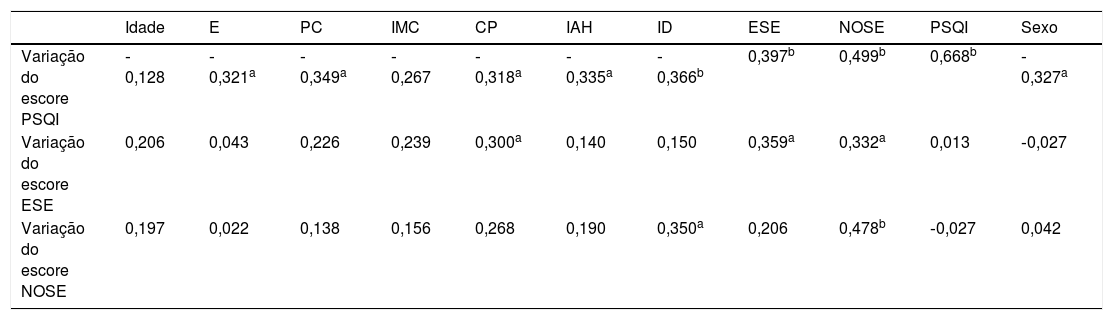
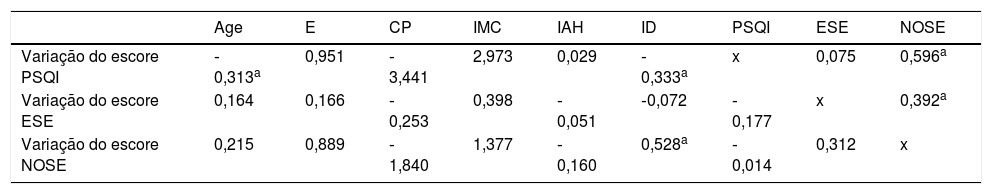
A correlação de Pearson foi feita em seguida para determinar os preditores para a melhoria na qualidade do sono (escore PSQI), disfunção diurna (escore ESE) e escore de obstrução nasal (escore NOSE); os resultados são mostrados na tabela 2. Após a análise univariada, foi feita uma análise multivariada através de regressão linear; os resultados são mostrados na tabela 3.
Análise univariada dos fatores que afetam a melhoria na qualidade do sono, disfunção diurna e obstrução nasal, com o coeficiente de correlação de Pearson
| Idade | E | PC | IMC | CP | IAH | ID | ESE | NOSE | PSQI | Sexo | |
|---|---|---|---|---|---|---|---|---|---|---|---|
| Variação do escore PSQI | ‐0,128 | ‐0,321a | ‐0,349a | ‐0,267 | ‐0,318a | ‐0,335a | ‐0,366b | 0,397b | 0,499b | 0,668b | ‐0,327a |
| Variação do escore ESE | 0,206 | 0,043 | 0,226 | 0,239 | 0,300a | 0,140 | 0,150 | 0,359a | 0,332a | 0,013 | ‐0,027 |
| Variação do escore NOSE | 0,197 | 0,022 | 0,138 | 0,156 | 0,268 | 0,190 | 0,350a | 0,206 | 0,478b | ‐0,027 | 0,042 |
CP, Circunferência do pescoço; E, estatura; ESE, Escala de Sonolência de Epworth; IAH, Índice de Apneia e Hipopneia; ID, Índice de Despertares; IMC, índice de massa corporal; NOSE; Nasal Obstruction Symptom Evaluation; PC, peso corporal; PSQI, Pittsburgh Sleep Quality Index.
Análise multivariada para fatores que afetam a melhoria na qualidade do sono, disfunção diurna e obstrução nasal por meio de coeficientes padronizados
| Age | E | CP | IMC | IAH | ID | PSQI | ESE | NOSE | |
|---|---|---|---|---|---|---|---|---|---|
| Variação do escore PSQI | ‐0,313a | 0,951 | ‐3,441 | 2,973 | 0,029 | ‐0,333a | x | 0,075 | 0,596a |
| Variação do escore ESE | 0,164 | 0,166 | ‐0,253 | 0,398 | ‐0,051 | ‐0,072 | ‐0,177 | x | 0,392a |
| Variação do escore NOSE | 0,215 | 0,889 | ‐1,840 | 1,377 | ‐0,160 | 0,528a | ‐0,014 | 0,312 | x |
CP, Circunferência do pescoço; E, estatura; ESE, Escala de Sonolência de Epworth; IAH, Índice de Apneia e Hipopneia; ID, Índice de Despertares; IMC, índice de massa corporal; NOSE; Nasal Obstruction Symptom Evaluation; PSQI, Pittsburgh Sleep Quality Index.
Os fatores que se correlacionaram com a melhoria na qualidade do sono na análise univariada foram sexo, estatura (E), peso corporal (PC), circunferência do pescoço (CP), IAH, ID, escore inicial do ESE e escore inicial da escala NOSE (tabela 2). No entanto, apenas a idade, o ID e o escore inicial da escala NOSE exibiram significância na análise multivariada (tabela 3). Escores iniciais mais altos da escala NOSE se correlacionaram com maior melhoria na qualidade do sono, enquanto idade mais avançada e ID inicial mais alto na PSG afetaram negativamente a melhoria na qualidade do sono. A circunferência do pescoço, escore inicial do ESE e escore inicial da escala NOSE se correlacionaram significativamente com a melhoria da disfunção diurna na análise univariada (tabela 2), mas o único preditor significativo na análise multivariada para melhoria da disfunção diurna foi o escore inicial da escala NOSE (tabela 3). Em ambas as análises univariada e multivariada, a melhoria nos sintomas de obstrução nasal mostrou uma correlação significativa somente com o ID inicial (tabelas 2 e 3).
Um teste t para amostras pareadas foi então feito para comparar as diferenças nos escores ESE, PSQI e NOSE antes e após o tratamento com fluticasona intranasal durante 4 semanas. A comparação foi feita em um grupo “geral” e em grupos divididos com base nos escores iniciais da escala NOSE (≥ 10 e < 10) (fig. 1). Os grupos divididos eram constituídos por 26 e 24 pacientes, respectivamente. No grupo “geral”, os escores de ESE, PSQI e NOSE diminuíram significativamente após 4 semanas de tratamento com fluticasona intranasal, de 10,42 para 8,74, 7,86 para 6,66 e 9,08 para 6,48, respectivamente. Uma diminuição significativa foi observada no grupo NOSE ≥ 10 em todas as três categorias, mas não no grupo NOSE < 10.
DiscussãoEmbora as evidências ainda sejam insuficientes para que medicamentos como os esteroides intranasais sejam prescritos de maneira geral para pacientes com AOS, estudos examinaram o efeito de esteroides intranasais em grupos específicos de pacientes com AOS. Ao revisar estudos anteriores, Kiely et al. conduziram um ensaio randomizado, controlado por placebo, para avaliar o efeito dos esteroides intranasais em pacientes com AOS e rinite coexistente, no qual a fluticasona intranasal melhorou o IAH e a resistência nasal das vias aéreas.17 Brouillette et al. verificaram que um tratamento de 6 semanas com fluticasona nasal podia diminuir a frequência de apneias e hipopneias mistas e obstrutivas em pacientes pediátricos com AOS.18 Uma metanálise de estudos controlados randomizados mostrou uma melhoria objetiva com o uso de corticosteroide intranasal em pacientes com AOS.9
Em nosso estudo, levantamos a hipótese de que, como o estreitamento das vias aéreas relacionado à obstrução nasal pode levar à AOS em alguns pacientes, os esteroides intranasais poderiam aliviar os sintomas em pacientes com distúrbios graves de obstrução nasal. Usamos a escala NOSE para esclarecer a gravidade dos sintomas de obstrução nasal e dividimos os pacientes em dois grupos com base nos escores NOSE > 10 e ≤ 10. Um escore NOSE maior foi o único fator independente significativamente relevante para qualidade do sono e melhoria da disfunção diurna. Após dividirmos os pacientes de acordo com os escores NOSE, melhorias significativas nos três escores sintomáticos (ESE, PSQI e NOSE) apareceram apenas no grupo com escores NOSE ≥ 10. Portanto, o tratamento com esteroides intranasais pode beneficiar pacientes com obstruções nasais graves em relação a sintomas subjetivos, como qualidade do sono e disfunção diurna; no entanto, o efeito foi mínimo em pacientes sem problemas óbvios de obstrução nasal. Em outro estudo sobre cirurgia nasal em pacientes com AOS com obstrução nasal crônica, Li et al. relataram que a cirurgia nasal resultou em uma redução efetiva da sonolência diurna e do ronco; entretanto, a eficácia no tratamento da AOS foi limitada.19 Resultados semelhantes em estudos futuros podem auxiliar a determinar que o tratamento da obstrução nasal pode beneficiar pacientes selecionados.
Como mencionado anteriormente, a obstrução nasal pode levar ao aumento da resistência nasal das vias aéreas, o que contribui para a obstrução das vias aéreas superiores durante o sono e é um fator de risco para AOS.3,4 Este estudo usou escores NOSE como uma ferramenta de triagem para determinar qual condição de pacientes com AOS provavelmente resultou de uma obstrução nasal, estabeleceu que o tratamento com esteroides intranasais pode ser um tratamento conservador adequado.
Além das aplicações para a seleção de tratamento, tem sido sugerido que a escala NOSE poderia servir como uma ferramenta de triagem simples, em vez do ESE, para pacientes com risco de AOS não diagnosticada e necessidades perioperatórias especiais.20
Os tratamentos atuais para obstrução nasal, como esteroides intranasais ou cirurgia nasal, ainda precisam ser estabelecidos como métodos viáveis de tratamento da AOS.7 Entretanto, para casos clínicos em que os pacientes não podem modificar seus estilos de vida ou tolerar a terapia com dispositivos CPAP e de avanço mandibular, os profissionais médicos podem considerar o uso de esteroides intranasais, particularmente porque as opções são limitadas. Contudo, mais evidências são necessárias para apoiar a viabilidade dessa opção. Além disso, os escores NOSE poderiam, potencialmente, ser usados como uma escala de triagem para a detecção precoce de pacientes de risco.
As limitações deste estudo foram o pequeno tamanho da amostra e a falta de seguimento por PSG após o período de tratamento de 4 semanas. Se pesquisas mais objetivas, como a rinomanometria, puderem ser feitas, os efeitos e mecanismos do tratamento com esteroides intranasais podem se tornar mais claros.
ConclusãoO tratamento com fluticasona intranasal pode ser útil para pacientes com AOS relacionada à obstrução nasal para melhorar a qualidade do sono e diminuir a disfunção diurna. O ponto de corte de 10 no escore da escala NOSE poderia determinar quais pacientes provavelmente se beneficiariam da aplicação do tratamento intranasal, que é uma ferramenta disponível e de baixo custo.
Conflitos de interesseOs autores declaram não haver conflitos de interesse.
Os dois primeiros autores contribuíram de forma igual para este estudo.
Como citar este artigo: Tam Y‐Y, Shao I‐H, Wu C‐C, Hsieh M‐L. The impact of intranasal fluticasone on patients with obstructive sleep apnea: a prospective study. Braz J Otorhinolaryngol. 2021;87:152–6.
A revisão por pares é da responsabilidade da Associação Brasileira de Otorrinolaringologia e Cirurgia Cérvico‐Facial.