Nasopharyngeal carcinoma, an epithelial‐derived malignant tumor which because of its anatomical location and atypical early symptoms, when diagnosed invasion and metastasis often have occurred. This requires a better understanding of the development mechanism, identifying diagnostic markers, and developing new treatment strategies.
ObjectiveTo study the relationship of LMP1 and Cripto‐1 in nasopharyngeal carcinoma.
MethodsThe expression of LMP1 and Cripto‐1 in specimens obtained from nasopharyngeal carcinoma patients (n = 42) and nasopharyngitis patients (n = 22) were examined. The expression of LMP1 and Cripto‐1 in LMP1‐negative and LMP1‐positive (CNE1‐LMP1) cells were also examined.
ResultsThe expression of LMP1 and Cripto‐1 was significantly higher in nasopharyngeal carcinoma than in nasopharyngitis (p < 0.05). Their expression in nasopharyngeal carcinoma with metastasis were significantly higher than that without metastasis (p < 0.05), which was correlated with TNM staging (p < 0.05). High Cripto‐1 expression and high proliferation rate were seen in CNE1‐LMP1 cells.
ConclusionsThe expression of LMP1 and Cripto‐1 in nasopharyngeal carcinoma is positively related. Their co‐expression might contribute to the proliferation and metastasis of nasopharyngeal carcinoma.
O carcinoma nasofaríngeo é um tumor maligno derivado do epitélio de localização anatômica recôndita e sintomas iniciais atípicos; quando diagnosticado, frequentemente invasão e metástases já ocorreram. Isso requer uma melhor compreensão do seu mecanismo de desenvolvimento, identificação dos marcadores diagnósticos e desenvolvimento de novas estratégias de tratamento.
ObjetivoEstudar a relação de LMP1 e Cripto‐1 no carcinoma nasofaríngeo.
MétodoA expressão de LMP1 e Cripto‐1 em espécimes obtidos de pacientes com carcinoma de nasofaringe (n = 42) e pacientes com nasofaringite (n = 22) foi analisada. A expressão de LMP1 e Cripto‐1 em células LMP1‐negativas e LMP1‐positivas (CNE1‐LMP1) também foi analisada.
ResultadosA expressão de LMP1 e Cripto‐1 foi significantemente maior na presença de carcinoma nasofaríngeo do que na nasofaringite (p < 0,05). Sua expressão em carcinomas com metástase foi significantemente maior do que em casos sem metástase (p < 0,05), o que se correlacionou com o estadiamento TNM (p < 0,05). Uma alta expressão de Cripto‐1 e alta taxa de proliferação foram observadas nas células CNE1‐LMP1.
ConclusõesA expressão de LMP1 e Cripto‐1 é positivamente relacionada com carcinoma nasofaríngeo. Sua coexpressão pode ser atribuída à proliferação e metástase do tumor.
O carcinoma nasofaríngeo (CNF), um tumor maligno derivado do epitélio com características regionais, étnicas e de agregação familiar especiais, é um dos cânceres mais comuns no sudeste da Ásia e no sul da China. Sua taxa de incidência no sul da China é de aproximadamente 200 milhões.1,2 Se diagnosticado e tratado precocemente, uma taxa de sobrevivência de 90% pode ser alcançada. Infelizmente, a maioria dos casos é diagnosticada nos estágios finais e a taxa de sobrevivência é inferior a 50%, principalmente devido a sua localização anatômica recôndita e a seis sintomas iniciais atípicos. Quando é diagnosticado, com frequência invasão e metástases já estão presentes. Embora a radioterapia de precisão e a quimioterapia‐alvo tenham melhorado significantemente a taxa de sobrevida, mais de 30% dos pacientes ainda sofrem recidiva local ou metástase a distância e a taxa de recorrência pode chegar a 82%. Quando há recidiva, a taxa de sobrevivência pode ser significantemente diminuída e o tempo médio de sobrevivência é de apenas 7,2 a 22 meses. A maioria dos pacientes morre devido à presença de metástases a distância, que é a principal razão para o fracasso do tratamento.3–6 Assim, a detecção, o diagnóstico e o tratamento precoces têm grande importância para a melhoria na taxa de sobrevivência. Isso requer uma melhor compreensão do seu mecanismo de desenvolvimento, identificação de marcadores diagnósticos e desenvolvimento de novas estratégias de tratamento.
A proteína de membrana latente 1 (LMP1) é uma proteína de membrana integrada que compartilha a via de transdução de sinal com membros da superfamília do receptor de TNF (fator de necrose tumoral). Como oncogene clássico, a LMP1 é tumorigênica. Nas células epiteliais, a LMP1 promove o crescimento celular, estimula a migração e a invasão e regula a diferenciação do epitélio escamoso. O último efeito também pode aumentar a capacidade de invasão de células tumorais.7 A LMP1 é a oncoproteína mais importante expressa pelo Vírus Epstein‐Barr (EBV) em células de CNF e é essencial para o crescimento e a transformação de células infectadas mediadas por EBV, que desempenham um papel importante na ocorrência, no desenvolvimento, na invasão e metástase de CNF.8
A LMP1 contém três domínios: um terminal N citoplasmático curto, seis regiões transmembrana e uma grande cauda C‐terminal citoplasmática. Ela interage através dos domínios citoplasmáticos (regiões de ativação C‐terminal ‐ CTAR 1 e 2) com moléculas adaptadoras da família de receptores do fator de necrose tumoral. Sua estrutura especial torna sua função semelhante à do membro CD40da família do receptor do TNF (TNFR) e pode desencadear uma série de vias de sinalização celular de maneira ligante‐independente, inclusive NF‐κB, JAK/STAT, p38/MAPK, PI3K/Akt e ERK‐MAPK/JNK/SAPK. Portanto, está envolvida na invasão de células cancerígenas, metástase e transformação maligna.9–13
A Cripto‐1, também conhecida como fator de crescimento‐1 derivado de teratocarcinógeno, é um membro da família Cripto‐1‐FRL‐1‐Cryptic (CFC) do Fator de Crescimento Epidérmico (EGF). É um modulador multifuncional envolvido na embriogênese e formação tumoral e essencial na regulação da embriogênese inicial, promove migração celular, angiogênese e manutenção de células‐tronco. O mRNA de Cripto‐1 e/ou sua expressão proteica foi encontrado em neoplasias de mama, colo do útero, testículos, pulmões, cólon, estômago, pâncreas e ovários.14,15 Numerosos estudos mostram que a transformação maligna, invasão, metástase e prognóstico ruim do tumor estão associados à alta expressão de Cripto‐1.16,17 Especialistas sugerem que a upregulação de Cripto‐1 pode desempenhar um papel na progressão maligna e na metástase do CNF humano.18,19 A proteína Cripto‐1 tem sido considerada como um biomarcador potencial para o progresso da invasão tumoral e metástase. Embora a infecção pelo EBV esteja intimamente associada ao CNF, seu mecanismo molecular principal, entretanto, como os mecanismos tumorigênicos relacionados à LMP1 no CNF, ainda não foram completamente elucidados. No entanto, sabe‐se que a LMP1 está envolvida em três proteínas quinases clássicas ativadas por mitógeno (MAPK): ERK‐MAPK, p38 MAPK e JNK/SAPK através da via NF‐kappa B típica e atípica e via PI3K.20–22 A Cripto‐1 desempenha um papel importante no desenvolvimento embrionário e na progressão tumoral como correceptor do fator nodal morfológico relacionado ao TGF‐ß.23 A Cripto‐1 pode interagir com ras, p38 MAPK e Wnt/B‐catenina através da via de sinalização do TGF‐β e regular diretamente a via clássica de transição epitelial‐mesenquimal (EMT) para promover fatores de transcrição, tais como Snail, Twist e Slug. A Cripto‐1 também interage com o TGF‐β1 e a ativina A e B para interferir e enfraquecer sua sinalização em várias linhagens celulares, atua como ligante Glicosil Fosfatidil Inositol (GPI), que ativa a via de sinalização MAPK e PI3K/proteína quinase B (Akt) para regular a proliferação, migração e sobrevivência celular.24–27 Portanto, é razoável sugerir que existe uma correlação entre LMP1 e Cripto‐1 em CNF humano.
Neste estudo, imuno‐histoquímica, ensaios de Western blot e reação de polimerase em cadeia em tempo real (RT‐PCR) foram usados para investigar a coexpressão da proteína LMP1 e da proteína Cripto‐1 na ocorrência e no desenvolvimento do CNF humano. Relatamos pela primeira vez a existência da correlação de LMP1 e Cripto‐1 no CNF humano. Nossos achados também podem fornecer novas informações sobre o mecanismo molecular envolvido na carcinogênese e progressão do CNF.
MétodoColeta e classificação de amostrasDe fevereiro de 2011 a fevereiro de 2016, foram coletadas amostras de mucosa nasofaríngea de 42 pacientes com carcinoma nasofaríngeo. Aqueles com metástase em linfonodos cervicais confirmados por ressonância magnética foram identificados. Todos os espécimes foram diagnosticados histopatologicamente de acordo com a classificação da OMS para carcinoma nasofaríngeo. Nenhum deles tinha sido submetido a radioterapia, quimioterapia ou outros tratamentos prévios. O estadiamento clínico TNM foi classificado de acordo com o estágio clínico de câncer de cabeça e pescoço de 2002da Union for International Cancer Control (UICC) para o estadiamento do carcinoma nasofaríngeo (versão 6). Quanto aos controles, no mesmo período foram coletadas amostras de tecidos de 22 pacientes com nasofaringite. Todas as amostras foram obtidas com o consentimento informado dos pacientes e o estudo foi aprovado pelo Comitê de Ética (n° K2016‐01‐01).
Análise imuno‐histoquímica das amostras de tecidoAs amostras frescas foram fixadas em formalina neutra a 10% e submetidas às etapas de processamento de tecidos de rotina. Uma série de secções reidratadas de 2,5μm de espessura foi submetida à etapa de recuperação de antígeno em tampão de citrato em ebulição por 1,5min, depois em H2O2 a 3% durante 10min para bloquear a catalase endógena, seguido por enxague com PBS. O método de coloração imuno‐histoquímica Elivision 2 Step foi aplicado, incubaram‐se primeiro as secções com o anticorpo primário correspondente, isto é, anticorpo monoclonal de camundongo anti‐LMP1 (1:500) (M0897, DAKO, Dinamarca) ou anticorpo policlonal de coelho anti‐Cripto‐1 (1:60) (ab19917, Abcam, EUA), a 37°C por 1h, seguido por anticorpo policlonal de cabra anticoelho ou anticamundongo IgG H&L (1:5000) (ab6721 e ab6789, Abcam, EUA) em temperatura ambiente por 30min. A reação da cor foi desenvolvida pelo tampão DAB. O PBS foi usado como controle negativo.
Sob exame com microscópio óptico, as células positivas para LMP1 e Cripto‐1 foram identificadas como a presença de coloração amarelada a amarronzada na membrana e no citoplasma. Com base na intensidade da cor, os níveis de expressão foram classificados em: 0 (negativo), 1 (positivo fraco), 2 (positivo moderado) e 3 (positivo forte), usou‐se a abordagem de escore duplo‐cego ao aleatoriamente selecionar 5 campos e 200 células em cada campo. Com base no número de células positivas contadas, os níveis positivos foram classificados como: 1 (0% ‐10% de células positivas), 2 (11% ‐50% de células positivas), 3 (51% ‐80% de células positivas) e 4 (81% – 100% de células positivas). Os níveis globais de expressão das proteínas LMP1 e Cripto‐1 foram calculados pela multiplicação do nível de expressão e do nível positivo: 0‐1 (‐), 2‐3 (+), 4‐6 (++) e 8‐16 (+++).28
Linhagens e cultura de célulasDuas linhagens celulares foram usadas neste estudo: CNE1 – células de CNF humano com alta diferenciação e células CNE1‐LMP1‐CNE1, com transfecção estável do gene LMP1. Ambas foram obtidas na Faculdade de Medicina. As células foram cultivadas rotineiramente em meio DMEM que continha 10% de soro bovino fetal (FBS, Gibco Life Technologies) a 37°C e 5% de CO2.
Experimento de proliferação de células CCK‐8Para comparar a taxa de crescimento de duas linhagens celulares, as células da fase de crescimento logarítmica foram semeadas em placas de 96 poços na densidade inicial de 2×103 células/poço e submetidas a ensaio de viabilidade com o kit CCK‐8 (Dojindo Laboratory) em 1, 2, 3, 4 e 5 dias, respectivamente. A densidade celular foi medida a 450nm em um analisador de imunoensaio ligado a enzimas (TECAN, Sunrise).
Verificação da expressão de LMP1Para verificar a expressão do gene LMP1 nas células CNE1‐LMP1 e CNE1, o RNA total foi extraído das células pelo reagente TRIzol (Invitrogen, Carlsbad, CA) e depois feita a transcrição reversa em cDNA. Todos os primers foram sintetizados pela Shanghai SanGon Biotechnology Co. e incluíram o primer forward do gene LMP1: 5’‐ CAACAACGGCAAGACTCCC‐3’,primer reverse 5’‐ CCTCAAAGAAGCCACCCTC ‐3’ e o tamanho do primer foi 146 pb. O primer forward do gene de referência GAPDH: 5’‐GAAGGTGAAGGTCGGAGTC‐3’, primerreverse 5’‐GCTCCTGGAAGATGGTGATG‐3’ e o tamanho do primer foi 233 pb. O volume do sistema de reação da PCR foi 20 μL (coloração de ácido nucleico SYBR Green I 10μL, os primers forward e reverse 0,4μL cada, volume de template de cDNA 2,0μL e dietil pirocarbonato 7,2μL). A PCR de 40 ciclos foi feita sob as seguintes condições: 95°C por 30 seg, 95°C por 5 seg, 60°C por 20 seg. O produto amplificado foi detectado por eletroforese em gel de agarose para verificar o tamanho da tira e garantir a especificidade dos produtos de PCR. O método ΔΔCq foi usado para quantificação relativa, ΔΔCt = grupo experimental (gene alvo Ct ‐ Ct GAPDH) – grupo controle (gene alvo Ct ‐ Ct GAPDH).
Análise da expressão de Cripto‐1Para analisar a expressão do gene de Cripto‐1 nas células CNE1‐LMP1 e CNE1, foi feita a RT‐PCR como descrito acima, com o uso do primer forward do gene Cripto‐1: 5’‐CCCAAGAAGTGTTCCCTGTG‐3’, primer reverse 5’‐TGCAGACGGTGGTAGTTCTG‐3’, e o tamanho do primer foi 138 pb.
Ensaio de Western blot das proteínas LMP1 e Cripto‐1As proteínas foram extraídas de células de crescimento logarítmico do frasco de cultura e a concentração de proteína foi determinada pelo método BCA. Para o ensaio de Western blot, a quantidade inicial para a proteína LMP1 e para a proteína Cripto‐1 foi 80μg e 30μg, respectivamente. Subsequentemente, cada amostra de proteína foi separada com eletroforese em gel de SDS‐PAGE a 12% antes de ser transferida para a membrana de PVDF. As membranas foram bloqueadas à temperatura ambiente por 1h com TBST que continha 5% de leite desnatado antes de ser incubadas com anticorpos primários monoclonal de camundongo (CS 1‐4, Abcam) para EBV LMP 1 (1:1000) (ab‐78113, Abcam), policlonal de coelho para Cripto‐1 (1:1000) (ab19917, Abcam), policlonal de coelho para beta Tubulina (1: 500) (ab6046, Abcam) a 4° C durante a noite, respectivamente. Após lavagem com solução TBST, as membranas de PVDF foram incubadas com o segundo anticorpo correspondente (IgG ‐ H&L policlonal de cabra anticoelho/camundongo (1:5000) (ab6721 e ab6789, Abcam) à temperatura ambiente durante uma hora. ECL líquido foi revelado e exposto e o Image J software foi usado para analisar o valor de cinza de cada banda.
Análises estatísticasOs valores quantitativos foram expressos como médias ± DP. Os níveis de expressão de LMP1 e Cripto‐1 em vários parâmetros clínicos‐patológicos foram calculados com o teste do qui‐quadrado. A correlação da expressão de LMP1 e Cripto‐1 foi calculada com a análise de correlação de postos de Spearman. A comparação dos níveis de expressão de mRNA e proteína entre o controle CNE1 e CNE1‐LMP1 foi feita com o teste t de amostras pareadas em todos os casos. Todas as análises estatísticas foram feitas com o programa SPSS 21.0 com α = 0,05 (bicaudal) para o teste padrão; o valor de p < 0,05 foi considerado estatisticamente significativo.
ResultadosDados demográficos dos pacientesO grupo CNF incluiu 29 homens e 13 mulheres (razão M / F = 2,23). A faixa etária variou de 25 a 74 anos (média de 52,7 ± 15,7 anos). O grupo com nasofaringite incluiu 16 homens e 6 mulheres (razão M / F = 2,67). A idade variou de 20 a 59 anos (média de idade de 39,3 ± 11,4 anos). No grupo CNF, 30 pacientes (71,4%) apresentavam metástase linfonodal cervical. A classificação histológica mostrou 10 casos de carcinoma de células escamosas queratinizante (23,8%) e 32 casos de carcinoma não queratinizante (76,2%). Entre eles, 5 casos no Estágio I, 9 casos no Estágio II, 18 casos no Estágio III e 10 casos no Estágio IV. O exame histológico de amostras de tecido obtidas de pacientes com nasofaringite confirmou que não havia sinais de carcinoma além da inflamação.
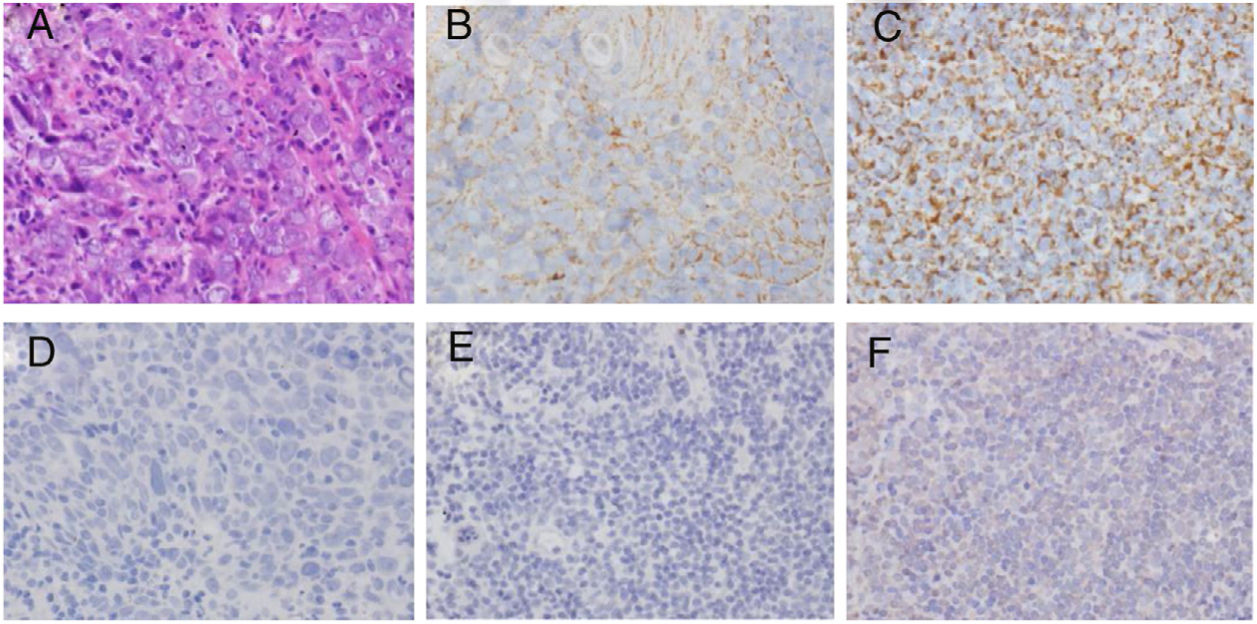
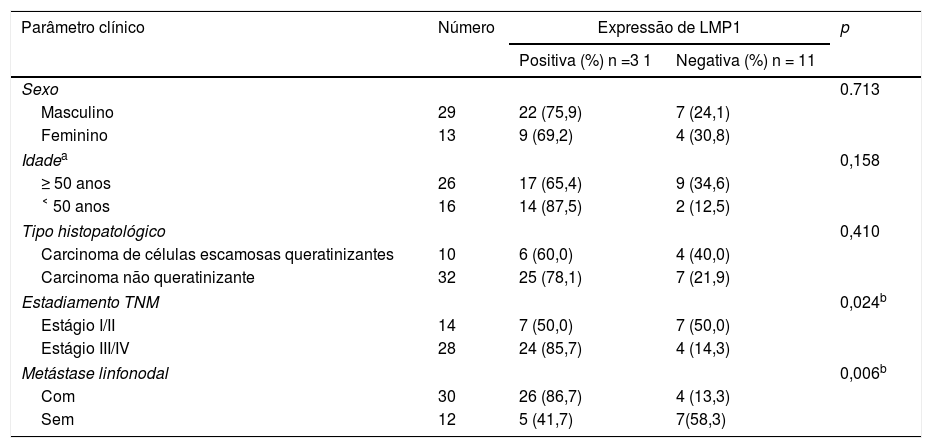
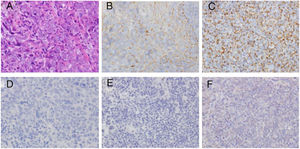
Expressão da proteína LMP1 no carcinoma nasofaríngeoO exame dos níveis de localização e expressão da proteína LMP1 em amostras de mucosa nasofaríngea mostrou que a taxa de expressão da proteína LMP1 em carcinoma nasofaríngeo foi de 73,8% e de 22,7% em tecido nasofaríngeo (p < 0,01), respectivamente (tabela 1). A distribuição da proteína LMP1 no carcinoma nasofaríngeo foi mais uniforme do que no tecido da nasofaringite (fig. 1). No entanto, diferentes níveis de expressão da proteína LMP1 foram observados em células cancerígenas.
Análise imuno‐histoquímica da expressão de LMP1. (A) Coloração H&E do tecido do CNF. (B) Expressão de LMP1 no tecido do CNF (+). (C) Expressão de LMP1 no tecido do CNF (+++). (D) Controle negativo da coloração de LMP1 no tecido do CNF. (E) Controle negativo da coloração de LMP1 em tecido de nasofaringite. (F) Expressão fraca de LMP1 em tecido da nasofaringite. Ampliação ×400.
Houve uma diferença estatisticamente significante (p < 0,01) entre a expressão da proteína LMP1 nos pacientes com (86,7%) e sem metástase linfonodal (41,7%). Uma análise mais aprofundada da relação entre a expressão da proteína LMP1 e os parâmetros patológicos do CNF mostrou que a expressão da proteína LMP1 mostrou boa correlação com o estadiamento TNM (tabela 2). A expressão nos estágios III e IV foi significantemente maior do que nos estágios I e II (p < 0,05). No entanto, não houve diferença estatisticamente significante em termos de sexo do paciente (p = 0,713), idade (p = 0,158) e tipo patológico do carcinoma nasofaríngeo (p = 0,410).
Relação entre a expressão de LMP1 e os parâmetros anátomo‐clínicos (teste do qui‐quadrado)
| Parâmetro clínico | Número | Expressão de LMP1 | p | |
|---|---|---|---|---|
| Positiva (%) n =3 1 | Negativa (%) n = 11 | |||
| Sexo | 0.713 | |||
| Masculino | 29 | 22 (75,9) | 7 (24,1) | |
| Feminino | 13 | 9 (69,2) | 4 (30,8) | |
| Idadea | 0,158 | |||
| ≥ 50 anos | 26 | 17 (65,4) | 9 (34,6) | |
| ˂ 50 anos | 16 | 14 (87,5) | 2 (12,5) | |
| Tipo histopatológico | 0,410 | |||
| Carcinoma de células escamosas queratinizantes | 10 | 6 (60,0) | 4 (40,0) | |
| Carcinoma não queratinizante | 32 | 25 (78,1) | 7 (21,9) | |
| Estadiamento TNM | 0,024b | |||
| Estágio I/II | 14 | 7 (50,0) | 7 (50,0) | |
| Estágio III/IV | 28 | 24 (85,7) | 4 (14,3) | |
| Metástase linfonodal | 0,006b | |||
| Com | 30 | 26 (86,7) | 4 (13,3) | |
| Sem | 12 | 5 (41,7) | 7(58,3) | |
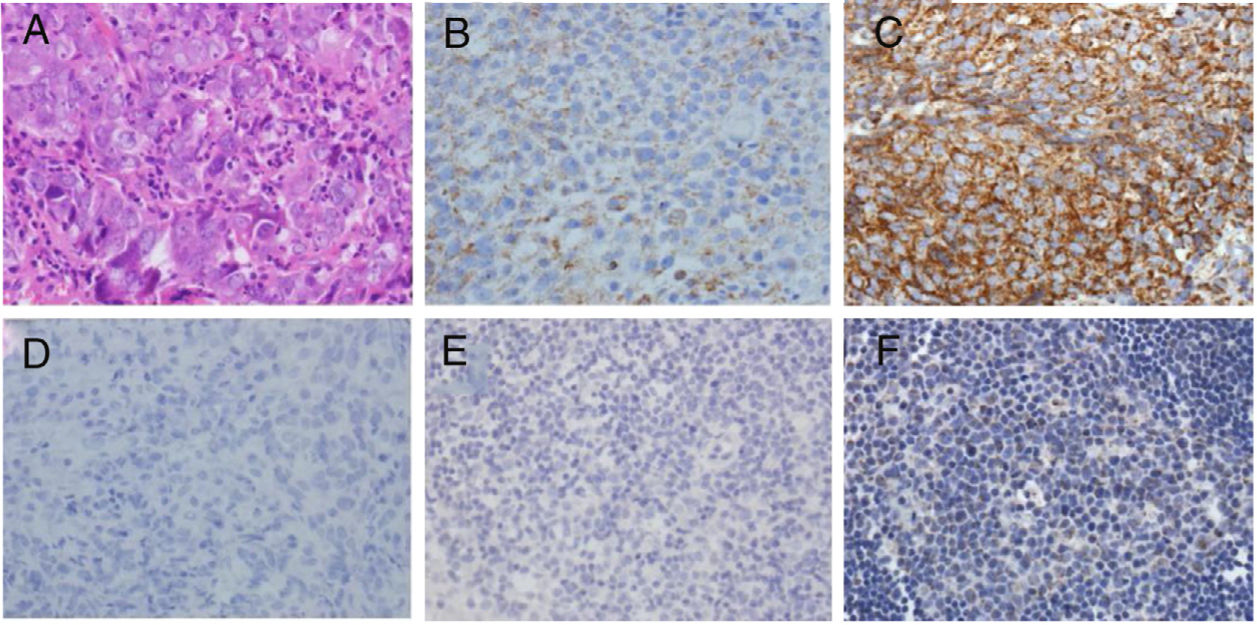
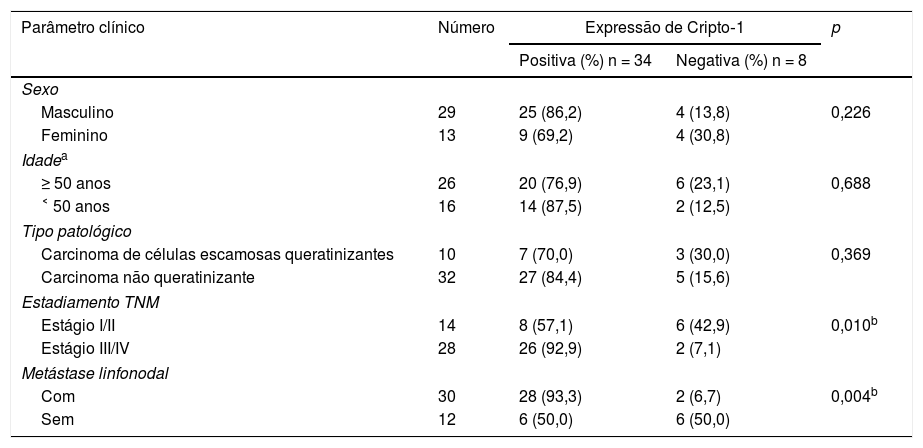
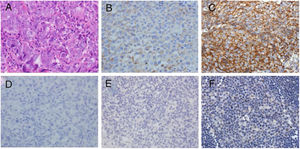
A análise dos níveis de localização e níveis de expressão da proteína Cripto‐1 em amostras de mucosa nasofaríngea mostrou que a taxa de expressão da proteína Cripto‐1 no carcinoma nasofaríngeo foi de 80,9% e de 36,4% na nasofaringite (p < 0,01), respectivamente (tabela 3). No entanto, diferentes níveis de expressão da proteína Cripto‐1 foram observados em células cancerígenas (fig. 2). Houve uma diferença estatisticamente significante (p < 0,01) entre a expressão da proteína Cripto‐1 em pacientes com (93,3%) e sem metástase linfonodal (50%). Uma análise mais aprofundada da relação entre a expressão da proteína Cripto‐1 e parâmetros patológicos do CNF mostrou que a expressão da proteína Cripto‐1 mostrou boa correlação com o estadiamento TNM. A expressão nos estágios III e IV foi significantemente maior do que nos estágios I e II (p < 0,05) (tabela 4). Entretanto, não houve diferença estatisticamente significante em termos de sexo do paciente (p = 0,226), idade (p = 0,688) e tipo patológico do carcinoma nasofaríngeo (p = 0,369).
Análise imuno‐histoquímica da expressão de Cripto‐1. (A) Coloração H&E do tecido do CNF. (B) Expressão de Cripto‐1 tecido do CNF (+). (C) Expressão de Cripto‐1 tecido do CNF (+++). (D) Controle negativo da coloração de Cripto‐1 tecido do CNF. (E) Controle negativo da coloração de Cripto‐1 em tecido de nasofaringite. (F) Expressão fraca de Cripto‐1 em tecido de nasofaringite. Ampliação ×400.
Relação entre a expressão de Cripto‐1 e os parâmetros anátomo‐clínicos (teste do qui‐quadrado)
| Parâmetro clínico | Número | Expressão de Cripto‐1 | p | |
|---|---|---|---|---|
| Positiva (%) n = 34 | Negativa (%) n = 8 | |||
| Sexo | ||||
| Masculino | 29 | 25 (86,2) | 4 (13,8) | 0,226 |
| Feminino | 13 | 9 (69,2) | 4 (30,8) | |
| Idadea | ||||
| ≥ 50 anos | 26 | 20 (76,9) | 6 (23,1) | 0,688 |
| ˂ 50 anos | 16 | 14 (87,5) | 2 (12,5) | |
| Tipo patológico | ||||
| Carcinoma de células escamosas queratinizantes | 10 | 7 (70,0) | 3 (30,0) | 0,369 |
| Carcinoma não queratinizante | 32 | 27 (84,4) | 5 (15,6) | |
| Estadiamento TNM | ||||
| Estágio I/II | 14 | 8 (57,1) | 6 (42,9) | 0,010b |
| Estágio III/IV | 28 | 26 (92,9) | 2 (7,1) | |
| Metástase linfonodal | ||||
| Com | 30 | 28 (93,3) | 2 (6,7) | 0,004b |
| Sem | 12 | 6 (50,0) | 6 (50,0) | |
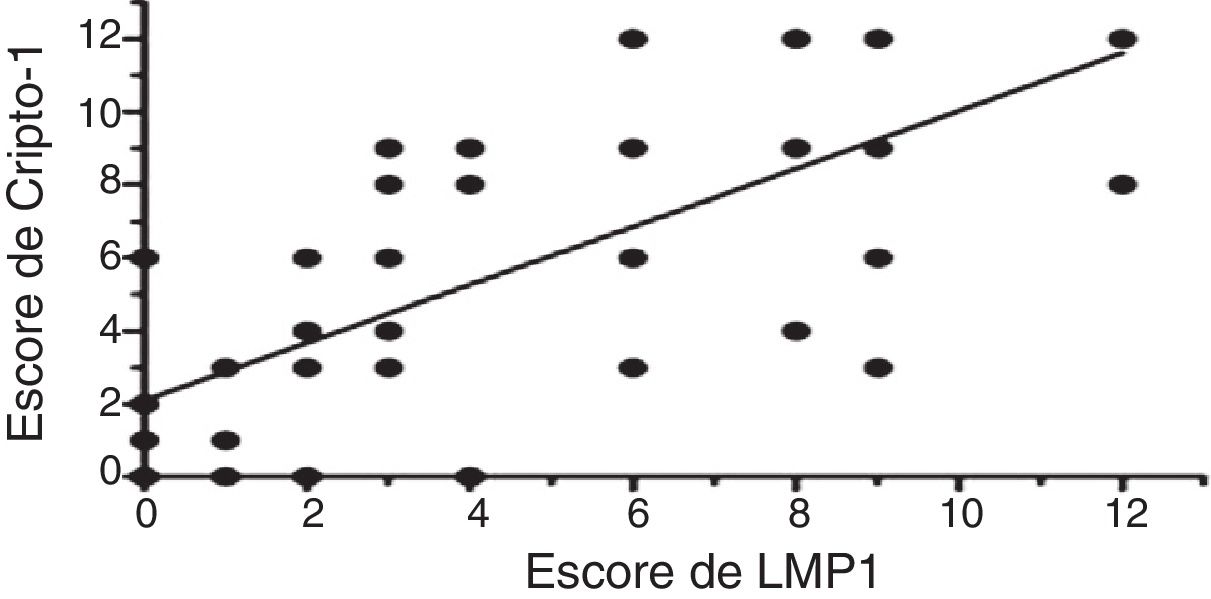
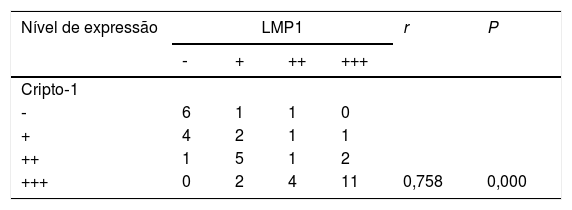
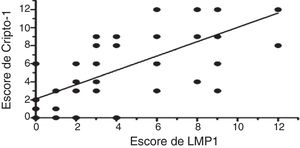
Os níveis de expressão da proteína LMP1 e da proteína Cripto‐1 obtidos através da coloração imuno‐histoquímica foram pontuados e os resultados são mostrados na tabela 5. O ensaio de correlação sugeriu que havia uma correlação positiva entre o nível de expressão da proteína LMP1 e proteína Cripto‐1 no tecido de CNF (r = 0,758, p = 0,01) (fig. 3).
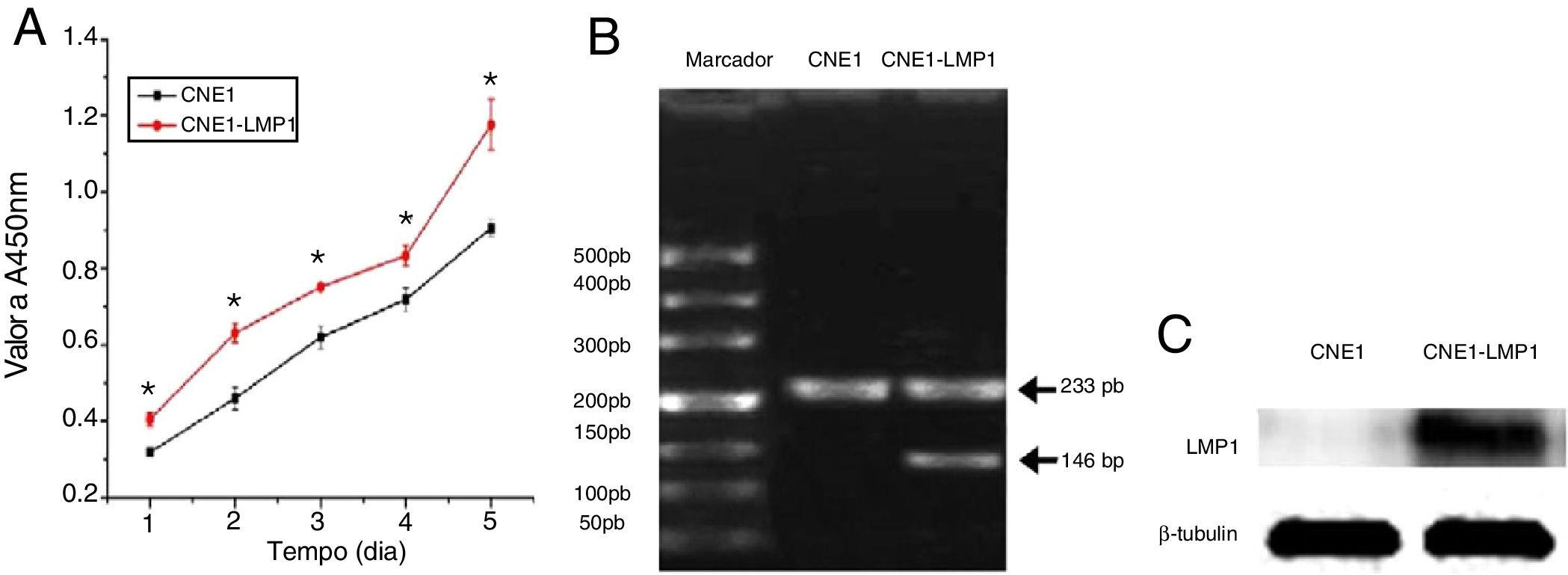
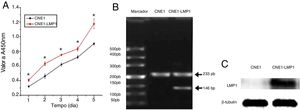
O ensaio de viabilidade de células de CNF mostrou que, sob as mesmas condições de cultura, as células CNE1‐LMP1 cresceram mais rapidamente do que as células CNE1 (fig. 4A). Isso pode sugerir que a LMP1 poderia facilitar o crescimento celular.
Forte expressão de mRNA e proteína de LMP1 em células CNE1‐LMP1O ensaio PCR real time (RT‐PCR) mostrou que não havia expressão de mRNA de LMP1 (146 pb) em células CNE1, enquanto havia uma forte expressão de mRNA de LMP1 em células CNE1‐LMP1 (fig. 4B). O ensaio Western blot também mostrou que a expressão da proteína LMP1 em células CNE1 era negativa, embora fosse positiva em células CNE1‐LMP1 (fig. 4C). Portanto, foi confirmado que a linhagem celular CNE1‐LMP1 foi estavelmente transferida com o gene LMP1 e foi capaz produzir a proteína LMP1.
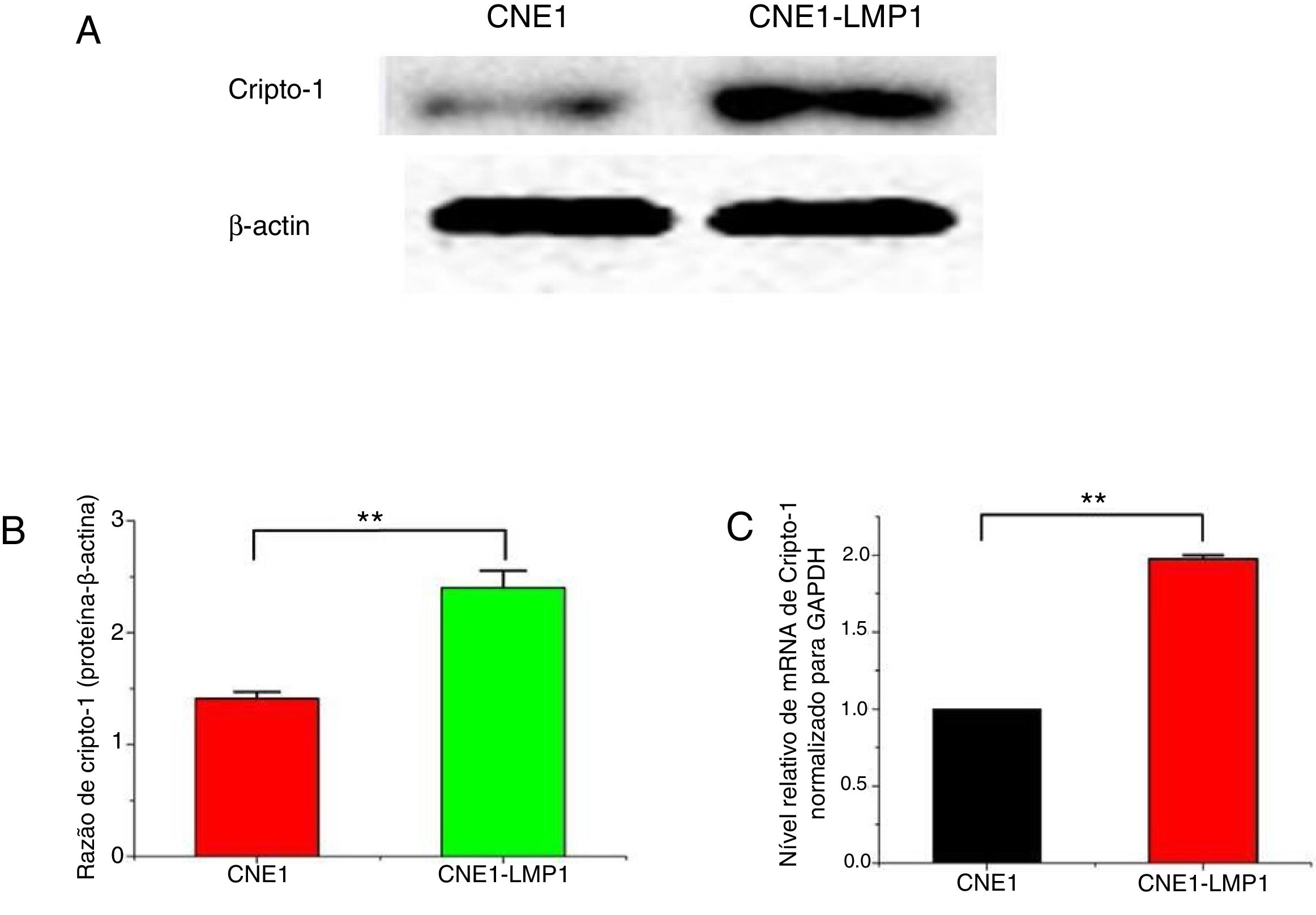
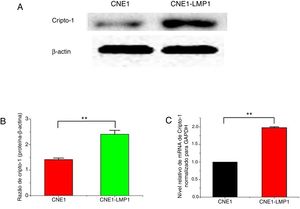
Forte expressão do mRNA e proteína de Cripto‐1 em células CNE1‐LMP1O ensaio de Western blot mostrou que a proteína Cripto‐1 foi expressa em ambas as células CNE1 e CNE1‐LMP1, mas houve diferença significante em relação ao nível de expressão (fig. 5A). O ensaio quantitativo mostrou que a expressão da proteína Cripto‐1 nas células CNE1‐LMP1 foi 1,7 vez maior do que nas células CNE1 (p < 0,05) (fig. 5B). Além disso, o ensaio RT‐PCR mostrou que o mRNA de Cripto‐1 foi expresso em células CNE1 e CNE1‐LMP1, mas houve diferença significante em relação ao nível de expressão. O nível de mRNA de Cripto‐1 nas células CNE1‐LMP1 foi 2 vezes mais elevado do que nas células CNE1 (p < 0,05) (fig. 5C).
DiscussãoEste estudo analisou, pela primeira vez, a coexpressão da proteína LMP1 e da proteína Cripto‐1 no CNF humano. A demonstração da coexpressão da proteína LMP1 e da proteína Cripto‐1 no tecido e nas células do CNF sugere que tal coexpressão esteja envolvida na ocorrência e na metástase do CNF humano.
A LMP1, que se acreditava ser a principal proteína oncogênica para EBV, correlacionou‐se positivamente com a metástase do CNF.29 A LMP1 pode recrutar uma série de citocinas e interagir com elas para ativar algumas vias de sinalização celular chave e causar inibição da apoptose, proliferação celular, metástase e levar a tumorigênese e desenvolvimento do tumor. Portanto, a LMP1 pode ser usada como um marcador diagnóstico de CNF.30,31 Nosso estudo também apoia essa conclusão. O estudo ex vivo mostrou que a proteína LMP1 foi expressa a uma taxa muito mais elevada no tecido humano do CNF do que no tecido de nasofaringite (73,8% contra 22,7%) (tabela 1). Além disso, a superexpressão de LMP1 foi associada com a classificação N, metástase distante e o estágio clínico (tabela 2).
A LMP1 pode facilitar a invasividade do CNF EBV‐positivo através da regulação da expressão de miR‐204.32 A invasão e a metástase são duas características que definem a patogênese e progressão de tumores malignos. A metástase é geralmente composta por etapas múltiplas, sequenciais, seletivas e interdependentes. A metástase inicial em linfonodos é mais comum no CNF, o que pode ser relacionado ao LMP1 do EBV. Isso é particularmente significativo em pacientes imunocompetentes.33,34 De fato, neste estudo, a comparação in vitro mostrou que as células CNE1‐LMP1 demonstraram maior capacidade de proliferação do que as células CNE1 com expressão negativa de LMP1 (fig. 4A). Isso pode ser usado como um indicador para a triagem da população de alto risco.
A Cripto‐1 desempenha um papel importante no processo de desenvolvimento embrionário e tumorigênese. Ela pode iniciar ou promover o desenvolvimento de vários tipos de câncer.35 Neste estudo, o método da imuno‐histoquímica foi usado para detectar a expressão da proteína Cripto‐1 em tecidos do CNF. Sua expressão foi muito mais elevada no tecido do CNF humano do que no tecido do nasofaringite (80,9% vs. 36,4%) (tabela 3). Isso está de acordo com os níveis de expressão da proteína Cripto‐1 no câncer de mama (i.e., 40% a 80%), câncer cervical invasivo (65%), câncer gástrico (54%) e neoplasia mucinosa papilar intraductal do pâncreas (59,5%).36,37
A correlação entre a expressão de Cripto‐1 e a atividade de proliferação ou invasão/potencial metastático de células cancerosas em amostras de tecido foi examinada em estudos in vitro e in vivo. As células epiteliais mamárias transduzidas de Cripto‐1 apresentam aumento nas taxas de proliferação. Em contraste, o nocaute do gene Cripto‐1 nas células epiteliais mamárias reduziu o crescimento dessas células, tanto in vitro como in vivo. Além disso, a superexpressão de Cripto‐1 promoveu a proliferação celular, o crescimento independente de ancoragem e a transformação de células epiteliais mamárias in vitro e a indução da hiperplasia da glândula mamária e formação de tumor no modelo de Cripto‐1 de tumor mamário em camundongos.38
Após a eliminação da expressão de Cripto‐1 em CNE‐2 e C666‐1 através do silenciamento de RNAi mediado por Lentivírus, foi verificado que o crescimento celular foi suprimido após a inibição da proteína endógena Cripto‐1 com o uso do silenciamento do gene de Cripto‐1. O modelo de xenotransplante em camundongos nus com instrumento de visualização de corpo inteiro constatou que o volume e o peso médios do tumor no grupo de camundongos transplantados foram significantemente menores in vivo.18
Neste estudo, o método de imuno‐histoquímica foi empregado para detectar a coexpressão das proteínas LMP1 e Cripto‐1 em tecidos de CNF. Os resultados mostraram que ambas as proteínas LMP1 e Cripto‐1 apresentaram expressão positiva em CNF, enquanto que os tecidos epiteliais da inflamação apresentaram expressão baixa e fracamente positiva (tabelas 1‐4) (figs. 1 e 2). No presente estudo, pela primeira vez, foi demonstrado in vitro e in vivo que a expressão de LMP1 e Cripto‐1 está positivamente correlacionada no CNF (p < 0,01) (tabela 5) (fig. 3). Invasão, metástase e recidiva são as características biológicas básicas que podem afetar a sobrevida de pacientes com CNF. Até hoje, a metástase tumoral geralmente observada em casos de CNF ainda é o maior obstáculo para a cura dos pacientes. Nossos resultados mostraram que a expressão das proteínas LMP1 e Cripto‐1 em pacientes com CNF com metástase em linfonodos cervicais foi significantemente maior do que em pacientes sem metástase linfonodal (p < 0,05). Isso indica que a alta expressão de LMP1 e Cripto‐1 pode desempenhar um papel fundamental na invasão e metástase do CNF, que estão relacionadas ao progresso adverso do tumor.
Em comparação com outros cânceres de cabeça e pescoço, a falta de características clínicas precoces típicas, alta taxa de recorrência local e metástase linfonodal cervical são fatores importantes para o mau prognóstico do CNF.39 Em muitos indicadores prognósticos clássicos de CNF, a metástase linfonodal cervical é a mais importante. Portanto, a superexpressão de LMP1 e Cripto‐1 provavelmente está envolvida no desenvolvimento do CNF. Com base no fato de que as proteínas LMP1 e Cripto‐1 eram coexpressas em células do CNF e no CNF (figs. 4 e 5), é razoável acreditar que elas estão envolvidas em várias vias de sinalização no desenvolvimento do tumor. Pode haver um fator de efeito de sinalização comum, que pode constituir um novo alvo em potencial para diagnóstico precoce e terapia‐alvo, bem como um novo marcador molecular prognóstico para CNF.
ConclusãoComo sugerido por este estudo, LMP1 e Cripto‐1 podem ser coexpressas no CNF. A expressão de Cripto‐1 é provavelmente regulada e afetada pela proteína LMP1. A proteína Cripto‐1 pode ser uma proteína efetora chave nas vias de sinalização reguladas pela proteína LMP1, promove desse modo a invasão tumoral e metástases. Portanto, vale a pena estudar os efeitos da regulação da LMP1 na expressão de Cripto‐1 na invasão e na metástase de CNF para entender as características moleculares da progressão do tumor e o mecanismo molecular do prognóstico do CNF.
Conflitos de interesseOs autores declaram não haver conflitos de interesse.
Este trabalho foi apoiado em parte pela pesquisa conjunta de alto nível e programa de construção do Hospital Provincial de Fujian (2017LHJJ07), Fundação Nacional de Ciências Naturais da China (Concessão n° 61475036,81471703), Disciplina de Especialidade Clínica do Programa de Construção de Fujian (Fujian HealthMedicine and Politics 2015 n° 593) e Projeto de Desenvolvimento de Equipe de Inovação (n° IRT 15R10).
Como citar este artigo: Ye Q, Li J, Wang X, Zhang X, Lin J, Huo Y, et al. In vivo and in vitro study of co‐expression of LMP1 and Cripto‐1 in nasopharyngeal carcinoma. Braz J Otorhinolaryngol. 2020;86:617–25.
A revisão por pares é da responsabilidade da Associação Brasileira de Otorrinolaringologia e Cirurgia Cérvico‐Facial.