As alterações neurológicas podem gerar distúrbios deglutitórios e a videoendoscopia da deglutição é um dos exames feitos para o seu diagnóstico e auxílio no manejo da disfagia.
ObjetivoIdentificar e descrever o protocolo para videoendoscopia da deglutição padronizado para a população adulta com transtornos neurológicos e suas etapas.
MétodoRevisão sistemática registrada na plataforma Prospero (CRD42018069428), realizada nos sites: Medline, Cochrane Library e Scielo; publicados entre 2009 e 2020. Foram incluídos ensaios clínicos randomizados, estudos transversais e longitudinais. Dois avaliadores independentes analisaram o delineamento do estudo e extrairam os dados dos estudos selecionados. As dúvidas de inclusão ou não dos estudos foram avaliadas por um terceiro avaliador. Artigos científicos incluídos englobam pacientes adultos neurológicos. Os desfechos avaliados: 1) diagnóstico de distúrbio deglutitório ou disfagia; (2) alteração de sensibilidade em região laríngea; (3) penetração laríngea do bolo alimentar ofertado; (4) aspiração traqueal do bolo alimentar ofertado.
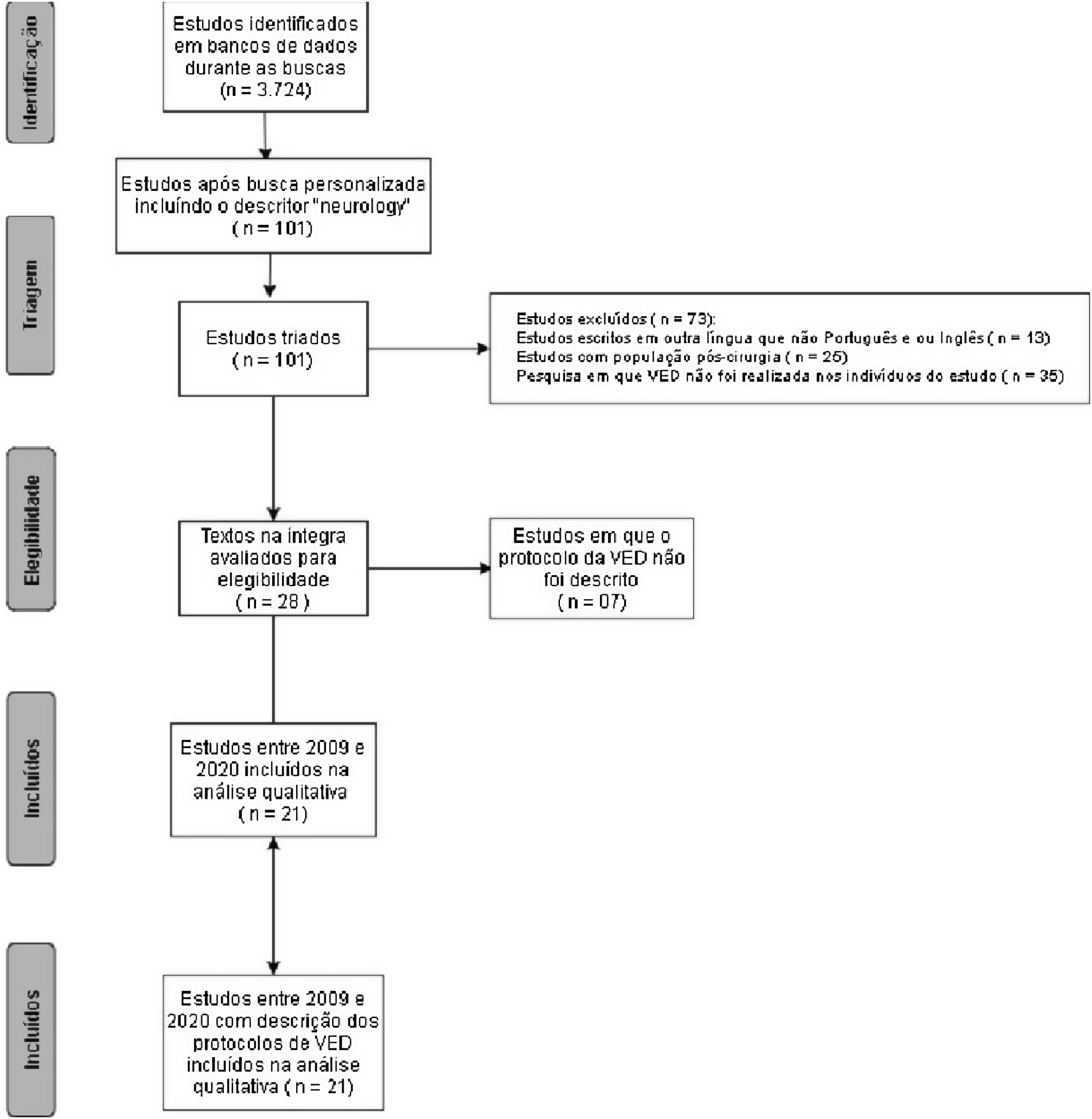
ResultadosForam selecionados inicialmente 3.724 artigos, após busca personalizada para pacientes com alterações neurológicas permaneceram 101 estudos. Ao final, 21 estudos qualitativos de 2009 a 2020 permaneceram na revisão sistemática e foram descritos detalhadamente e comparados. Sete estudos usaram protocolos das instituições promotoras e quatro citaram usar o mesmo protocolo. A reprodutibilidade fidedigna dos protocolos é viável apenas em três dos artigos, mesmo com protocolos diferentes.
ConclusõesNão há protocolo padronizado ou validado para avaliar a deglutição da população adulta neurológica.
A avaliação endoscópica da deglutição (FEES ou VED) é um dos exames usado para avaliar a função da deglutição e, atualmente, é considerado um exame já estabelecido para identificação de disfagia tanto em crianças quanto em adultos. Descrita em 1988 por Langmore1 em artigo científico, em 2001 a VED teve as suas etapas detalhadas.2 Recentemente publicou‐se um estudo histórico sobre a VED,3 que descreve a evolução dos protocolos utilizados para a realização do exame e o seu manejo da disfagia, assim como algumas validações em populações específicas.
Alguns estudos publicados sobre a VED se detiveram na validação de protocolos para populações específicas, como pacientes extubados,4 frente ao câncer de cabeça e pescoço,5 junto aos traqueostomizados,6 na paralisia de prega vocal,7 osteopatia,8 miastenia gravis.9 Outros estudos validaram protocolos de VED para populações com transtornos neurológicos. Entretanto, nem todos descreveram o protocolo usado e validado, de forma a ser usado na prática clínica, ou mesmo ter seu estudo reproduzido para confirmação de resultados em populações similares.
O foco do uso da VED frente às populações de etiologia neurológica apresenta algumas particularidades, visto que a realização do exame na população adulta neurológica pode ser dificultada em razão de fatores como: o aspecto cognitivo;10,11 a postura de tronco e cabeça durante o exame; e a ocorrência de fadiga.12–14 Esses fatores podem levar à interrupção do exame, o que dificulta o diagnóstico e plano terapêutico.
Em geral, o protocolo de avaliação da VED é dividido em três etapas: a primeira é a observação cuidadosa da anatomia, das secreções e a visualização dos movimentos das estruturas nasais, orofaríngeas e laríngeas frente à solicitação de fala e respiração. Alguns protocolos incluem a avaliação da sensibilidade de região orofaríngea, através do toque do endoscópio em regiões específicas;15,16 a segunda etapa se constitui pela avaliação direta da deglutição, com oferta de comidas e líquidos em diferentes consistências; a terceira compõe‐se da verificação de manobras posturais, variações de consistências e pela observação de comportamentos alimentares, identificam‐se, diretamente, posturas e consistências alimentares que favoreçam a ingestão oral de forma mais segura.
As avaliações instrumentais para avaliar a função da deglutição,a VED e a videofluoroscopia da deglutição (VFSS) são consideradas padrão‐ouro.17
A VFSS é um exame em que se observa o processo da deglutição desde a captação do bolo, passa por todas as fases da deglutição (fase preparatória oral, fase oral, fase faríngea e fase esofágica).18 Logo, esse é um exame que determina o grau (leve, moderado, grave) de alteração da deglutição. Em contrapartida, a VED observa a fase faríngea da deglutição, contudo tem a vantagem de identificar o exato local de resíduo nessa fase da deglutição, a sua quantidade e identificar qual manobra melhor faz a limpeza parcial ou total desse resíduo. Adicionalmente, a VED, pelo fato de não usar radiação, demonstra maior facilidade de reprodutibilidade e replicabilidade, tanto em pacientes no leito quanto em ambulatório. Portanto, na população adulta com transtornos neurológicos, em sua avaliação e em seu acompanhamento terapêutico, a VED frequentemente é indicada.19
Logo, o uso de protocolo específico por fonoaudiólogos e médicos durante a execução da VED facilita a realização do exame e do diagnóstico clínico, oferece recomendações baseadas em evidências e reduz índice de variações. O objetivo deste estudo é identificar e descrever, com base na revisão sistemática da literatura científica, o protocolo da VED para ser usado na população adulta neurológica com detalhamento e possibilidade de padronização mundial.
MétodoFez‐se uma revisão sistemática da literatura, norteada pela pergunta: “Existe um protocolo para realização da VED e, se sim, é validado para ser usado universalmente junto aos pacientes adultos com doenças neurológicas?”
Este estudo foi registrado junto à plataforma Prospero (CRD42018069428). As bases de dados consultadas foram PubMed/Medline, Cochrane Library, Web of Science e SciELO. Os principais descritores relacionados ao tema investigado, cruzados foram: avaliação VED; adultos; doença neurológica avaliação da deglutição, como mostram as estratégias apresentadas na tabela 1. O desfecho de cada estudo foi considerado, ou seja: presença de diagnóstico de transtorno de deglutição ou disfagia; sensação laríngea prejudicada (em nível das pregas vocais); presença de penetração laríngea de bolo alimentar; e/ou ocorrência de aspiração traqueal.
Estratégias de busca para os bancos de dados selecionados
| Banco de dados | Período de busca | Descritores usados Decs e Meshs | Resultado inicial (n) |
|---|---|---|---|
| PubMed/ Medline | Março a Julho/2018 | Endoscopic swallowing assessment AND assessment procedures fiberoptic endoscopic evaluation of swallowing AND protocols of assessments | 445 |
| Março/2020 | Endoscopic swallowing assessment AND assessment procedures fiberoptic endoscopic evaluation of swallowing AND protocols of assessments | 1546 | |
| Março/2020 | Endoscopic swallowing assessment AND assessment procedures AND neurology | 77 | |
| Cochrane Library | Março/2018 | Endoscopic swallowing assessment AND assessment procedures fiberoptic endoscopic evaluation of swallowing AND protocols of assessments | 83 |
| Março⧸2020 | Endoscopic swallowing assessment AND assessment procedures fiberoptic endoscopic evaluation of swallowing AND protocols of assessments | 1630 | |
| Março⧸2020 | Endoscopic swallowing assessment AND assessment procedures AND neurology | 14 | |
| SciELO. | Março/2018 | Endoscopic swallowing assessment AND assessment procedures fiberoptic endoscopic evaluation of swallowing AND protocols of assessments | 20 |
| Março/2020 | Endoscopic swallowing assessment AND assessment procedures fiberoptic endoscopic evaluation of swallowing AND protocols of assessments | 20 | |
| Março/2020 | Endoscopic swallowing assessment AND assessment procedures AND neurology | 10 |
A revisão incluiu estudos transversais, ensaios clínicos randomizados e estudos de coorte longitudinais, que usaram a avaliação VED como avaliação‐padrão, junto aos pacientes com doenças neurológicas. Outros tipos de estudos ou formatos foram excluídos, bem como estudos transversais que incluíram crianças e/ou adolescentes. A seleção dos artigos cobriu o período entre 2009 e 2019. O levantamento dos dados bibliográficos ocorreu entre março de 2018 e março 2020, com base nos critérios de inclusão supracitados (tabela 1)
A primeira fase da seleção de artigos foi a exclusão de estudos duplicados, seguida da leitura e análise de títulos e resumos de todos os trabalhos identificados. Após, ocorreu a leitura completa dos estudos selecionados, o que levou à exclusão de trabalhos que não atenderam à proposta da revisão. Os artigos selecionados foram submetidos à avaliação metodológica de acordo com a lista de verificação fornecida pelo relatório Strengthening the Reporting of Observational Studies in Epidemiology (Strobe)20 para estudos transversais, os quais receberam o valor 1 quando o item foi contemplado, 0 quando não contemplado e 0,5 quando parcialmente contemplado. Após, foram estabelecidas as médias entre os valores atribuídos pelos dois avaliadores. Todas as fases foram feitas por dois dos autores/pesquisadores, de maneira independente. Frente a dúvidas de inclusão do estudo ou não, o terceiro autor/avaliador foi acionado. Este estudo incluiu apenas os artigos com pelo menos 70% do escore determinado pela lista de verificação Strobe. A média aritmética de pontuação dos estudos foi de 17,86; totalizando uma proporção de 81% de escore Strobe. Os artigos incluídos foram analisados quanto à declaração de possibilidade de viés, limitações dos estudos, número de participantes, gênero, idade e método estatístico (tabela 2). Todos os procedimentos da revisão aqui apresentados foram conduzidos de acordo com Checklist Preferred Reporting Items for Systematic Reviews and Meta‐Analyses (Prisma).
Média entre avaliadores cegados da avaliação de publicação dos estudos observacionais segundo a ferramenta Strobe
| Itens/Artigos – média | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1. Título e Resumo | 1 | 1 | 1 | 1 | 0,75 | 1 | 0,75 | 1 | 1 | 1 | 0,75 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 |
| 2. Introdução: Contexto//fundamentos | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 |
| 3. Objetivos | 0,75 | 1 | 0,75 | 1 | 1 | 1 | 1 | 0,75 | 1 | 0,5 | 0,75 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 |
| 4. Método: Desenho do estudo | 0,5 | 1 | 1 | 0 | 0,5 | 1 | 1 | 0,5 | 1 | 1 | 0,5 | 1 | 1 | 0,5 | 0,5 | 0,5 | 1 | 1 | 1 | 0,5 | 1 |
| 5. Contexto | 0,5 | 0,75 | 1 | 0,75 | 0,75 | 1 | 0,75 | 1 | 1 | 1 | 0,75 | 1 | 0,5 | 0,75 | 1 | 1 | 1 | 1 | 1 | 0,75 | 0,75 |
| 6. Participantes | 1 | 1 | 0,5 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 0,75 | 0,75 | 1 | 1 | 1 | 1 | 1 | 1 | 1 |
| 7. Variáveis | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 0,75 | 1 |
| 8. Fontes de dados//medidas | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 0,5 | 1 | 1 | 0,75 | 1 |
| 9. Vieses | 0,5 | 0,5 | 0,25 | 0,5 | 0,25 | 0,5 | 0,5 | 0,5 | 0,25 | 0,25 | 0,5 | 0,25 | 0,25 | 0,5 | 0 | 0,25 | 0 | 0 | 0,5 | 0,25 | 0 |
| 10. Tamanho amostral | 0,5 | 0,5 | 0 | 0 | 0 | 1 | 0,25 | 0,25 | 0,25 | 0,5 | 0,25 | 0,5 | 0 | 0,25 | 0,5 | 0,25 | 0,5 | 0 | 0,5 | 0,5 | 0,5 |
| 11. Variáveis quantitativas | 0,5 | 0,5 | 1 | 1 | 0,5 | 1 | 1 | 0,5 | 0,5 | 0,5 | 0,5 | 0,5 | 0,75 | 0,5 | 0,5 | 0,5 | 0 | 0,5 | 1 | 0,5 | 0,5 |
| 12. Métodos estatísticos | 1 | 1 | 0,25 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 0,5 | 1 | 0 | 1 | 1 | 1 | 0,5 |
| 13. Resultados: Participantes | 1 | 1 | 1 | 1 | 0,75 | 1 | 0,75 | 1 | 1 | 1 | 0,75 | 1 | 0,75 | 1 | 1 | 1 | 1 | 0,5 | 1 | 1 | 0 |
| 14. Dados descritivos | 0,5 | 0,75 | 1 | 0,75 | 0,75 | 1 | 0,75 | 0,75 | 1 | 0,75 | 0,75 | 0,75 | 0,75 | 0,75 | 0,75 | 0,75 | 0,75 | 0,5 | 0,75 | 0,75 | 0,25 |
| 15. Dados das variáveis | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 0,75 | 1 |
| 16. Resultados principais | 1 | 0,75 | 1 | 1 | 1 | 1 | 0,75 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 0,75 | 1 | 1 | 0,5 |
| 17. Outras análise | 1 | 1 | 0,25 | 1 | 1 | 1 | 0,5 | 0,25 | 1 | 1 | 0,5 | 0,5 | 1 | 0,5 | 0,5 | 1 | 0 | 0,5 | 0,5 | 0,5 | 0 |
| 18. Discussão: Resultados chave | 1 | 1 | 1 | 1 | 1 | 0,75 | 1 | 1 | 1 | 1 | 1 | 0,75 | 1 | 1 | 0,75 | 1 | 1 | 1 | 1 | 1 | 1 |
| 19. Limitações | 0,75 | 0,75 | 0 | 1 | 1 | 1 | 1 | 0 | 0,25 | 0,5 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 0,25 | 0,75 |
| 20. Interpretação | 1 | 1 | 1 | 1 | 1 | 0,5 | 1 | 0,75 | 1 | 1 | 1 | 1 | 0,75 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 |
| 21. Generalização | 0,75 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 0,25 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 0,5 |
| 22. Outra informação: Financiamento | 1 | 0,5 | 0 | 0 | 1 | 0,5 | 1 | 1 | 0,5 | 0 | 1 | 1 | 0 | 0 | 0,25 | 0 | 0,5 | 1 | 0,5 | 0 | 1 |
| Total | 18,25 | 19 | 16 | 18 | 18,25 | 20,25 | 19 | 17,25 | 18,75 | 18 | 18 | 19,25 | 16,75 | 17,5 | 17,25 | 18,25 | 16,25 | 17,75 | 19,75 | 16,25 | 15,25 |
1. Warnecke et al.26; 2. Mandysova et al.21; 3. D’ottaviano et al.31; 4. Pilz et al.36; 5. Somasundaram et al.37; 6. Leder et al.22; 7. de Lima Alvarenga, et al.23; 8. Marian et al.32; 9.Nienstedt et al.27; 10. Pflug et al.28; 11. Umay et al.40; 12. Braun et al.24; 13. Farneti et al.41; 14. Imaizumi et al.34; 15. Schröder et al.35; 16. Shapira‐Galitz et al.30; 17. Souza et al.38;18. Souza et al.39; 19. Suntrup‐Krueger et al.25; 20. Warnecke et al.29; 21. Gozzer et al.33
A média aritmética entre os trabalhos avaliados foi de 17,03 pontos, sendo a mínima pontuação a de 15,25 e a máxima de 20,25. A pontuação mínima para a avaliação dos estudos foi de 69% e a média foi de 78% de aplicabilidade dos estudos.
A seleção dos estudos feita por dois avaliadores independentes em três bancos de dados, conforme descrito na metodologia. Ao total encontrou‐se 3.824 estudos publicados com base nos descritores cruzados “fiberoptic endoscopic evaluation of swallowing AND protocols of assessments” e “endoscopic swallowing assessment AND assessment procedures”.
A partir da busca personalizada e da inclusão do descritor “neurology” com vistas ao direcionamento para artigos feitos com população adulta neurológica, foram eleitos 77 artigos na plataforma PubMed, 14 na Cochrane Library, 10 na Scielo, totalizaram 101 artigos. Em busca de elegibilidade dos artigos e a partir da leitura de resumos, foram excluídos os artigos que não contemplavam os critérios de inclusão do estudo e permaneceram 28 artigos para a leitura na íntegra e esses foram analisados por duas avaliadoras cegadas.
No fim, 21 estudos publicados entre 2009 e 2020, consideradas como publicações atualizadas, foram incluídas na revisão sistemática por serem os únicos com protocolos completos de VED descritos nas publicações. A descrição da busca dos artigos é descrita na figura 1 com base nas diretrizes Prisma (fig. 1).
Desses, 18 estudos são transversais, 2 transversais longitudinais e um de aplicação de protocolo desenvolvido por meio de coorte. As doenças neurológicas avaliadas nos estudos selecionados foram: paralisia supranuclear progressiva (PSP), esclerose lateral amiotrófica (ELA), idosos hospitalizados com alguma condição de saúde, doença de Parkinson (DP), acidente vascular encefálico (AVE), distrofia miotônica tipo 1 (DM1), miastenia gravis (MG), idosos> 60 anos, traumatismo cranioencencefálico (TCE) e demência vascular. A descrição dos artigos e as características metodológicas dos artigos constam na tabela 3.
Análise dos estudos selecionados
| Autor, data de publicação | Doença neurogênica | Número de pacientes/ sexo | AvaliaçãoAssociada | Etapas da VED | Consistências Testadas (alimento/utensílio) | Volumes | Resultados da VED na Função Deglutitória |
|---|---|---|---|---|---|---|---|
| Warnecke et al., 200929 | AVC agudo | 153 (80 mulheres) | Protocolo de Dzeiwas feito por neurologista e fonoaudiólogoVED após 24 horas da admissão hospitalar | 1. Avaliação estrutural inicialmente com endoscopia2. Avaliação do gerenciamento de secreções3. Avaliação funcional da deglutição | a. Pastosab. Líquidoc. Sólido‐macio | a. Colher de chá de purêb. Colher de chá de água com contraste alimentícioc. pequeno pedaço de pão branco | Escala de 6 pontos para determinar severidade da disfagia, sendo que 1 sem penetração laríngea ou aspiração laringotraqueal com sólido macio (sem alteração) e 6 penetração ou aspiração com saliva (grave) |
| Obs: Quantidade e número de ofertas não especificadas | |||||||
| Warnecke et al., 201026 | PSP | 18/11 homens | Levodopa‐test; FEES com acompanhamento de ORL e Fonoaudióloga | 1. VED em estado “off” de levedopa; | a. Pudim (gelatina) | a. 3×8mL pudim | Escape posterior do alimento ou líquido; |
| DP | 15/11 homens | 2. Dose de 200mg levedopa administrada | b. Líquido (água) | b. 3×5mL líquido | Eventos de penetração e ou aspiração; | ||
| 3. Nova VED era feita 60min após | c. Sólido macio (pão branco) | c. 3× pedaços de pão (3 cm/ 3 cm/ 0,5 cm) | Presença ou ausência de resíduos | ||||
| Obs: Todos os alimentos corados de azul ou verde | |||||||
| Mandysova et al., 201121 | AVC | 87/SD | Brief Bedside Dysphagia Screening TestFEES com acompanhamento de ORL e enfermeira | 1. Avaliação física – função motora dos músculos e reflexos envolvidos na deglutição; | a. Líquido grosso | a. Quatro colheres de chá | Escala de Penetração‐aspiração Rosenbek et al. |
| MG | 2. Avaliação funcional da deglutição | b. Líquido fino (colher) | b. Quatro colheres de chá | ||||
| DP | c. Líquido fino (copo) | c. 60mL no copo | |||||
| ELA | d. Avaliação voz paciente após deglutições | Obs.: Caso o paciente tossir, engasgar, apresentar voz molhada ou escape de líquido da boca em tempo<de 1min o exame era interrompido. | |||||
| ORL | Obs.: Não especificado se os alimentos foram corados durante execução dos exames | ||||||
| D’Ottaviano et al., 201331 | ELA | 11 (6 homens) | Protocolo descrito no estudo, acompanhado por ORL e Fonoaudióloga | 1. Questionário auto avaliação da deglutição | a. Pastoso (água mais duas colheres de espessante Resource Thicken Up ‐ Nestlé® | a. 5 e 10 mL | Escape posterior |
| 2. Avaliação mobilidade de língua e fasciculações | b. Líquido (água) | b. 5 e 10 mL | Resíduo de comida | ||||
| 3. Avaliação funcional da deglutição | c. Sólido (bolacha água e sal) | c. Metade de bolacha água e sal | Penetração laríngea | ||||
| Obs: Todos os alimentos corados de azul. | Aspiração traqueal | ||||||
| Cronometragem de tempo até ocorrer a aspiração traqueal | |||||||
| Resposta à aspiração traqueal | |||||||
| Pilz et al., 201436 | DM1Controles | 45 DM1 (28 homens) | Protocolo de LangmoreEscala funcional de ingestão oral – FOISAcompanhado por otorrinolaringologista e fonoaudióloga. | 1. Paciente sentado. | a. Líquido fino (água) | a. 10mL (3 ofertas) | Escala FOIS e percepção visual das variáveis durante VED: |
| 10 controles (7 mulheres) | 2. Avaliação da funcionalidade e morfologia das estruturas orofaríngeas | b. Líquido grosso (purê de maçã) | b. 10mL (3 ofertas) | Deglutições múltiplas | |||
| 3. Bolo alimentar ou líquido inserido em cavidade oral por meio de seringa | c. sólido (bolacha água e sal) | c. 1 pedaço de sólido | Latência no início do reflexo faríngeo | ||||
| Obs.: Todos os alimentos corados de azul. | Resíduo em valécula pós‐ deglutição | ||||||
| Resíduo em seios piriformes pós‐ deglutição | |||||||
| Penetração laríngea ou aspiração traqueal | |||||||
| Somasundaram et al., 201437 | AVC agudo de artéria cerebral média esquerda | 67 (todos homens) | Entrevista inicial ‐ história clínica completa; | VED feita por fonoaudióloga e neurologista experientes;Protocolo de Langmore2; | 1. Líquido espessado | a. 3× água espessada | Avaliação da disartria, disfonia, tosse volitiva e reflexo de GAG; |
| Exame físico;EAT‐10 antes da realização da VED; | 1. Avaliação estrutural | 2. Semisólido | b. 3× pudim | Escala de penetração‐aspiraçãoFrente à presença de resíduo faríngeo, paciente foi observado por 2min para identificar deglutição voluntaria após, para limpeza oral; | |||
| Avaliação Cínica da Deglutição – protocolo do local;VED; | 2. Observação de secreção ou acúmulo de saliva | 3. Líquido | c. 3× água | ||||
| Obs: pacientes da unidade de AVC triados por médicos e avaliados por fonoaudiólogo após 24 horas da admissão; | 3. Avaliação funcional da deglutição | 4. Sólido | d. 3× pão branco | ||||
| Obs: Todas as consistências foram coradas com corante alimentício azul. | Obs: Quantidades não especificadas. | ||||||
| Leder et al., 201622 | Idosos hospitalizados | 961 (524 homens) | Yale Swallow ProtocolVED – com Protocolo Padrão Langmore modificado, como avaliação complementar para alguns pacientes;Acompanhado por ORL e Fonoaudióloga | 1. Visualização da narina mais pérvia para passagem de endoscópio sem anestesia; | a. Pastoso (pudim) | 5 a 10mL para cada consistência | Presença ou ausência de Aspiração traqueal; |
| 2. Avaliação morfológica das estruturas da orofaringe; | b. Líquido (leite desnatado) | Deglutição funcional definida com ausência de aspiração; | |||||
| 3. Avaliação funcional da deglutição | c. Sólido (bolacha água e sal) | Deglutição não funcional com presença de aspiração em qualquer das consistências testadas durante VED. | |||||
| Obs: Não especificado se alimentos foram corados durante execução dos exames. | |||||||
| Marian et al., 201732 | AVC | 50 (25 cada sexo) | Triagem de deglutição com água, frente a presença de sintomas preditivos de disfagia, encaminhamento para a VED;Protocolo da Langmore com modificações;Escala de 6 pontos para AVC;Acompanhamento clínico por neurologista e fonoaudióloga. | 1. Pacientes avaliados no leito em unidade de AVC com cabeceira elevada | a. Pastoso (pudim) | 3×3mL para cada consistência | Escala Penetração‐aspiração ‐ Escala FEEDS – escala de 6 pontos de severidade de disfagia em avaliação endoscópica (1 sendo o melhor desempenho e 6 sendo o pior desempenho) |
| 2. Endoscópio era passado pela narina mais permeável com aplicação de anestésico local | b. Líquido (não especificado) | ||||||
| 3. Acúmulo de secreção em região orofaríngea avaliado conforme escala de gravidade | c. Sólido macio (pão branco) | ||||||
| 4. Avaliação funcional da deglutição | Obs: Todos os alimentos corados de azul. | ||||||
| Alvarenga et al., 201723 | Idosos>60 anos | 100 idosos (58 mulheres) | Entrevista inicialProtocolo de Langmore modificadoAcompanhamento médico. | Auto administrado pelo participante: | a. Pudim morango | a. 10 mL | Avaliados como desfechos: |
| 1. Avaliação da funcional da deglutição | b. Leite desnatado | b. 50mL em copo | 1. Estase de saliva na faringe | ||||
| c. Bolacha água e sal | c. Uma bolacha água e sal. | 2. Resíduo faríngeo | |||||
| Obs: Alimentos corados de verde com corante alimentício. | 3. Penetração laríngea | ||||||
| 4. Aspiração laringo‐traqueal | |||||||
| 5. Sensibilidade laríngea. | |||||||
| Nienstedt et al., 201727 | DP | 119 DP | VED com acompanhamento de ORL; | 1. Aplicação de lidocaína | a. Líquida | a. 90mL água | Escala penetração‐aspiração, Escala de Murray na versão breve |
| 32 Controle | Avaliações:MDS‐UPDRS; Escala H&Y;NMS‐Quest;MOCADSFS | 2. Avaliação funcional da deglutição | b. Sólido | b. Biscoito (91mm e 20g) | |||
| c. Sólido macio | c. Metade de um pão com manteiga (94×90×9mm, 28g) | ||||||
| Pflug et al., 201828 | DP | 119 DP | VED com ORL cegados para os estágios da doença;Avaliação MDS‐UPDRSEscala H&YNMS‐QuestMOCAAvaliação da depressão – questionário de Beck, versão alemã | 1. Avaliação inicial com ORL com solicitação para: tossir ou pigarrear após comer ou beber; histórico de aspiração ou pneumonia; | a. Líquida | a. Colher de chá para água | Escala de restrições de deglutição – SSR |
| 32 Controle | 2. Avaliação funcional da deglutição | b. Sólida | b. 90mL água com canudo | Escala de penetração‐aspiração | |||
| c. Sólido macio | c. 1 biscoito (91mm, 20g) | Escape prematuro posterior e resíduos. | |||||
| d. Meio pedaço de pão com manteiga (95×90×9, 28g) | |||||||
| Umay et al., 201840 | MG | 36 MG (20 mulheres) | VED | 1. Sem anestesia | a. Líquida | a. Água (90 mL) | Escore de nível da disfagia foi usado 1–6, sendo 1 deglutição normal e 2–6 foi considerado disfagia, de leve a severa. |
| 25 Controle(14 mulheres) | Manometria | 2. Protocolo de Dzeiwas | b. Semi‐sólida | b. Iogurte | |||
| EAT‐10 | c. Sólida | c. Biscoito | |||||
| Eletromiografia de superfície | |||||||
| VFD | |||||||
| Braun et al., 201924 | Idosos pós‐AVC | 152 (94 homens) | GUSSVED considerando Protocolo padrão Langmore frente a sinais e sintomas de disfagia | 1. Aplicação de descongestionante nasal (Xylometazolin) e anestesia local (2% lidocaína gel) | a. Pastosa | a. 3× água com espessante | Escala de penetração‐aspiração de Rosenbek.Desfechos: FOIS, FEDSS |
| 2. Observação das estruturas anatômicas, mobilidade das estruturas e gerenciamento de saliva | b. Líquido | b. 3× água rala | |||||
| 3. Avaliação funcional da deglutição | c. Sólido | c. 3× sólido (não especificado) | |||||
| Obs: Oferta em colher de chá; colher de sopa; e gole no copo. | |||||||
| Farnetti et al., 201941 | Diferentes etiologias: DP, demência vascular, AVC, TCE. | 16 adultos (11 homens) | Protocolo próprio com consistências baseadas na iniciativa globalVED associada a escala penetração‐aspiração, FOIS e DOSS | 1. Avaliação da funcional da deglutição | a. Pastosa | a. 5cc pure | Vídeos avaliados por 2 avaliadores independentes e experientes em VED. |
| b. Sólida | b. 1⧸4 bolacha cracker (água e sal) | Desempenho da deglutição avaliado por: Escala penetração‐aspiração, FOIS e DOSS. | |||||
| c. Líquida | c. 5 cc líquido | Desfecho: tempo médio para limpeza de resíduos/consistência. | |||||
| Imaizumi et al., 201934 | Idosos com diferentes comorbidades: doença cerebrovascular, demência, DP | 106 (76 mulheres): | VED feito em pacientes com risco para disfagia com base em respostas de dois questionários como EAT‐10Triagem com VED | 1. VED feita por ORL | a. Grau de acúmulo de saliva em valécula e seios piriforme; | Saliva | FEES associado a Escala Penetração‐aspiração |
| G1– alteração deglutitória detectável; | Sem alimentos – para identificação da severidade da alteração de deglutição | 2. Avaliação sem alimentos com base no sistema desenvolvido por Hyodo et al. | b. Reflexo de fechamento glótico com toque de endoscópio em epiglote ou aritenóide | Nível de cuidado necessário | |||
| G2 – alteração deglutitória não detectável | c. Reflexo de início da deglutição com base em tempo de white‐out. | Nível de consciência | |||||
| d. Limpeza e clareamento faríngeo após deglutição de 3mL de água corada | Habilidade de comer via oral | ||||||
| Habilidades em atividades de vida diária | |||||||
| Suntrup‐Krueger et al., 201925 | AVC agudo recém extubados | 133 | VED feita 48h após extubação acompanhado por fonoaudióloga e neurologista. | 1‐ Avaliação do gerenciamento das secreções | a. Pastosa | Não especificados os volumes para cada consistência | Sensibilidade (intacta, reduzida ou ausente) |
| Avaliações para extubação: | 2‐ Observação de deglutições espontâneas por minuto | b. Líquido | FEDSS>1 considerado disfagia | ||||
| Escala de coma de Glasgow, Temperatura corporal, Batimentos cardíacos, Pressão sistólica, Respiração espontânea em volume, Pressão positiva na expiração, Índice de respiração superficial rápida | 3‐ Avaliação da sensibilidade laríngea pelo toque em estruturas faringolaríngeas | c. Sólido macio | 3‐Ounce teste com água feito 72h após extubação e 24h após FEES | ||||
| 4‐ Protocolo de FEES validado para pacientes pós‐AVC | |||||||
| Schroder et al., 201935 | DP | Coorte de 105 pacientes,20 pacientes selecionados: | Protocolo de Langmore | 1. Avaliação funcional da deglutição | a. Pastosa | a. Gelatina verde | Escape prematuro |
| G1 – 10 sem sinais de disfagia; | b. Líquido | b. Água corada azul | Eventos de penetração‐aspiração | ||||
| G2 – 10 com sinais de disfagia faríngea | c. Sólido macio | c. Pão branco (3×3×0,5 cm) | Resíduos avaliados pela Escala de severidade de disfagia de 0–3, sendo 0 sem alterações deglutitórias e 3 sendo disfagia grave (penetração‐aspiração com 2–3 consistências). | ||||
| Substância P da saliva foi coletada no G1 e no G2 | |||||||
| Shapira‐Galitz et al., 201930 | AVC | 136 (25 do Kaplan Medical Center e 111 do Sheba Medical Center) | Protocolo de Langmore com pequenas modificações | 1. Pequena quantidade de anestesia local (gel de 2% de Lindocaina hidroclorida) | a. Pastosa | a. Purê de maçã com corante verde (com colher) | Escala de penetração‐aspiração |
| TCE | 51 controle | 2. Avaliação funcional da deglutição | b. Sólido | b. Pão integral (dois pedaços com casca e um sem casca) | Resíduos determinados como 0 se ausente em todas as consistências e 1 para resíduo apresentado em cada consistência, sendo a máxima pontuação 3 se presente nas três consistências | ||
| Doenças neuromusculares degenerativas | c. Líquido | c. Leite 3% de gordura com corante verde (com canudo e direto no copo) | |||||
| Obs: 3 ofertas de cada consistência, com aproximadamente 5cc de volume cada bolo | |||||||
| Souza et al., 2019a38 | DM 1 | 1 (homem, 66 anos) | Avaliação clínica de deglutição | 1. VED com ORL e fonoaudiólogo | a. Pastosa | a. Suco dietético sabor pêssego | Sensibilidade laríngea |
| VED. | 2. Avaliação de sensibilidade laríngea | b. Líquido espessado | b. Suco mais espessante instantâneo | Escape oral prematuro | |||
| 3. Avaliação funcional da deglutição | Obs: Consistências de acordo com IDDSI | Obs: Todas as consistências foram coradas com corante alimentício azul. | Resíduos faríngeos | ||||
| As Consistências ofertadas em 3, 5 e 10ml por meio de colheres descartáveis | Penetração e aspiração laringotraqueal | ||||||
| Souza et al., 2019b39 | AVC | G1:10 (AVC – 8 homens); | VED por médico. | 1. VED feita sem anestesia | a. Pastosa | Obs.: Todas as consistências coradas com corante alimentício azul, oferecidas 5mL, não sendo descritos o número de ofertas e quais alimentos para cada consistência. | Escala de resíduos faríngeos com base na Escala YPRSSRS |
| ELA | G2:10 (ELA – 5 homens); | 2. Avaliação funcional da deglutição com protocolo da instituição | b. Líquida espessada | ||||
| DP | G3:10 (DP –5 homens) | Obs: Consistências de acordo com IDDSI | |||||
| Gozzer et al., 202033 | ELA | 20 (13 homen) | VED feito por ORL e fonoaudiólogo concomitantemente | 1. Estruturas observadas em movimento, inicialmente com emissão da vogal ⧸i⧸ | a. Pastosa | Obs: Não detalha quantidade ofertada em cada consistência | Escape oral posterior; |
| Protocolo de avaliação funcional da deglutição da institucional | 2. Sensibilidade laríngea foi avaliada por toque com nasofibroscópio nas pregas ariepiglóticas e aritenoides | b. Líquido espessado | Resíduo faríngeo; | ||||
| 3. Avaliação funcional da deglutição. | c. Líquido | Penetração laríngea; | |||||
| Obs: Consistências de acordo com IDDSI | Aspiração laringotraqueal |
VED, Vídeo Endoscopia da Deglutição; FESS, Fiberoptic Endoscopic Evaluation of Swallowing; ORL, Otorrinolaringologista; PSP, Paralisia Supranuclear Progressiva; DP, Doença de Parkinson; AVC, Acidente Vascular Cerebral; MG, Miastenia Gravis; ELA, Esclerose Lateral Amiotrófica; sd, sem dados; Obs., Observação; DM 1, Distrofia Muscular do tipo 1; FOIS, Functional Oral Intake Scale; FEEDS, Functional Evaluation of Eating Difficulties Scale; MDS‐UPDRS, Movement Disorder Society's Unified Parkinson's Disease Rating Scale; H&Y, Escala Hoehn & Yahr; NMS‐Quest, Non‐Motor Symptoms Assessed by Non‐Motor Symptoms Questionnaire; MOCA, Montreal Cognitive Assessment; DSFS, Drooling Severity and Frequency Scale; mL, Mililitro;, mm, Milímetro; mg, Miligramas; cc, Centímetro cúbico; SSR, Sympathetic Skin Responses; VFD, Videofluoroscopia da Deglutiçao; GUSS, Gugging Swallowing Screening; DOSS, Dysphagia Outcome and Severity Scale; IDDSI, International Dysphagia Diet Standardization Initiative; YPRSSRS, Yale Pharyngeal Residue Severity Rating Scale.
A avaliação metodológica dos estudos foi feita por meio do relatório Strobe, por avaliação individual de duas avaliadoras cegadas e independentes, e atenderam à proposta desta revisão 21 estudos selecionados para essa revisão sistemática, 5 deles com pontuação alta,21–25 e um em destaque quanto aos seus resultados e análise estatística apresentadas.25
Ao se verificarem os riscos de vieses dentro dos estudos, alguns estudos expuseram suas limitações e encontrou‐se em Warnecke et al.26 que, para evitar viés de aferição, os exames de VED feitos no estudo foram avaliados por dois juízes independentes e aleatoriamente, ou seja, fora da ordem em que os exames foram feitos. Alvarenga et al.23 referiram como uma das limitações do estudo um provável viés de amostra, pois os pacientes que aceitaram provavelmente o fizeram em virtude de apresentar sintomas deglutitórios. Braun et al.24 comentaram sobre um possível viés de seleção ao pesquisar pacientes em unidade de terapia intensiva, demonstraram que a amostra do estudo estava mais severamente acometida. Suntrup‐Krueger et al.25 apontaram limitações sobre possíveis resultados enviesados do estudo pelo fato de em unidade de terapia intensiva haver um alto conhecimento de disfagia pós‐extubação. Nienstedt et al.27 e Pflug et al.28 expuseram que minimizaram o viés de seleção e Warnecke et al.29 comentaram um possível viés de seleção com base nos critérios de inclusão e exclusão do estudo. Shapira‐Galitz et al.30 aventaram uma possibilidade de viés de avaliação no momento em que os pesquisadores precisaram ler o questionário, por telefone, para os pacientes. D’Ottaviano et al.,31 Leder et al.,22 Mandysova et al.,21 Marian et al.,32 Gozzer et al.,33 Imaizumi et al.,34 Schroder et al.,35 Pilz et al.,36 Somasundaram et al.,37 Souza et al.,38 Souza et al.,39 Umay et al.40 e Farnetti et al.41 não descreveram a verificação de vieses.
O número de pacientes avaliados nos estudos selecionados variou de um a 961, todos adultos e ou idosos, entre homens e mulheres, e 6 dos estudos fizeram avaliação em um grupo controle comparativamente com pareamento de idade.25,27,28,30,36,40
Entre os protocolos nos 21 estudos, 7 dos artigos usaram protocolos das instituições onde as pesquisas foram feitas ou mesmo protocolos apenas detalhados nos artigos; 2 usaram o protocolo de Dzeiwas et al.;42 2 estudos usaram protocolo de Langmore;1 2 usaram protocolo de Langmore;43 4 usaram o protocolo de Langmore,2 um artigo fez as avaliações de VED com protocolo de Warnecke et al.;9 um estudo avaliou por meio do Brief Bedside Dysphagia Screening Test;21 um usou o FEES levedopa‐test;26 um fez avaliações sem uso de alimentos por meio do protocolo de Hyodo et al.44 Entretanto, ainda que os estudos tenham citado o uso do mesmo protocolo para realização da VED, na descrição dos protocolos observamos diferenças nas consistências escolhidas, nos alimentos e nos volumes, não caracterizando o mesmo protocolo. A forma de captação das imagens da VED não foi discutida nos artigos, por isso não discutida nesta revisão sistemática.
No detalhamento dos protocolos, apenas 3 dos estudos citaram a International Dysphagia Diet Standardisation Initiative (IDDSI)45 como base para padronizar as consistências alimentares ofertadas durante a VED dos estudos. Nesses foram ofertadas consistências pastosa e líquida espessada e um dos estudos incluiu a avaliação de líquido, além das demais consistências citadas. Três dos artigos apresentaram melhor e mais precisos detalhamentos dos protocolos usados para a realização da VED, Warnecke et al.,26 Shapira‐Galitz et al.30 e Souza et al.,38 especificaram as consistências testadas, declararam os alimentos que foram usados para cada consistência, a quantidade ofertada em cada momento e quantas vezes foi ofertada cada consistência. Dos 21 estudos, 11 citaram haver usado corante alimentício para contrastar a cor dos alimentos em relação às estruturas, de cor azul ou verde e possíveis secreções presentes durante o exame.
Entre os desfechos avaliados pelos estudos Alvarenga et al.23 Gozzer et al.,33 Souza et al.38 Souza et al.39 foram descritos como: escape oral posterior, resíduos faríngeos, penetração laríngea, aspiração laringotraqueal e sensibilidade laríngea. O estudo feito por Souza et al.39 avaliou principalmente resíduos, todos eles de acordo com cada consistência testada. Os estudos de Warnecke et al.9 Warnecke et al.26 Marian et al.32 e Braun et al.24 fizeram uso da escala de severidade para disfagia em seus desfechos, a Fiberoptic Endoscopic Dysphagia Severity Score (FEDSS).9 Quanto à autonomia e capacidade de ingesta por via oral com base na escala Functional Oral Intake Scale (FOIS), foram avaliadas como desfechos pelos estudos de Leder et al.,22 Farnetti et al.,41 Imaizumi et al.34 e por Shapira‐Galitz et al.30 No estudo de Imaizumi et al.34 a Classificação Internacional de Funcionalidade também foi usada para a avaliação. Os desfechos detalhados em cada estudo separadamente estão na tabela 4.
Prevalência e desfechos de deglutição avaliados e demonstrados pelos estudos selecionados
| Autoria do estudo, data de publicação | Desfechos da deglutição | Número absoluto de pacientes que apresentaram o desfecho/total de pacientes (doença de afetação) | ||||||
|---|---|---|---|---|---|---|---|---|
| Warnecke et al., 20099 | FEDSS | N de pacientes que apresentaram cada escore | ||||||
| 1 | 73 | |||||||
| 2 | 25 | |||||||
| 3 | 20 | |||||||
| 4 | 15 | |||||||
| 5 | 12 | |||||||
| 6 | 8 | |||||||
| Predição da FEDSS para escala modificada do ranking | ||||||||
| Independência (mRS 0–2) | 76 (49,7%) | |||||||
| Dependência (mRS 3–6) | 77 (50,3%) | |||||||
| Warnecke et al., 201026 | Severidade da disfagia | |||||||
| Achados não relevantes | 3⧸18 (PSP) | 2⧸15 (DP) | ||||||
| Disfagia leve | 7⧸18 (PSP) | 5⧸15 (DP) | ||||||
| Disfagia moderada | 5⧸18 (PSP) | 3⧸15 (DP) | ||||||
| Disfagia severa | 3⧸18 (PSP) | 5⧸15 (DP) | ||||||
| [1,0]Mandysova et al., 201121 | Alterada VED × Alterada BBDS | 31 (87) × 66 (87); S=87,1%; E=30,4% | ||||||
| Alterada VED × Alterada BBDS pacientes neurológicos | 21 (72) × 57 (72); S=95,2%; E=27,5% | |||||||
| D’Ottaviano et al.201331 | Fases da deglutição alteradas | |||||||
| Preparatória oral | 7/11 (ELA) | |||||||
| Trânsito oral e faríngeo | 11/11 (ELA) | |||||||
| Fase faríngea | 11/11 (ELA) | |||||||
| Penetração laríngea ou aspiração traqueal | 10/11 (ELA) | |||||||
| Pilz et al., 201436 | Aspiração de líquido fino | 17/45 (DM1) | ||||||
| Aspiração de líquido grosso | 02/45 (DM1) | |||||||
| Diferença média entre DM1 × controles | ||||||||
| Líquido fino | 0,56 (0,17, 0,95) | |||||||
| Líquido grosso | 1,27 (0,90, 1,64) | |||||||
| Sólido | 1,63 (0,46, 5,87) | |||||||
| A maior diferença entre os grupos é em relação a um maior pedaço de sólido em comparação ao líquido. | ||||||||
| Somasundaram et al., 201437 | Desfechos de avaliação clínica e VED, n (%) | Disfagia (n=41) | Sem disfagia (n=26) | |||||
| Disartria | 9 (22) | 10 (39) | ||||||
| Disfonia | 4 (10) | 7 (27) | ||||||
| Reflexo GAG alterado | 13 (32) | 2 (8) | ||||||
| Tosse voluntária alterada | 26 (63) | 8 (31) | ||||||
| Tosse após deglutição | 25 (61) | 5 (19) | ||||||
| Alteração vocal após deglutição | 1 (3) | 1 (4) | ||||||
| Leder et al., 201622 | Status de ingesta oral dos pacientes | |||||||
| Homens | ||||||||
| Via oral | 392⧸961 | |||||||
| Nada por via oral | 132⧸961 | |||||||
| Mulheres | ||||||||
| Via oral | 329⧸961 | |||||||
| Nada por via oral | 105⧸961 | |||||||
| Marian et al., 201732 | Escala de severidade da disfagia (FEDSS) | |||||||
| Grade 1 normal | 0/50 (AVC) | |||||||
| Grade 2 | 0/50 (AVC) | |||||||
| Grade 3 | 24/50 (AVC) | |||||||
| Grade 4 | 6/50 (AVC) | |||||||
| Grade 5 | 18/50 (AVC) | |||||||
| Grade 6 grave | 0/50 (AVC) | |||||||
| Alvarenga et al., 201723 | Estase de saliva | 94 (não) 6 (sim) | ||||||
| Resíduo faríngeo | 61 (não) 39 (sim) | |||||||
| Penetração laríngea | 91 (não) 9 (sim) | |||||||
| Aspiração | 98 (não) 2 (sim) | |||||||
| Sensibilidade laríngea | 8 (não) 92 (sim) | |||||||
| Nienstedt et al., 201727 | Escore DSFS | Pacientes DP (119) | PAS 1–2 (80) | PAS 7–8 (28) | Pacientes DP (119) | Controles (32) | ||
| 2 (somente lábios úmidos) | 59 (50%) | 46 (58%) | 11 (39%) | 88 (74%) | 28 (88%) | |||
| 4 | 18 (15%) | 14 (18%) | 4 (14%) | 25 (21%) | 3 (9%) | |||
| 5 | 20 (17%) | 11 (14%) | 5 (18%) | 3 (3%) | 0 (0%) | |||
| 6 | 10 (8%) | 5 (6%) | 3 (11%) | 3 (3%) | 1 (3%) | |||
| 7 | 8 (7%) | 4 (5%) | 2 (7%) | |||||
| 8 | 1 (1%) | 0 (0%) | 1 (4%) | |||||
| 9 Sialorreia (molhando roupas, mãos objetos, constantemente) | 3 (3%) | 0 (0%) | 2 (7%) | |||||
| Pflug et al., 201828 | Pacientes com Doença de Parkinson (119) | |||||||
| Presença de disfagia, n (%) | 113 (95) | |||||||
| Penetração laríngea ou aspiração, n (%) | 66 (55) | |||||||
| Aspiração isolada, n (%) | 30 (25) | |||||||
| Consistência com maior percentagem de aspiração | Líquida (água) | |||||||
| PAS dos pacientes que aspiraram água, n (%) | 7–8, 28 (23,5) | |||||||
| PAS pacientes que aspiraram pão com manteiga, no | 7–8, 5 dos 28 anteriores | |||||||
| PAS 2–6, n (%) | 37 (31%) | |||||||
| Resíduos no geral, mais comumente com pão, n (%) | 111 (93%) | |||||||
| “Build‐up” com pão | 60 (50%) | |||||||
| “Build‐up” considerado severo | 23 (19%) | |||||||
| Escape prematuro (escore>1) para água, n (%) | 11 (8) | |||||||
| Escape prematuro (escore>1) para biscoito, n (%) | 21 (18) | |||||||
| Escape prematuro (escore>1) para pão, n (%) | 4 (3) | |||||||
| Umay et al., 201840 | Desfechos em EAT‐10 e VED | EAT‐10 | VED | |||||
| Grupo 1 (n=24) sem disfagia | 9 (37,5%) | 0 | ||||||
| Grupo 2 (n=12) com disfagia | 10 (83,3%) | 11 (91,7%) | ||||||
| Grupo 3 (n=25) controles saudáveis | 2 (8%) | 0 | ||||||
| Braun et al., 201924 | FEDSS (2–6) determinando disfagia | 110 (72,4%) | ||||||
| FOIS (modificação de dieta) | 105 (69,1%) | |||||||
| 48 (31,6%) com restrição via oral | ||||||||
| 57 (37,5%) diminuição restrições | ||||||||
| 76,6% nada por via oral (não alteraram desfecho inicial pré e pós‐FEES) | ||||||||
| Farnetti et al., 201941 | Tempo – Consistência – escala FOIS: | |||||||
| Tempo total – pastoso | ‐1,32 | |||||||
| Tempo em seg – pastoso | 1,12 | |||||||
| Tempo total – regular (sólido) | ‐1,92 | |||||||
| Tempo seg – regular | ‐2,43 | |||||||
| Tempo total – líquido | ‐0,43 | |||||||
| Tempo seg – líquido | ‐0,90 | |||||||
| Tempo‐Consistência‐escala DOSS: | ||||||||
| Tempo total – pastoso | ‐0,29 | |||||||
| Tempo em seg – pastoso | 0,02 | |||||||
| Tempo total – regular (sólido) | ‐1,33 | |||||||
| Tempo seg – regular | ‐0,93 | |||||||
| Tempo total – líquido | ‐0,48 | |||||||
| Tempo seg – líquido | ‐0,63 | |||||||
| Imaizumi et al., 201934 | Desfechos avaliados: | Alteração de deglutição não detectável (n=64) | Alteração de deglutição detectável (n=42) | |||||
| VED escore | 2 | 5 | ||||||
| Aspiração laringotraqueal (número pacientes) | 7 | 17 | ||||||
| Penetração‐aspiração laríngea escore médio | 1 | 2 | ||||||
| Habilidade de comer via oral (Classificação internacional de Funcionalidade) (número pacientes) nível 2 | ||||||||
| Suntrup‐Krueger et al., 201925 | Extubação bem sucedida (101) | Reintubação (32) | ||||||
| 3‐Ounce teste com água | 16,6±15,5 | 18,1±43,2 | ||||||
| Tempo após a extubação, horas | 12 (17,6) | 13 (68,4) | ||||||
| Fracasso no teste, n (%) | ||||||||
| Avaliação de secreções, n (%) | 70 (82,4) | 6 (23,1) | ||||||
| Normal | 7 (8,2) | 1 (3,8) | ||||||
| Valécula | 7 (8,2) | 7 (26,9) | ||||||
| Vestíbulo laríngeo, temporariamente | 1 (1,2) | 12 (46,2) | ||||||
| Vestíbulo laríngeo, permanentemente | 0,3±0,7 | 2,0±1,2 | ||||||
| Escala de Secreção de Murray | ||||||||
| Frequência de deglutições espontâneas, n (%) | ||||||||
| 0 min | 0 (0,0) | 8 (30,8) | ||||||
| 1–3 min | 32 (37,6) | 15 (57,7) | ||||||
| >3 min | 53 (62,4) | 3 (11,5) | ||||||
| Sensibilidade faríngea, n (%) | ||||||||
| Intacta | 40 (47,1) | 1 (3,8) | ||||||
| Reduzida | 15 (17,6) | 12 (46,2) | ||||||
| Ausente | 4 (4,7) | 7 (26,9) | ||||||
| Não especificada | 26 (30,6) | 6 (23,1) | ||||||
| Consistência pastosa, No expostos (%) | 73 (85,9) | 7 (26,9) | ||||||
| Penetração | 13 (15,3) | 3 (11,5) | ||||||
| Aspiração | 4 (4,7) | 3 (11,5) | ||||||
| Líquido, No expostos (%) | 77 (90,6) | 19 (73,1) | ||||||
| Penetração | 37 (43,5) | 18 (69,2) | ||||||
| Aspiração | 25 (29,4) | 15 (57,7) | ||||||
| Sólido macio, No expostos (%) | 33 (38,8) | 0 (0,0) | ||||||
| Penetração | 1 (1,2) | – | ||||||
| Aspiração | 0 (0,0) | – | ||||||
| Escape posterior | ||||||||
| Sem escape | 21 (24,7) | 0 (0,0) | ||||||
| Em valéculas | 21 (24,7) | 2 (7,7) | ||||||
| Em seios piriformes | 14 (16,5) | 4 (15,4) | ||||||
| Em vestíbulo laríngeo | 17 (20,0) | 17 (65,4) | ||||||
| Não especificado | 12 (14,1) | 3 (11,5) | ||||||
| Schroder et al., 201935 | Discretos resíduos faríngeos, n (%) | 10 (50%) | ||||||
| Local desses resíduos, valéculas | 10 (100%) | |||||||
| Local desses resíduos, seios piriformes | 3 (30%) | |||||||
| Escape prematuro | 0 (0%) | |||||||
| Eventos de penetração⧸aspiração | 0 (0%) | |||||||
| Concentração da substância P na saliva | ||||||||
| Nos pacientes com disfagia faríngea | 9.644 pg⧸mL | |||||||
| Nos pacientes controles | 17.591 pg⧸mL | |||||||
| Shapira‐Galitz et al.,201930 | Desfechos nos pacientes com diagnósticos neurológicos: | 54 (39,7%) | ||||||
| EAT‐10 validação hebraico | 15,87±8,98 | |||||||
| Escala penetração‐aspiração | 4,43±3,04 | |||||||
| VED escore | 2,56±2,0 | |||||||
| FOIS – escala de quantidade de comida ingerida pela boca | 5,85±1,42 | |||||||
| Souza et al., 2019a38 | Primeira VED | Última VED | ||||||
| 5 mL | 10 mL | 5 mL | 10 mL | |||||
| Pastoso | ||||||||
| Escape oral posterior | 1 | 1 | 1 | NT | ||||
| Resíduos faríngeos em valéculas | 2 | 2 | 3 | NT | ||||
| Resíduos faríngeos em seios piriformes | 1 | 2 | NT | |||||
| Penetração laríngea | 0 | 0 | 3 | NT | ||||
| Aspiração laringotraqueal | 0 | 0 | 0 | NT | ||||
| Líquida espessada | 1 | 1 | 1 | NT | ||||
| Escape oral posterior | 1 | 2 | 2 | NT | ||||
| Resíduos faríngeos em valéculas | 1 | 2 | 2 | NT | ||||
| Resíduos faríngeos em seios piriformes | 1 | 1 | 2 | NT | ||||
| Penetração laríngea | 3 | 3 | 5 | NT | ||||
| Aspiração laringotraqueal | 0 | 00 | NT | |||||
| Líquida | ||||||||
| Escape oral posterior | 1 | 1 | 1 | NT | ||||
| Resíduos faríngeos em valéculas | 1 | 1 | 1 | NT | ||||
| Resíduos faríngeos em seios piriformes | 1 | 1 | 1 | NT | ||||
| Penetração laríngea | 3 | 3 | 5 | NT | ||||
| Aspiração laringotraqueal | 0 | 0 | 7 | |||||
| Souza et al., 2019b39 | Frequência total de resíduos em consistências pastosa e líquida | Presença | Ausência | |||||
| Pastosa (n=30) | 19 (63,33%) | 11 (36,67%) | ||||||
| Líquida espessada (n=27) | 16 (59,26%) | 11 (40,74%) | ||||||
| Resíduos em valéculas consistência pastosa | Escala Yale (0–2) | Escala Yale (3–4) | ||||||
| GI | 9 (90%) | 1 (10%) | ||||||
| GII | 9 (90%) | 1 (10%) | ||||||
| GIII | 9 (90%) | 1 (10%) | ||||||
| Resíduos em seios piriformes consistência | ||||||||
| Pastosa | ||||||||
| GI | 10 (100%) | 0 (0%) | ||||||
| GII | 9 (90%) | 1 (10%) | ||||||
| GIII | 10 (100%) | 0 (0%) | ||||||
| Resíduos em valéculas consistência líquida espessada | ||||||||
| GI | 9 (100%) | 0 (0%) | ||||||
| GII | 8 (89%) | 1 (11%) | ||||||
| GIII | 9 (100%) | 0 (0%) | ||||||
| Resíduos em seios piriformes consistência líquida espessada | ||||||||
| GI | 9 (100%) | 0 (0%) | ||||||
| GII | 8 (89%) | 1 (11%) | ||||||
| GIII | 9 (100%) | 0 (0%) | ||||||
| Gozzer et al., 202033 | Desfechos avaliados: | Líquido | Líquido espessado | Pastoso | ||||
| Escape oral posterior | 10 (55%) | 10 (52,6%) | 10 (50%) | |||||
| Resíduo faríngeo | 4 (22,2%) | 8 (42,1%) | 8 (40%) | |||||
| Penetração laríngea | 7 (38,8%) | 5 (26,3%) | 6 (30%) | |||||
| Aspiração laringotraqueal | 3 (16,6%) | 1 (5,2%) | 1 (5%) | |||||
BBDS, Brief Bedside Dysphagia Screening: escala breve de triagem de disfagia no leito; S, Sensibilidade; E, Especificidade; FEEDS, Functional Evaluation of Eating Difficulties Scale; PSP, Paralisia supranuclear progressiva; DP, Doença de Parkinson; VED, Vídeo endoscopia da deglutição; ELA, Esclerose lateral amiotrófica; DM 1, Distrofia muscular do tipo 1; PAS, Escala de penetração‐aspiração; EAT‐10, Eating Assessment Tool; FOIS, Functional Oral Intake Scale; NT, Não Testado.
O objetivo dessa revisão sistemática, de identificar protocolo padronizado e validado para avaliação endoscópica da deglutição em pacientes com doença neurológica de base, não foi contemplado. Todas as pesquisas avaliadas e selecionadas para fazer parte deste estudo trouxeram protocolos descritos e detalhados, porém nenhum validado. Mandysova et al.21 desenvolveram um teste de triagem de disfagia para aplicação à beira do leito e o validaram com base na VED, porém não é um protocolo de VED validado para a população neurológica. Dziewas et al.42 foi citado em alguns dos artigos como protocolo validado de VED, porém se trata do desenvolvimento e da validação de um novo escore de avaliação da gravidade de disfagia, não corresponde a um protocolo de VED validado para população neurológica. Já o Hyodo Score44 foi desenvolvido e validado para identificar a presença e grau da disfagia, de forma indireta, ou seja, sem o uso de líquidos e de alimentos, apenas com base no manejo da secreção e sensibilidade intraoral, em pacientes neurológicos, consequentemente não caracteriza um protocolo de VED, mas um escore de avaliação. Quanto a todos os estudos que citaram protocolo de Langmore, em diferentes anos de publicação (1988, 1998, 2001) e atualizações, esses são considerados guidelines, conforme a própria autora afirma em um artigo recente de 2017,3 necessitam de validação para diferentes populações.
Quanto aos protocolos apresentados pelos estudos selecionados, 7 entre 21 estudos usaram as consistências pastosa, líquida, sólido macio, 6 das pesquisas usaram pastoso, líquido e sólido, os demais estudos usaram consistências diversas, como exemplo de líquido e líquido espessado apenas. Considerando a existência da padronização das consistências com base no IDDSI, uma iniciativa internacional de padronização de dietas45 desde 2015 e atualizado em 2019, apenas Souza et al.,38 Souza et al.39 e Gozzer et al.33 usaram a validação internacional. O IDDSI favorece o uso da mesma nomenclatura mundialmente, facilita a padronização e a validação de protocolos de avaliação como da VED para populações com transtornos neurológicos, por exemplo. Contudo, 13 dos 21 estudos foram publicados após 2015, ano de criação e publicação do IDDSI, e não usaram a padronização internacional, o que dificulta a validação de um protocolo.
Os volumes apresentados nos protocolos dos estudos foram amplamente variados, desde estudos que testaram todas as consistências em 3, 5 e 10mL, outros testaram apenas 10mL três vezes, outros identificaram volumes como tamanho da colher ofertada, a colher de chá foi a especificada, até estudos que não especificaram volumes nem número de ofertas ou mesmo utensílios usados.
Alguns dos utensílios usados por alguns estudos foram canudo, copo, porém sem especificar tamanho ou mesmo diâmetro de cada utensílio, o que dificulta a compreensão da quantidade ofertada ao participante do estudo. Logo, o uso de colheres, canudos ou copos sem especificar tamanho e quantidade não pode ser caracterizado como descrição de volumes, pois existem diferentes diâmetros e tamanhos de cada um desses utensílios. Adicionalmente, estudos que citaram o mesmo protocolo, na descrição do artigo usaram consistências e volumes diferentes, consequentemente não caracterizaram o mesmo protocolo.
Por fim, a presença de fonoaudiólogo para a oferta do alimento e orientar a deglutição dos pacientes durante a VED ao lado do médico que faz a endoscopia foi citada em 11 dos 21 estudos selecionados. A avaliação da deglutição e de suas possíveis alterações através da VED é de responsabilidade médica exclusiva no Brasil, a atuação do fonoaudiólogo é de acompanhar a avaliação e verificar as respostas do paciente frente às manobras corporais para a alimentação. O trabalho em equipe é padrão‐ouro para um diagnóstico preciso e determinação de plano terapêutico adequado àquele paciente.
Quanto à qualidade dos estudos mesmo em se considerando um ponto de corte alto, a maioria dos estudos obteve avaliação como bons ou satisfatórios, o que dificulta a consideração de qualquer um desses protocolos para padronização e ou validação para VED na população neurológica. Entretanto, três desses estudos foram os que detalharam melhor seus procedimentos e protocolo de avaliação de VED26,30,38 em que três estudos trouxeram todos os itens minuciosamente detalhados desde as consistências testadas, um deles usou o IDDSI, os volumes ofertados em unidade de “mL” ou “cc”, citou o uso do corante alimentício para favorecer contraste em relação às estruturas e secreções do organismo, alimentos e líquidos ofertados de acordo com cada consistência, quantas vezes cada uma foi ofertada e quais utensílios foram usados para oferta de cada uma das consistências. A forma de captura das imagens da VED não foi discutida nos artigos, por isso não foi ressaltada nesta revisão sistemática.
Contudo, nenhum desses protocolos foi validado para população neurológica. A não existência de protocolo validado dificulta a padronização da avaliação e altera a abordagem terapêutica amplamente, visto que toda a reabilitação é baseada em uma avaliação detalhada, precisa e confiável. O diagnóstico adequado e correto é a base para qualquer reabilitação e gerenciamento das disfagias em pacientes adultos com doença neurológica.
A importância da existência de protocolo padronizado e validado para populações neurológicas é evidente, inclusive para populações específicas, visto que cada doença neurológica tem suas particularidades e fisiopatologias diferentes, assim como a apresentação da disfagia. As características da disfagia variam amplamente de acordo com o diagnóstico neurológico, a literatura traz detalhadamente essas diferenças, quanto à disfagia em doença de Parkinson,46 disfagia na paralisia supranuclear progressiva (PSP),47 disfagia na esclerose lateral amiotrófica (ELA),48 assim como a disfagia no traumatismo cranioencefálico (TCE),49 entre outras.
Algumas das limitações enfrentadas nesta revisão sistemática foram o possível viés de avaliação da qualidade dos estudos pelo fato de uma das avaliadoras cegadas ser a mesma a fazer as médias dos itens e da pontuação final e o não uso do terceiro avaliador nesta fase do estudo. Além de existir possível viés de seleção dos estudos, pois delimitamos pesquisas mais recentes, dos últimos 11 anos, talvez tenhamos deixado de fora pesquisas historicamente importante para esse tema, embora citadas na introdução e discussão.
A falta de um protocolo padronizado e validado para a população adulta com doenças neurológicas limita significativamente uma avaliação detalhada, precisa e focada nas possíveis dificuldades deglutitórias enfrentadas por esses pacientes. O diagnóstico clínico da disfagia pode estar sendo subestimado ou superestimado de acordo com o protocolo usado e os desfechos avaliados. Esta revisão sistemática, primeira na área, ressalta a necessidade da validação de protocolos com foco em adultos com doenças neurológicas de base considerando as características das disfagias e sua fisiopatologia. O diagnóstico adequado, confiável e preciso é a base para o gerenciamento da deglutição dessas populações.
ConclusãoA reprodutibilidade fidedigna dos protocolos é viável apenas em três dos artigos, mesmo que apresentem protocolos diferentes, porém nenhum padronizado ou validado para a população adulta com transtornos neurológicos.
Conflitos de interesseOs autores declaram não haver conflitos de interesse.
O presente trabalho foi realizado com apoio da Coordenação de Aperfeiçoamento de Pessoal de Nível Superior ‐ Brasil (CAPES) ‐ Código de Financiamento 001.
Como citar este artigo: Prikladnicki A, Santana MG, Cardoso MC. Protocols and assessment procedures in fiberoptic endoscopic evaluation of swallowing: an updated systematic review. Braz J Otorhinolaryngol. 2022;88:445–70.
A revisão por pares é da responsabilidade da Associação Brasileira de Otorrinolaringologia e Cirurgia Cérvico‐Facial.