Acute otitis media is a disease with high global prevalence, that can lead to several acute complications and auditory sequelae. Data regarding the auditory evaluation in the acute phase of acute otitis media are scarce.
ObjectiveTo evaluate the main audiometric changes (air and bone conduction thresholds) in the initial phase of an acute otitis media episode.
MethodsA case‐control study was performed. Patients diagnosed with acute otitis media with less than 7 days of evolution in relation to the complaint onset were selected, and healthy volunteers were selected as controls. The acute otitis media and control groups were submitted to pure tone and vocal audiometry.
ResultsThe acute otitis media group included a total of 27 patients (30 ears). Hearing loss was present in 90.0% of the ears with acute otitis media, with conductive loss in 14 (46.67%) and mixed loss in 13 (43.33%). Both the air and bone conduction thresholds obtained with the tonal audiometry in the acute otitis media group were significantly worse than the controls at all tested frequencies (p <0.05). In patients with acute otitis media, we observed that the thresholds for frequency>1kHz (bone conduction) and 3kHz (air conduction) were significantly worse in patients with tinnitus compared to patients without tinnitus.
ConclusionDuring the first 7 days of evolution after the onset of an isolated episode of acute otitis media, we observed significant increases in bone and air thresholds at all frequencies, especially> 2kHz, compared to healthy ears.
A otite média aguda é uma doença de elevada incidência global, que pode levar a diversas complicações agudas e sequelas auditivas. Dados referentes à avaliação auditiva na fase aguda da otite média aguda são escassos.
ObjetivoAvaliar as principais alterações audiométricas (limiares em via aérea e óssea) na fase inicial de um episódio de otite média aguda.
MétodoRealizou-se estudo de caso‐controle. Selecionamos pacientes com diagnóstico de otite média aguda, com menos de sete dias de evolução em relação ao início das queixas, e voluntários saudáveis foram selecionados como controles. Os grupos otite média aguda e controle foram submetidos a audiometria tonal, vocal e audiometria.
ResultadosO grupo otite média aguda incluiu 27 pacientes (30 orelhas). Observou‐se presença de perda auditiva em 90% das orelhas com otite média aguda, condutiva em 14 (46,67%) e mista em 13 (43,33%). Tanto os limiares auditivos por via aérea quanto os limiares por via óssea obtidos com audiometria tonal do grupo otite média aguda eram significativamente piores em relação aos controles, em todas as frequências testadas (p <0,05). Em pacientes com otite média aguda, observamos que os limiares das frequências acima de 1 kHz (via óssea) e 3 kHz (via aérea) eram significantemente piores entre pacientes com zumbido em comparação a pacientes sem zumbido.
ConclusãoNos primeiros sete dias de evolução do quadro inicial de um episódio isolado de otite média aguda, observamos aumentos significativos dos limiares ósseos e aéreos em todas as frequências, principalmente nas acima de 2 kHz, em comparação a orelhas sadias.
A otite média aguda (OMA) é uma doença com altos índices globais de incidência (10,85%), acomete 709 milhões de pessoas/ano.1 A otite média também se associa a altos índices de complicações agudas graves e potencialmente fatais, que incluem complicações intratemporais (mastoidite aguda e apicite petrosa, por exemplo) e intracranianas (como trombose de seio sigmoide, abscesso intracraniano e meningite).2,3 Mesmo em casos não complicados, diversos estudos demonstraram que otite média se associa à série de sequelas permanentes, que incluem perda auditiva, zumbido e sintomas vestibulares.4–8 Em relação à perda auditiva, estima‐se que 30,82 a cada 10.000 pessoas com diferentes tipos de otite média apresentem sequelas auditivas (limiares auditivos acima de 25 dBNA) permanentes.1
A perda auditiva mais frequentemente observada durante episódios agudos de OMA é a condutiva. Porém, estudos recentes demonstraram também diversos graus de sequela auditiva neurossensorial, especialmente nas frequências agudas (2–8 kHz) e altas frequências em pacientes com história de OMA aguda e recorrente.4,9 Apesar de o impacto clínico da perda auditiva em altas frequências ter sido pouco estudado, ela já foi associada à deterioração de percepção de tons musicais, dificuldades na localização sonora e percepção de fala (especialmente em ambientes ruidosos) e zumbido.10–13 Adicionalmente, uma coorte de 30 anos também demonstrou que adultos com história de OMA recorrente na infância obtiveram piores limiares auditivos14 e apresentaram prevalência significativamente maior de zumbido13,15 em comparação a indivíduos sem história de OMA.
Considerando que as frequências agudas são as mais afetadas na OMA,5 a avaliação auditiva na fase aguda do processo infeccioso pode ser uma parte importante e precoce na identificação de possíveis lesões ao epitélio sensorial coclear e complicações agudas, como a labirintite serosa ou supurativa.4,16–18 Dessa maneira, torna‐se possível introduzir o tratamento adequado precocemente e elevar as chances de recuperação auditiva. Entretanto, dados referentes à avaliação das alterações auditivas na fase aguda da OMA são escassos. Portanto, o objetivo deste estudo é avaliar se, na fase aguda, a OMA leva a alterações de limiares auditivos (em via óssea e aérea) nas frequências de 500 Hz–4kHz em comparação a orelhas saudáveis.
MétodoFez‐se estudo clínico transversal de caso‐controle, de fevereiro a dezembro de 2018, com amostragem não probabilística de conveniência. Fez‐se também cálculo amostral, com base na disponibilidade de casos provenientes do nosso pronto‐socorro que preenchiam integralmente todos os critérios de exclusão definidos. Assumindo erro amostral de 15% e nível de confiança a 95%, o cálculo amostral resultou em 25 indivíduos.
Selecionaram‐se pacientes com diagnóstico de OMA, em um pronto‐socorro de um hospital universitário terciário. Neste estudo, casos de OMA foram definidos de acordo com os seguintes critérios diagnósticos: 1) Início agudo de sinais e sintomas clínicos; 2) Presença de efusão em orelha média, indicada pela presença de abaulamento da membrana timpânica, mobilidade limitada de membrana timpânica, nível líquido em orelha média e/ou otorreia; e 3) Sinais e sintomas de inflamação local, indicados pela presença de eritema característico de membrana timpânica ou otalgia.19
Este estudo foi aprovado pelo Comitê de Ética em Pesquisa de nossa instituição (número de protocolo 0364/2017) e também obedeceu aos princípios ditados pela Declaração de Helsinque para pesquisas em seres humanos.20
Definiram‐se como critérios de inclusão pacientes acima de 18 anos, com menos de sete dias decorridos entre o início dos sintomas e o diagnóstico. Excluíram‐se pacientes (1) com doença otológica prévia; (2) com perda auditiva identificada previamente ao quadro agudo de otite média; (3) portadores de comorbidades que pudessem levar a um quadro de perda auditiva neurossensorial, tais como doenças metabólicas, vasculares e autoimunes; (4) sindrômicos ou com malformações de orelha externa; (5) com presença de alterações cognitivas; (6) com histórico de traumatismo crânio‐encefálico; (7) com perfuração de membrana timpânica de causa não relacionada à otite média; (8) submetidos a cirurgia otológica prévia; (8) com histórico de exposição crônica ao ruído; e (9) com histórico de cânceres que afetassem o osso temporal ou submetidos à quimioterapia sistêmica ou radioterapia da região da cabeça e pescoço. Os pacientes selecionados foram submetidos à audiometria convencional tonal (250 Hz–8 kHz), vocal e imitanciometria, quando a MT se encontrava íntegra. Analisamos a via óssea nas frequências de 500 Hz–4kHz e a via aérea nas frequências de 250 Hz–8 kHz; de acordo com os resultados, definimos como “perda auditiva” quando os limiares eram maiores do que 25 dBNA em qualquer frequência testada. O valor da diferença entre os limiares obtidos pela via óssea e via aérea em cada frequência foi denominado como “gap aéreo‐ósseo”. Em casos que a diferença interaural foi maior ou igual a 40dB na via aérea ou óssea, usamos mascaramento na orelha não testada, pois a atenuação é praticamente nula. O mascaramento foi feito com a técnica de platô desenvolvida por Hood,21 levou‐se em conta sua eficácia nos casos em que é possível ocorrer supermascaramento. Para diminuir o risco de viés de aferição, todas as audiometrias foram feitas pela mesma fonoaudióloga, especialista em audiologia clínica, no mesmo equipamento.
Analisou‐se a audiometria vocal em dois parâmetros: 1) Limiar de Reconhecimento de Fala (LRF); e 2) Índice Percentual de Reconhecimento de Fala (IPRF).22 A classificação da imitânciometria se baseou nos critérios propostos por Jerger de acordo com a pressão em orelha média em tipos A (pico em +200 a ‐99 daPa), C (pico em ‐100 a ‐400 daPa) ou B (curva plana).23
Para comparação dos resultados obtidos com o grupo de estudo (OMA), selecionaram‐se indivíduos saudáveis, sem história pregressa de otite média, como controles. Os controles foram selecionados com os mesmos critérios de inclusão e exclusão aplicados ao grupo OMA e foram submetidos à mesma rotina de avaliação audiométrica.
Para comparar os limiares ósseos e aéreos dos pacientes de OMA com os indivíduos do grupo controle, usamos o teste não paramétrico de Mann‐Whitney. Fez‐se o teste de Spearman para correlacionar as variáveis idade e limiares auditivos ósseos. Os resultados dos testes estatísticos foram considerados significantes quando o valor de p ˂ 0,05.
ResultadosDemografia, anamnese e exame físicoO grupo final de pacientes com OMA foi constituído por 27 pacientes. Desses, 15 eram do sexo masculino (55,5%) e 12 do feminino (44,5%), com média de 36,13 anos (mediana=37,5 anos; variação=18–67 anos; desvio‐padrão [DP]=11,77 anos). Foram avaliadas 30 orelhas com OMA, já que três pacientes (11,1%) apresentaram OMA em ambas as orelhas. O grupo controle compreendeu 16 indivíduos (32 orelhas). No grupo controle, a idade média dos indivíduos era de 35,12 anos (mediana=35 anos; variação=18–62 anos; DP=12,19 anos), oito eram do sexo masculino (50%) e oito do feminino (50%). Não encontramos diferenças significativas entre a idade média e distribuição quanto ao sexo entre os grupos OMA e Controle (p> 0,05).
O tempo médio de evolução entre o início das queixas de OMA e a avaliação clínica foi de 4,7 dias. Em relação aos sintomas clínicos 100% dos pacientes apresentaram otalgia; 81,5% hipoacusia; 81,5% zumbido; e 74,1% plenitude aural. Todos os pacientes analisados apresentavam no mínimo dois dos sintomas clínicos mencionados acima. A otoscopia de todos os pacientes com OMA revelou presença de hiperemia e em quatro pacientes com OMA observamos presença de perfuração de membrana timpânica. Nenhum indivíduo do grupo controle apresentava queixas auditivas ou alterações à otoscopia.
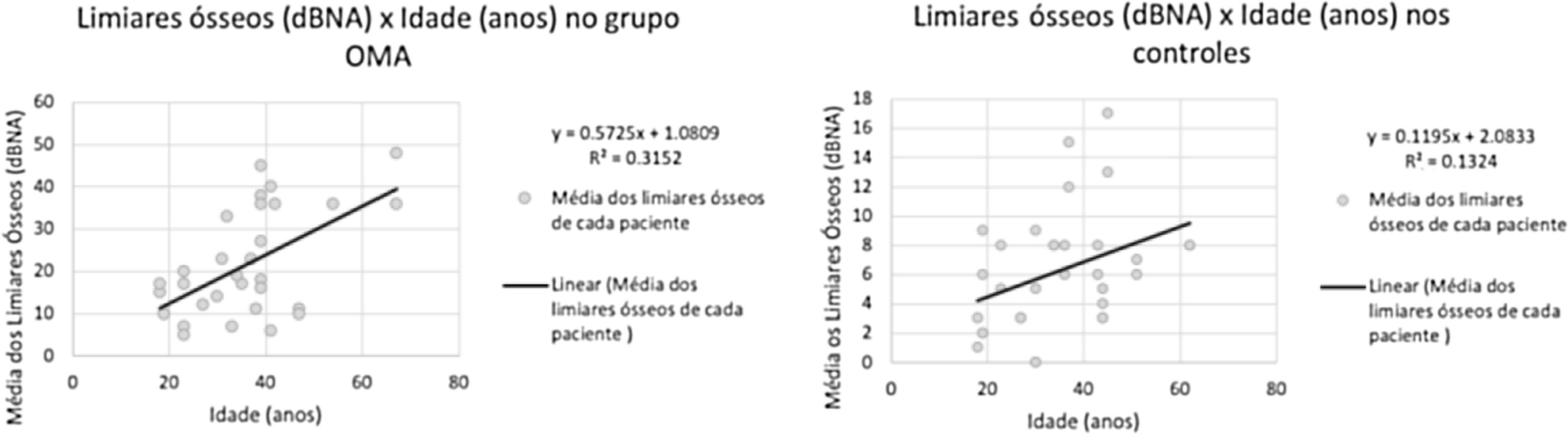
Resultados audiométricosInicialmente, avaliamos os limiares ósseos e aéreos da orelha contralateral em pacientes com OMA unilateral em comparação com as audiometrias do grupo controle. Tal comparação não evidenciou diferenças significativas entre nenhuma das frequências (p> 0,05). Das 30 orelhas com OMA, observou‐se que em 27 (90%) havia presença de perda auditiva identificada em audiometria, sendo esta perda condutiva em 14 (46,67%) e mista em 13 (43,33%). Nos três pacientes com audiometria dentro da normalidade, fizemos análise comparativa com a orelha contralateral, que demonstrou limiares ósseos inferiores no lado doente em relação ao contralateral, sem gap aéreo‐ósseo (OMA, limiar médio=15,0 dBNA; orelha contralateral, limiar médio=5,33 dBNA; p> 0,05). No grupo controle, todos os indivíduos apresentavam resultados audiométricos dentro dos valores de normalidade (˂ 25 dBNA). Observamos, tanto no grupo controle quanto no grupo OMA, correlação positiva entre idade e aumento dos limiares ósseos (coeficiente R=0,509 e 0,457 respectivamente) (fig. 1). No grupo controle, os limiares testados por via óssea foram exatamente iguais aos obtidos por via aérea em todas as frequências.
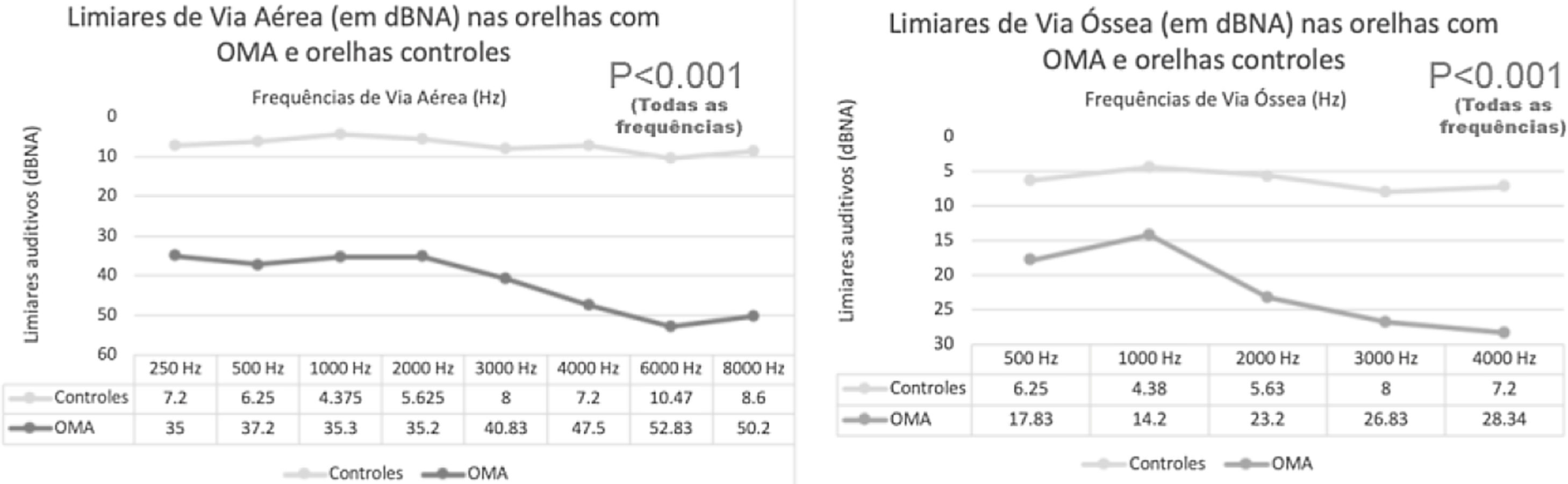
Análise comparativa entre os resultados audiométricos obtidos pelo teste por via aérea evidenciou que entre pacientes com OMA os limiares auditivos eram significativamente piores em comparação aos do grupo controle (p <0,001) (fig. 2). Para diminuir a influência de alterações na condução sonora nos pacientes com OMA, também analisamos comparativamente os resultados obtidos com o teste por via óssea nos pacientes com OMA com os limiares ósseos dos controles. Essa análise também revelou que os limiares ósseos dos pacientes com OMA também foram significantemente piores em relação aos controles, em todas as frequências (p <0,001) (fig. 2).
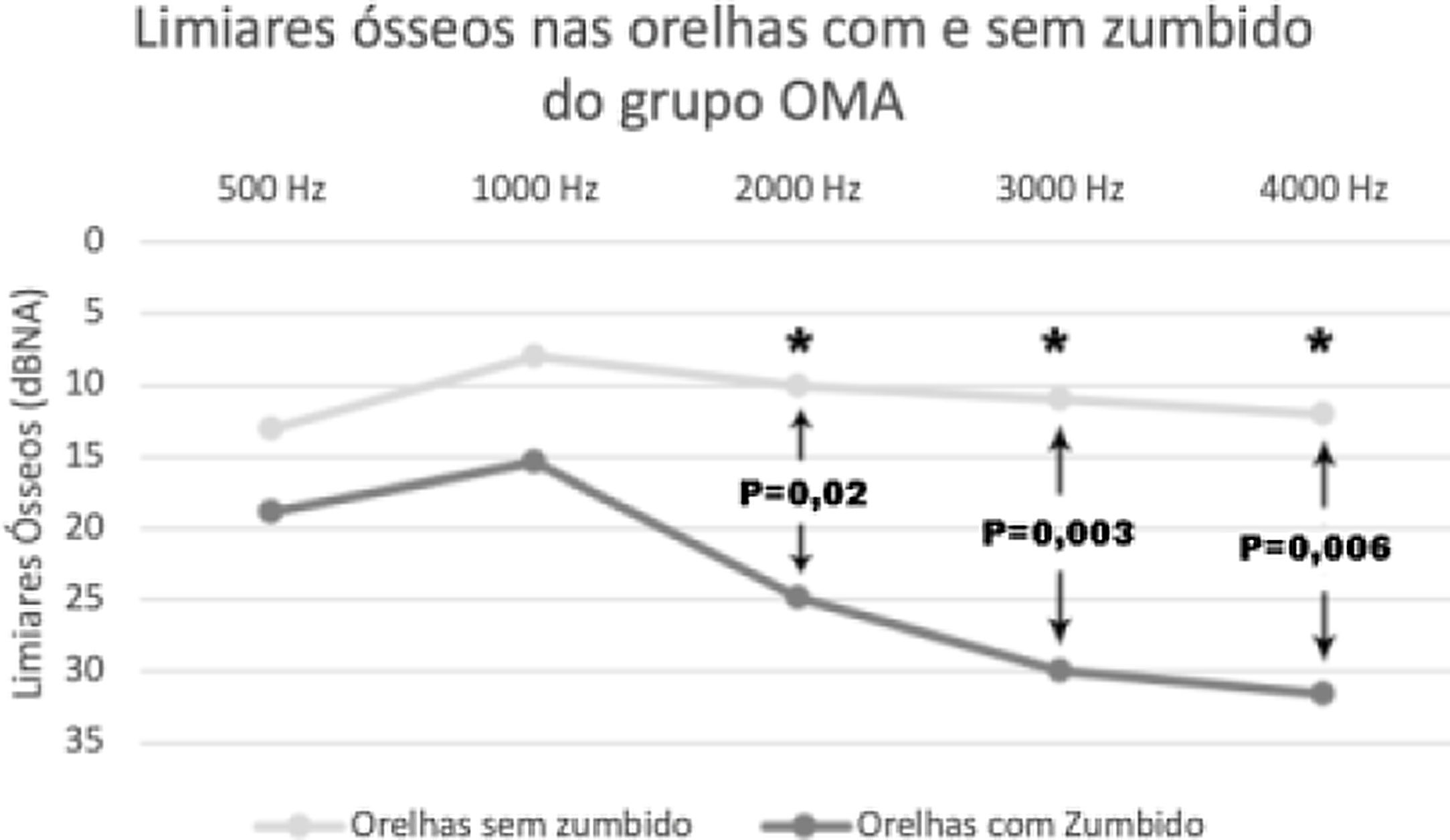
Fizemos também, entre pacientes com OMA, avaliação comparativa entre os limiares ósseos e aéreos de pacientes com e sem zumbido. Encontramos limiares aéreos médios de 44 dBNA nas orelhas com zumbido vs. 25,75 dBNA nas orelhas sem zumbido (tabela 1). Os limiares ósseos médios das orelhas com zumbido foram de 23,96 dBNA vs. 10,8 dBNA das orelhas sem zumbido (fig. 3). A diferença entre os limiares das orelhas com zumbido e sem zumbido foi significante nas frequências a partir de 2kHz para a via óssea e a partir de 4kHz para a via aérea (tabela 1)
Valores de p demonstram ou não significância entre os limiares de Via Aérea (VA) e de Via Óssea (VO), ao comparar as orelhas com e sem zumbido do grupo OMA
| 250 Hz | 500 Hz | 1 kHz | 2 kHz | 3 kHz | 4 kHz | 6 kHz | 8 kHz | |
| VO | p=0,482 | p=0,194 | p=0,02a | p=0,003a | p=0,006a | |||
| VA | p=0,07 | p=0,087 | p=0,109 | p=0,082 | p=0,082 | p=0,005a | p=0,01a | p=0,03a |
* Valor de p considerado estatisticamente significativo (< 0.05).
Com relação à audiometria vocal, observamos piores valores de LRF (Limiar de Reconhecimento de Fala) nas orelhas com OMA (p <0,001) (LRF médio de 38,5 dBNA nas orelhas com OMA; LRF médio de 7,65 dBNA nas orelhas controles). Observamos diferença estatisticamente significante ao comparar os valores de IPRF (Índice Percentual de Reconhecimento de Fala) das orelhas do grupo OMA com as orelhas do grupo controle (p=0,004). Contudo, somente duas orelhas (6,67%) desse grupo obtiveram valores de IPRF abaixo de 92%. No grupo controle, 97% das orelhas apresentaram IPRF de 100% e apenas uma orelha desse grupo (3,1%) apresentou IPRF de 96%. Entre os pacientes com OMA, observamos piores valores de LRF nas orelhas com zumbido (LRF médio=40,56 dBNA) em comparação às orelhas sem zumbido (LRF médio=27,5 dBNA), porém essa diferença não foi estatisticamente significante (p=0,104) (fig. 4). Também não observamos diferenças significativas entre o IPRF das orelhas com e sem zumbido do Grupo OMA (p=0,313).
Em relação à imitanciometria, 20 de 30 orelhas com OMA (66,67%) apresentaram curva tipo B e cinco (16,67%) apresentaram curva tipo C. Uma orelha apresentou curva tipo A e em quatro orelhas não foi possível fazer a imitânciometria, pois se observou a presença de perfuração timpânica.
DiscussãoApesar de a OMA se tratar de doença com elevada incidência e prevalência e que pode cursar com sequelas auditivas permanentes, a hipoacusia e queixas auditivas resultantes costumam ser subvalorizadas.24 Porém, estudos prévios demonstraram que a OMAs pode cursar com rebaixamento de limiares auditivos, principalmente nas altas frequências (8–16kHz).4,9,25 Entretanto, a avaliação audiométrica em pacientes com OMA não complicada não é feita rotineiramente, é reservada para casos mais severos e complicados, fato que contribui sobremaneira para o subdiagnóstico dessas sequelas.26
Entre as 30 orelhas com OMA estudadas, observou‐se presença de alterações de limiares auditivos em 90%. Apesar da observação de que déficits condutivos foram ligeiramente predominantes (46,67%), a presença de perda auditiva mista atingiu 43,33% da amostra, sugerindo que a presença de componente neurossensorial na perda auditiva pode ocorrer em porção considerável dos pacientes com OMA. A prevalência encontrada neste estudo foi superior à previamente reportada na literatura, que variou entre 2,4%9 e 10,6%.4 Uma possível explicação para tais diferenças reside no fato de nosso hospital ser terciário, atende mais comumente pacientes encaminhados por outras instituições em casos de doenças mais severas ou de apresentação atípica.
A literatura mostra possíveis explicações fisiopatológicas para a presença de cada tipo de perda auditiva secundária à OMA: os déficits condutivos na fase aguda são principalmente ocasionados pela presença de fluido em orelha média9 e o componente neurossensorial provavelmente ocorre por inflamação intracoclear, gerada pela passagem de toxinas e agentes inflamatórios da orelha média para a orelha interna através da membrana da janela redonda.27–29 Esse mecanismo foi comprovado em estudos em cobaias, que demonstraram que a membrana da janela redonda é semipermeável a diversos mediadores inflamatórios.27–29 Esses mediadores se concentram, principalmente, na região inicial do giro basal da cóclea, que corresponde tonotopicamente às frequências agudas.30–32 Clinicamente, estudos translacionais também correlacionaram positivamente a região nas quais as principais alterações patológicas foram encontradas (giro basal da cóclea) às frequências auditivas mais frequentemente atingidas pela OMA (altas frequências).28 Outro possível fenômeno que pode levar à perda auditiva na fase inicial da OMA é a presença de hidropsia endolinfática transitória, causada por variações pressóricas na orelha média, por alterações na mobilidade da membrana da janela redonda ou pelo processo inflamatório intracoclear. Esse fenômeno já foi demonstrado em estudos clínicos e também em ossos temporais – nesse sentido, Paparella et al. observaram que mais de 60% de 194 ossos temporais com otite média tinham algum sinal característico de hidropsia.33
Para minimizar o impacto das alterações de condução sonora na análise dos limiares auditivos, analisamos comparativamente os resultados obtidos por via óssea nos pacientes com OMA com os limiares ósseos dos controles. Em nossa amostra, observamos piores limiares ósseos em todas as frequências (500 Hz–4 kHz) nas orelhas com OMA; tal diferença foi mais acentuada nas frequências de 3kHz e 4kHz. Nesse sentido, este estudo parece ser o primeiro a fazer esse tipo de análise durante a fase aguda de OMA em um grupo de pacientes. O relato de caso publicado por Margolis e Nelson34 corroboram nossos achados: neste estudo, os autores observaram que o componente neurossensorial precedeu o surgimento das alterações de condução e foi resultado, provavelmente, do processo inflamatório local que se estendeu ao giro basal da cóclea – isso ocorreria antes mesmo do acúmulo significativo de fluido em orelha média.25,34 Em nosso estudo, observamos, em algumas orelhas, fenômeno semelhante: em três orelhas com OMA sem gap aéreo‐ósseo e limiares menores de 25 dBNA, os limiares auditivos em todas as frequências testadas estavam piores em comparação com a orelha contralateral, o que sugere possível lesão funcional aguda. Adicionalmente, os autores também observaram que as frequências acometidas foram principalmente acima de 2kHz,34 outro achado também observado em nosso estudo.
Observamos que uma parcela significativa (81,5%) dos pacientes com OMA se queixou de zumbido. Nesses pacientes com zumbido, os limiares auditivos por via óssea foram significativamente piores nas frequências acima de 1kHz em comparação aos pacientes com OMA sem zumbido. Apesar de a correlação de zumbido com perda auditiva em altas frequências já ter sido estabelecida,35 poucos estudos correlacionam o zumbido como possível sequela da OMA.9 Cordeiro et al.9 demonstraram que a presença de zumbido após seis meses do episódio agudo de OMA apresentou associação positiva com a presença de piores limiares em comparação a pacientes sem zumbido. Uma possível explicação desses achados, do ponto de vista fisiopatológico, se dá pela associação entre otite média e lesões no epitélio sensorial da cóclea, inclusive diminuição significativa da população de células ciliadas internas e externas.6,36 Nesse sentido, há evidência preliminar na literatura que correlaciona essas lesões sensoriais (principalmente disfunção de células ciliadas internas e sinaptopatia na conexão neural com células ciliadas internas)35,37 com a presença de zumbido. Portanto, é plausível afirmar que graus mais severos de lesão em orelha interna secundários à OMA se correlacionem também à maior ocorrência de zumbido.35
Este estudo tem algumas limitações que devem ser destacadas. Por se tratar de um estudo transversal, não pudemos analisar se o aumento dos limiares ósseos era temporário ou permanente, assim como não pudemos acompanhar as evoluções das queixas dos pacientes ou dos achados otoscópicos. O número total de pacientes incluídos neste estudo, apesar de cumprir os requisitos definidos no cálculo amostral, foi reduzido. Esse fato provavelmente advém dos critérios rígidos e restritivos de exclusão aplicados, que – apesar de impactar negativamente no número de possíveis casos – foram necessários para avaliar de forma fidedigna o impacto da fase inicial da OMA nos resultados audiométricos. Outra limitação deste estudo é que, embora os resultados obtidos pelo teste audiométrico pela via óssea minimizassem o impacto da perda auditiva condutiva nos limiares reais, eles não representam, necessariamente, a função coclear.38 Apesar dessas limitações, nossos resultados têm relevância clínica direta. A frequência elevada de pacientes com perda auditiva mista sugere que, mesmo em pacientes com OMA não complicada, há alteração importante da função coclear durante a fase aguda. Nesse mesmo sentido, mesmo em orelhas que não apresentaram rebaixamento da via óssea abaixo de 25 dBNA (sugeriu perda auditiva puramente condutiva), os limiares de via óssea foram piores do que os encontrados nas orelhas saudáveis. Espera‐se que este estudo incentive estudos prospectivos subsequentes, dedicados a avaliar o impacto clínico e audiométrico tardio relacionados a essas alterações observadas na fase aguda da OMA.
ConclusãoNos primeiros sete dias de evolução do quadro inicial de um episódio isolado de OMA, observamos aumentos significativos dos limiares ósseos em todas as frequências (principalmente acima de 2 kHz) em comparação à via aérea em orelhas sadias.
FinanciamentoRCM e ALPK receberam bolsa de estudo da Coordenação de Aperfeiçoamento Pessoal de Nível Superior (Capes) (Código de financiamento: 001.)
Conflitos de interesseOs autores declaram não haver conflitos de interesse.
Como citar este artigo: Kasemodel AL, Costa LE, Monsanto RC, Tomaz A, Penido NO. Sensorineural hearing loss in the acute phase of a single episode of acute otitis media. Braz J Otorhinolaryngol. 2020;86:767–73.
A revisão por pares é da responsabilidade da Associação Brasileira de Otorrinolaringologia e Cirurgia Cérvico‐Facial.