People with vestibular loss present a deficit in the vestibular system, which is primarily responsible for promoting postural control, gaze stabilization, and spatial orientation while the head moves. There is no effective treatment for a bilateral loss of vestibular function. Recently, a vestibular implant was developed for people with bilateral loss of vestibular function to improve this function and, consequently, the quality of life of these patients.
ObjectiveTo identify in the scientific literature evidence that vestibular implants in people with vestibular deficit improves vestibular function.
MethodsOne hundred and forty six articles were found from five databases and 323 articles from the gray literature mentioning the relationship between vestibular implant and vestibular function in humans. The PICOS strategy (Population, Intervention, Comparison and Outcome) was used to define the eligibility criteria. The studies that met the inclusion criteria for this second step were included in a qualitative synthesis, and each type of study was analyzed according to the bias risk assessment of the Joanna Briggs Institute through the critical assessment checklist Joanna Briggs institute for quasi‐experimental studies and the Joanna Briggs institute critical assessment checklist for case reports.
ResultsOf the 21 articles included in reading the full text, 10 studies were selected for the qualitative analysis in the present systematic review. All ten articles analyzed through the critical assessment checklist Joanna Briggs institute showed a low risk of bias. The total number of samples in the evaluated articles was 18 patients with vestibular implants.
ConclusionsTaken together, these findings support the feasibility of vestibular implant for restoration of the vestibulo‐ocular reflex in a broad frequency range and illustrate new challenges for the development of this technology.
Pessoas com perda vestibular apresentam um déficit no sistema vestibular, o qual é o principal responsável pelo controle postural, pela estabilização do olhar e orientação espacial enquanto a cabeça se movimenta. Não há tratamento efetivo para uma perda vestibular bilateral. Recentemente, foi desenvolvido um implante vestibular para pessoas com perda vestibular bilateral para melhorar essa função e, consequentemente, a qualidade de vida desses pacientes.
ObjetivoIdentificar na literatura científica evidências de que o implante vestibular melhora a função vestibular de pessoas com déficit vestibular.
MétodoCento e quarenta e seis artigos foram encontrados em cinco bases de dados e 323 arti-gos da literatura cinzenta, mencionando a relação entre implante vestibular e função vestibular em humanos. A estratégia PICOS (População, Intervenção, Comparação e Desfechos) foi uti-lizada para definir os critérios de elegibilidade. Os estudos que preencheram os critérios de inclusão para esta segunda etapa foram incluídos em uma síntese qualitativa, e cada tipo de estudo foi analisado de acordo com a avaliação de risco de viés do Joanna Briggs Institute através da critical appraisal checklist for quasi-experimental studies e da critical appraisa lchecklist for case reports.
ResultadosDos 21 artigos incluídos cujos textos completos foram lidos, 10 foram selecionados para a análise qualitativa na presente revisão sistemática. Todos os dez artigos analisados ??através da critical appraisal checklist mostraram um baixo risco de viés. O número total de amostras nos artigos avaliados foi de 18 pacientes com implantes vestibulares.
ConclusõesEm conjunto, esses achados apoiam a viabilidade do implante vestibular para a restauração do reflexo vestíbulo‐ocular em uma ampla faixa de frequências e ilustram novos desafios para o desenvolvimento desta tecnologia.
Todos os dias somos confrontados com uma variedade de situações dinâmicas em que informações precisas sobre movimentos da cabeça e do corpo e posições espaciais da cabeça e do corpo são necessárias para garantir o funcionamento adequado do sistema vestibular e, consequentemente, garantir a segurança e o bem‐estar do paciente.1 O sistema vestibular é um dos principais sistemas responsáveis por garantir o controle postural, a estabilização do olhar e a orientação espacial, contribui para a manutenção do equilíbrio.2
Esse sistema consiste em um conjunto de órgãos sensoriais localizados na orelha interna, composto de três canais semicirculares e dois órgãos otolíticos (sáculo e utrículo), responsáveis por fornecer ao córtex informações simultâneas sobre a posição da cabeça em relação ao corpo e produzir o reflexo vestíbulo‐ocular (RVO), que tem a função de gerar movimentos oculares compensatórios em relação à direção da cabeça para manter um campo de visão estável na retina.1
Se o sistema for danificado por uma doença, envelhecimento ou lesão, a pessoa apresentará uma perda da função vestibular. Como resultado, terá um RVO ineficiente ou ausente e, consequentemente, uma redução da acuidade visual durante o movimento.3,4 Esses déficits vestibulares podem causar sintomas como oscilopsia, desequilíbrio, vertigem, desorientação espacial e alterações cognitivas, entre outros,5 comprometem a capacidade do paciente de fazer atividades diárias básicas, como caminhar.6
Apesar dos avanços científicos, as opções terapêuticas existentes são limitadas e de baixa eficácia em certos casos.7 Estudos mostram que, apesar do treinamento intensivo de equilíbrio, alguns pacientes não apresentam melhoria significativa, mantêm sintomas incapacitantes com interferência nas atividades diárias e laborais.1,3,6,8 Nesse contexto, alguns grupos de pesquisa sugerem um implante vestibular (IV) para substituir a função dos órgãos vestibulares.8–11
Implantes vestibularesAtualmente, o uso de IV em humanos tem sido estudado por grupos de pesquisa na Europa (Geneva University Hospitals e Maastricht University Medical Center) e nos Estados Unidos (University of Washington) como opção terapêutica para pessoas com perda vestibular definitiva sem melhoria com tratamento clínico.12,13 Estudos em animais 10,11,14,15 e humanos 8,10,12 mostraram que a estimulação elétrica é um meio potencialmente eficaz de ativar o sistema vestibular.
O IV consiste em uma modificação do implante coclear (IC), contém de um a três eletrodos “vestibulares” retirados do conjunto de eletrodos cocleares, cada um construído com um arranjo de eletrodos finos de 2,5mm com um diâmetro de 150μm, implantados no espaço perilinfático adjacente ao labirinto membranoso de cada canal semicircular.13 Assim, em vez de detectar informações de som como o IC, ele captura as informações sobre o movimento, usa sensores fixados na cabeça, que alimentam um processador especial, onde são convertidas para um padrão neural apropriado.2 Em seguida, esses padrões neurais de informações de movimento processado são transmitidos na forma de correntes elétricas distribuídas através dos eletrodos vestibulares, para o estimulador implantado, o qual transfere a informação para o sistema nervoso central (SNC).2,8 Nesse conceito, o IV tem como objetivo transmitir padrões neurais “artificiais” para o SNC, semelhantes àqueles codificados pelo sistema vestibular com função normal.2
Até o momento, duas estratégias cirúrgicas foram descritas para o IV: a abordagem cirúrgica intralabiríntica1,8,12,16 e a abordagem extralabiríntica.15,17,18 Com a abordagem intralabiríntica, cada canal semicircular é aberto e os eletrodos são inseridos até que entrem em contato com as células ciliadas da ampola.12 Com uma abordagem extralabiríntica, o labirinto não é aberto e os eletrodos são colocados diretamente sobre os nervos.13
A evolução do conhecimento sobre um tema específico em medicina requer revisões sistemáticas (RS) para encontrar, reconhecer e sintetizar as evidências científicas que apoiem as propostas de boas práticas clínicas em saúde.19 O objetivo desta RS é identificar evidências na literatura científica de que o IV em pessoas com déficit vestibular melhora a função vestibular.
MétodoNeste estudo, foi feita uma RS por ser uma metodologia reconhecida para pesquisa científica de alto nível na área da saúde. O primeiro passo para iniciar uma RS é formular uma questão de pesquisa específica que contenha a população‐alvo, a intervenção ou exposição, uma comparação (se aplicável), os desfechos esperados e os tipos de estudo que podem responder à pergunta (Picos).19 Nesta RS, a seguinte questão foi colocada: pessoas com perda vestibular que usam IV apresentam melhoria na função vestibular?
Estratégia de buscaA estratégia de busca feita nesta RS seguiu os critérios recomendados pelo método Preferred Reporting Items for Systematic Reviews and Meta‐Analyses (Prisma)19 e para os quais o protocolo foi registrado em 6 de junho de 2018 no banco de dados International Prospective Register of Systematic Reviews (Prospero)20 sob número de registo CRD42018093469.
A busca foi feita nas bases de dados PubMed, Scopus, Lilacs, Livivo e Speech Bite. A literatura cinzenta foi consultada através do banco de dados do Google Scholar. Não houve restrição quanto ao período ou idioma da publicação.
As palavras‐chave da estratégia de busca são descritas a seguir: vestibular loss OR vestibular deficit OR vestibulopathy OR vestibular dysfunction OR vestibular deficiency AND vestibular implant OR vestibular prosthesis OR neural prosthesis AND vestibular function. Essa estratégia de busca foi adaptada às demais bases de dados, os termos correspondentes foram aplicados em português e espanhol na Lilacs. Em seguida, foi feita uma busca manual das referências dos artigos selecionados.
Após a busca, as referências de cada banco de dados foram exportadas para o programa EndNote X8 (https://endnote.com/) e, em seguida, essas mesmas referências foram exportadas do EndNote X8 para o programa Rayyan QCRI (https://rayyan.qcri.org/). O objetivo desses dois programas foi registrar todos os artigos duplicados encontrados na literatura científica, promover maior confiabilidade na seleção de artigos e prosseguir para a etapa de elegibilidade.
Critérios de elegibilidadeA estratégia Picos (Paciente, Intervenção, Comparação, Desfechos) foi usada para definir os critérios de elegibilidade.19 Como critérios de inclusão foram selecionados os indivíduos com perda vestibular que usaram o IV, considerou‐se como intervenção a prótese vestibular e como comparação o período antes e após a cirurgia de IV em cada indivíduo. Os resultados precisavam conter uma avaliação da função vestibular e os estudos deveriam ser dos tipos clínicos prospectivos, casos clínicos e relatos de casos. Os critérios de exclusão foram pacientes que não eram candidatos a implante vestibular, estudos em animais e in vitro e estudos sem dados pós‐operatórios.
Todos os estudos foram analisados para elegibilidade nas fases de triagem com base nos critérios de inclusão e exclusão. Na primeira fase, todos os estudos foram selecionados com base no título e resumo por dois revisores de forma independente. Não houve discordância entre os revisores, descartou‐se a necessidade de consultar um terceiro revisor. No caso de falta do resumo, mas com um título aplicável, o estudo foi incluído na segunda fase.
Na segunda fase, os mesmos dois revisores leram o texto completo de cada artigo selecionado, usaram os mesmos critérios de inclusão e exclusão, mas acrescentaram a justificativa da exclusão para cada estudo descartado. Os estudos que preencheram os critérios de inclusão nessa segunda etapa foram incluídos em uma síntese qualitativa e cada tipo de estudo foi analisado de acordo com a avaliação de risco de viés do Joanna Briggs Institute (JBI),21 através do JBI critical appraisal checklist para estudos quase‐experimentais e o JBI critical appraisal checklist para relatos de caso.
No JBI critical appraisal checklist, cada pergunta deve ser respondida através de quatro opções: yes (Y), no (N), unclear (U) e not applicable (NA) [isto é, sim (S), não (N), incerto (I) e não aplicável (NA)]. O cálculo da porcentagem de risco de viés é feito pela quantidade de “Y” que foi selecionada na checklist. Quando a resposta “NA” foi selecionada, a questão não foi considerada no cálculo, de acordo com as diretrizes do Joanna Briggs Institute.21 Até 49% considera‐se um risco alto de viés. De 50% a 70% o risco é moderado e acima de 70% o risco de viés é baixo.
Após essas avaliações, os estudos selecionados foram submetidos a uma análise estatística para verificar a possibilidade de se construir uma metanálise. Essa análise combina e resume os resultados de vários estudos, aumenta assim a precisão e o poder da evidência dos resultados.
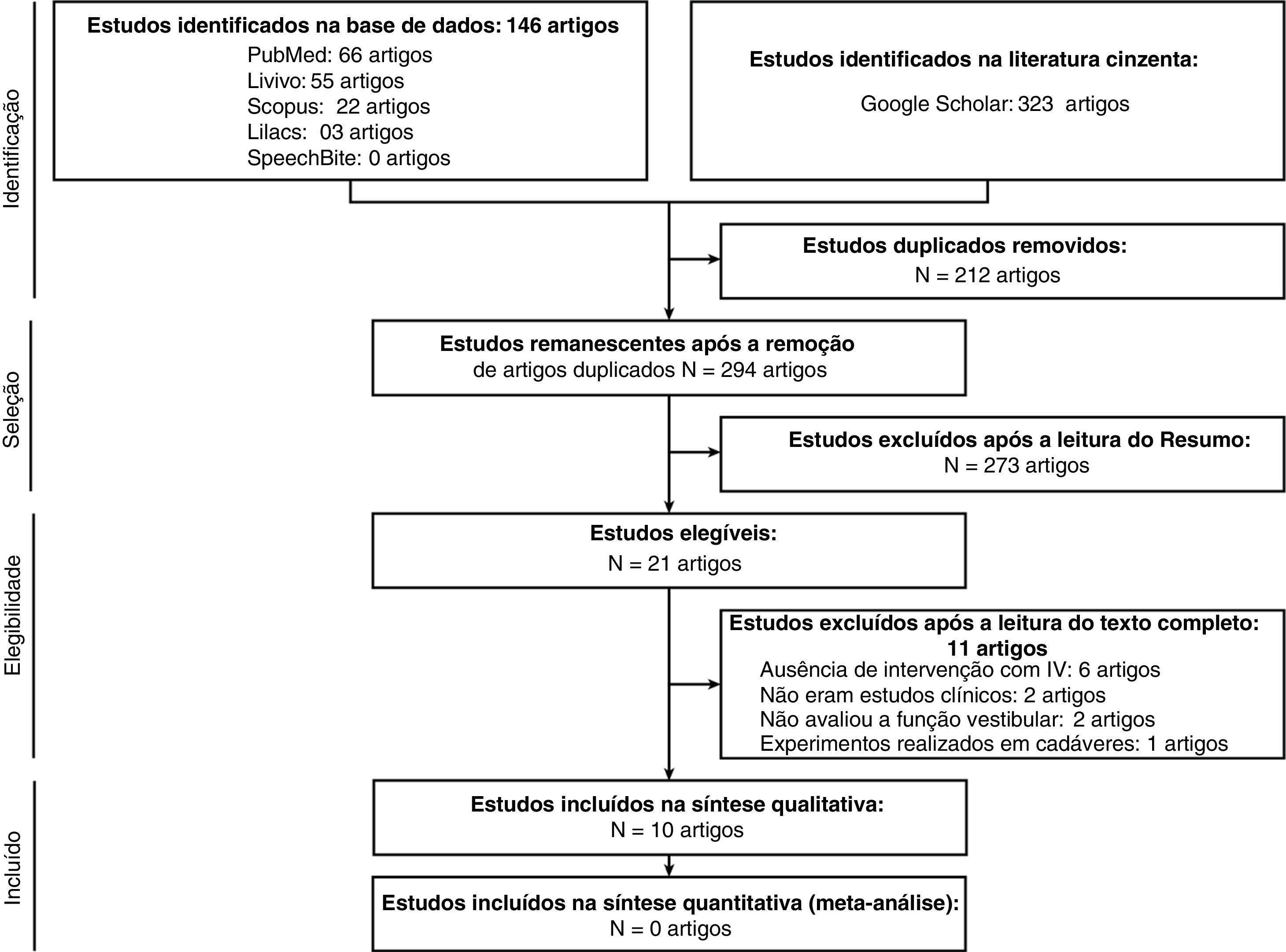
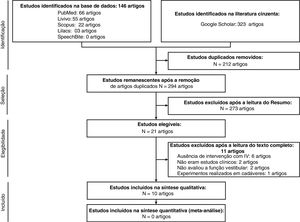
ResultadosNa primeira fase desta RS, 146 artigos foram encontrados em cinco bases de dados e 323 artigos na literatura cinzenta. Após a eliminação de 212 estudos duplicados, foram selecionados 294 para leitura de títulos e resumos. Desses, 273 foram excluídos de acordo com os critérios de exclusão estabelecidos. Dos 21 artigos incluídos na segunda etapa, a qual consistiu em ler o texto completo de cada estudo, 11 foram excluídos pelos seguintes motivos: em seis artigos12,18,22–25 não houve intervenção com IV; dois2,26 artigos não eram estudos clínicos; dois artigos27,28 não avaliaram a função vestibular e em um29 estudo o experimento foi feito em cadáveres. No fim, 10 estudos foram selecionados para a análise qualitativa nesta RS (tabela 1). Não foram encontrados estudos ao se fazer uma busca manual das referências dos artigos. Todo o processo de seleção de artigos é descrito na figura 1, que mostra o diagrama de fluxo Prisma para inclusão.
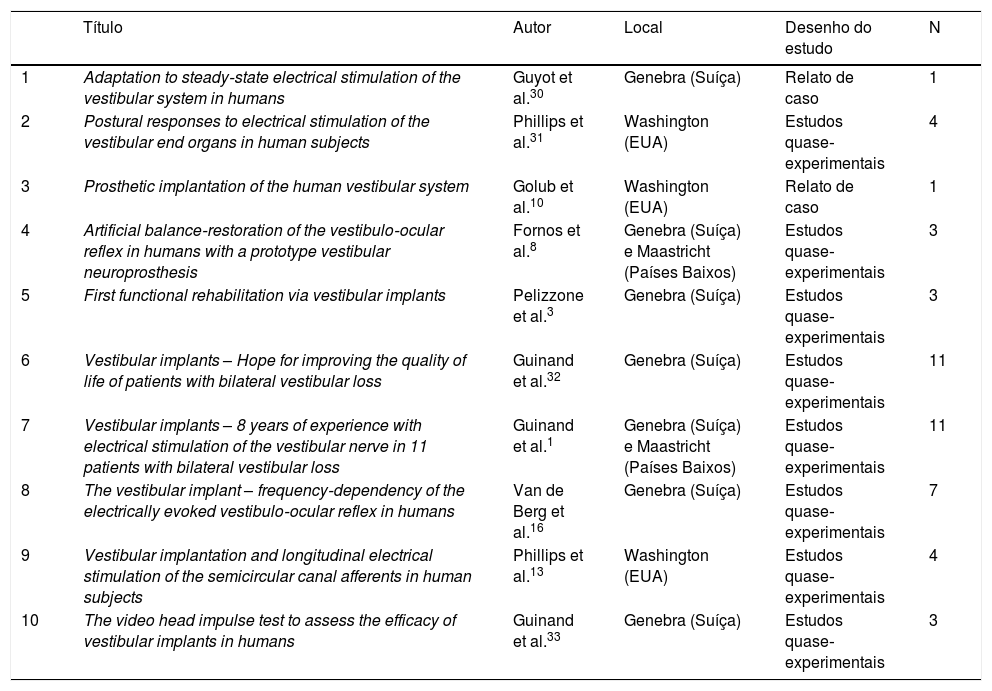
Estudos selecionados de acordo com os critérios de inclusão e exclusão estabelecidos na revisão sistemática
| Título | Autor | Local | Desenho do estudo | N | |
|---|---|---|---|---|---|
| 1 | Adaptation to steady‐state electrical stimulation of the vestibular system in humans | Guyot et al.30 | Genebra (Suíça) | Relato de caso | 1 |
| 2 | Postural responses to electrical stimulation of the vestibular end organs in human subjects | Phillips et al.31 | Washington (EUA) | Estudos quase‐experimentais | 4 |
| 3 | Prosthetic implantation of the human vestibular system | Golub et al.10 | Washington (EUA) | Relato de caso | 1 |
| 4 | Artificial balance‐restoration of the vestibulo‐ocular reflex in humans with a prototype vestibular neuroprosthesis | Fornos et al.8 | Genebra (Suíça) e Maastricht (Países Baixos) | Estudos quase‐experimentais | 3 |
| 5 | First functional rehabilitation via vestibular implants | Pelizzone et al.3 | Genebra (Suíça) | Estudos quase‐experimentais | 3 |
| 6 | Vestibular implants – Hope for improving the quality of life of patients with bilateral vestibular loss | Guinand et al.32 | Genebra (Suíça) | Estudos quase‐experimentais | 11 |
| 7 | Vestibular implants – 8 years of experience with electrical stimulation of the vestibular nerve in 11 patients with bilateral vestibular loss | Guinand et al.1 | Genebra (Suíça) e Maastricht (Países Baixos) | Estudos quase‐experimentais | 11 |
| 8 | The vestibular implant – frequency‐dependency of the electrically evoked vestibulo‐ocular reflex in humans | Van de Berg et al.16 | Genebra (Suíça) | Estudos quase‐experimentais | 7 |
| 9 | Vestibular implantation and longitudinal electrical stimulation of the semicircular canal afferents in human subjects | Phillips et al.13 | Washington (EUA) | Estudos quase‐experimentais | 4 |
| 10 | The video head impulse test to assess the efficacy of vestibular implants in humans | Guinand et al.33 | Genebra (Suíça) | Estudos quase‐experimentais | 3 |
Em relação às características gerais dos artigos incluídos, o primeiro publicado a fazer um IV em um paciente humano era de 2011,30 sete artigos1,3,8,16,30,32,33 foram de autoria do grupo de Genebra‐Maastricht e três10,13,31 foram de autoria do grupo de Washington. No geral, esses dois grupos fizeram a cirurgia de IV em 18 pessoas, de 34 a 76 anos (tabela 2). O grupo de Genebra‐Maastricht fez seu primeiro implante vestibular em 2007 em um homem de 68 anos. Esse grupo fez dois tipos de cirurgia de IV em 14 pacientes com perda vestibular de diferentes etiologias, com seis pacientes implantados pela via extralabiríntica e oito com a abordagem intralabiríntica. O grupo de Washington fez seu primeiro IV em um homem de 56 anos. De acordo com as publicações, esse grupo usou a abordagem intralabiríntica para implante em quatro pacientes com diagnóstico de doença de Ménière unilateral.
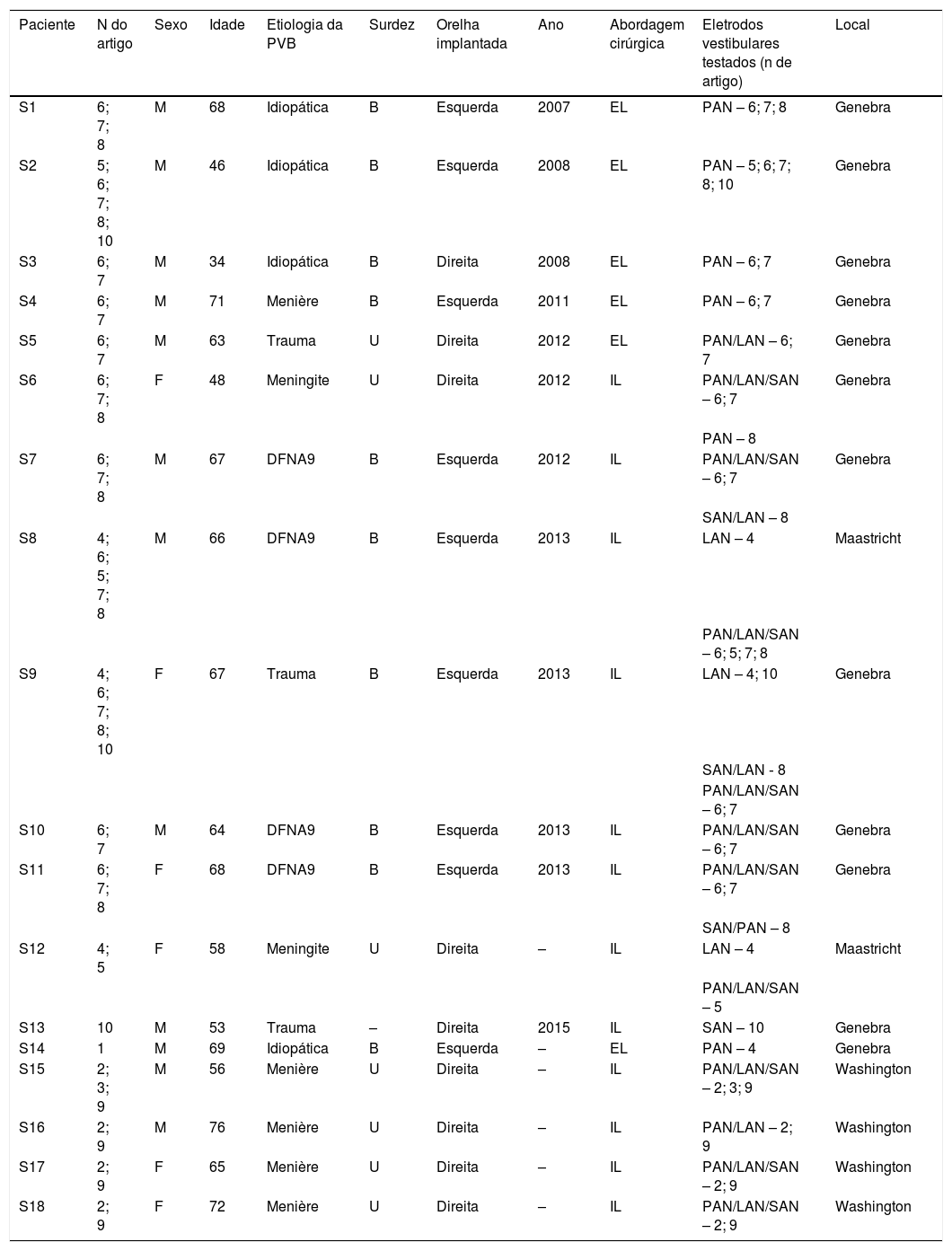
Dados demográficos e detalhes do implante para cada paciente com hipofunção vestibular bilateral
| Paciente | N do artigo | Sexo | Idade | Etiologia da PVB | Surdez | Orelha implantada | Ano | Abordagem cirúrgica | Eletrodos vestibulares testados (n de artigo) | Local |
|---|---|---|---|---|---|---|---|---|---|---|
| S1 | 6; 7; 8 | M | 68 | Idiopática | B | Esquerda | 2007 | EL | PAN – 6; 7; 8 | Genebra |
| S2 | 5; 6; 7; 8; 10 | M | 46 | Idiopática | B | Esquerda | 2008 | EL | PAN – 5; 6; 7; 8; 10 | Genebra |
| S3 | 6; 7 | M | 34 | Idiopática | B | Direita | 2008 | EL | PAN – 6; 7 | Genebra |
| S4 | 6; 7 | M | 71 | Menière | B | Esquerda | 2011 | EL | PAN – 6; 7 | Genebra |
| S5 | 6; 7 | M | 63 | Trauma | U | Direita | 2012 | EL | PAN/LAN – 6; 7 | Genebra |
| S6 | 6; 7; 8 | F | 48 | Meningite | U | Direita | 2012 | IL | PAN/LAN/SAN – 6; 7 | Genebra |
| PAN – 8 | ||||||||||
| S7 | 6; 7; 8 | M | 67 | DFNA9 | B | Esquerda | 2012 | IL | PAN/LAN/SAN – 6; 7 | Genebra |
| SAN/LAN – 8 | ||||||||||
| S8 | 4; 6; 5; 7; 8 | M | 66 | DFNA9 | B | Esquerda | 2013 | IL | LAN – 4 | Maastricht |
| PAN/LAN/SAN – 6; 5; 7; 8 | ||||||||||
| S9 | 4; 6; 7; 8; 10 | F | 67 | Trauma | B | Esquerda | 2013 | IL | LAN – 4; 10 | Genebra |
| SAN/LAN ‐ 8 | ||||||||||
| PAN/LAN/SAN – 6; 7 | ||||||||||
| S10 | 6; 7 | M | 64 | DFNA9 | B | Esquerda | 2013 | IL | PAN/LAN/SAN – 6; 7 | Genebra |
| S11 | 6; 7; 8 | F | 68 | DFNA9 | B | Esquerda | 2013 | IL | PAN/LAN/SAN – 6; 7 | Genebra |
| SAN/PAN – 8 | ||||||||||
| S12 | 4; 5 | F | 58 | Meningite | U | Direita | – | IL | LAN – 4 | Maastricht |
| PAN/LAN/SAN – 5 | ||||||||||
| S13 | 10 | M | 53 | Trauma | – | Direita | 2015 | IL | SAN – 10 | Genebra |
| S14 | 1 | M | 69 | Idiopática | B | Esquerda | – | EL | PAN – 4 | Genebra |
| S15 | 2; 3; 9 | M | 56 | Menière | U | Direita | – | IL | PAN/LAN/SAN – 2; 3; 9 | Washington |
| S16 | 2; 9 | M | 76 | Menière | U | Direita | – | IL | PAN/LAN – 2; 9 | Washington |
| S17 | 2; 9 | F | 65 | Menière | U | Direita | – | IL | PAN/LAN/SAN – 2; 9 | Washington |
| S18 | 2; 9 | F | 72 | Menière | U | Direita | – | IL | PAN/LAN/SAN – 2; 9 | Washington |
Ano, ano de implantação; B, bilateral; EL, extralabiríntica; Idade, idade na implantação; IL, intralabiríntica; LAN, nervo ampular lateral; PAN, nervo ampular posterior; SAN, nervo ampular superior; U, unilateral.
Como existe um risco não negligenciável de induzir perda auditiva profunda com a cirurgia de implante, nos casos de indivíduos com surdez unilateral, o IV foi implantado na mesma orelha afetada.
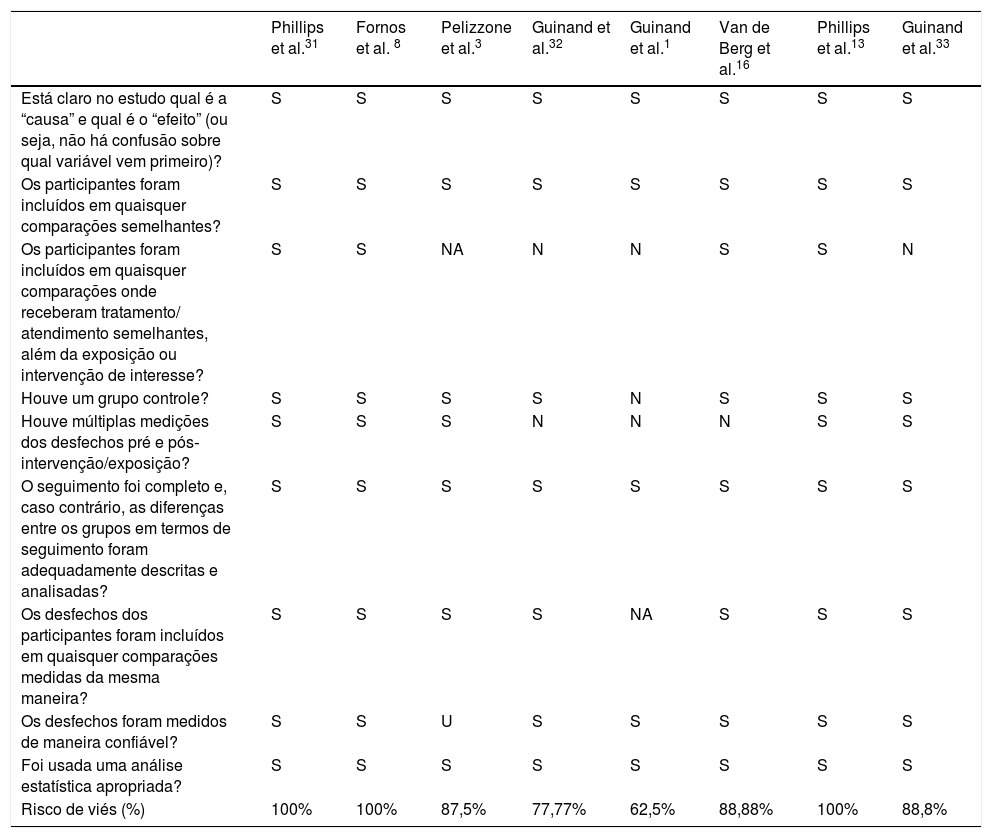
Todos os dez artigos foram analisados com a JBI critical appraisal checklist para estudos quase‐experimentais (tabela 3) e a JBI critical appraisal checklist para relatos de caso (tabela 4), de acordo com cada tipo de estudo, e nove artigos3,8,10,13,16,30–33 apresentaram baixo risco de viés e um artigo1 mostrou risco moderado de viés.21
JBI Critical appraisal checklist para estudos quase‐experimentais
| Phillips et al.31 | Fornos et al. 8 | Pelizzone et al.3 | Guinand et al.32 | Guinand et al.1 | Van de Berg et al.16 | Phillips et al.13 | Guinand et al.33 | |
|---|---|---|---|---|---|---|---|---|
| Está claro no estudo qual é a “causa” e qual é o “efeito” (ou seja, não há confusão sobre qual variável vem primeiro)? | S | S | S | S | S | S | S | S |
| Os participantes foram incluídos em quaisquer comparações semelhantes? | S | S | S | S | S | S | S | S |
| Os participantes foram incluídos em quaisquer comparações onde receberam tratamento/ atendimento semelhantes, além da exposição ou intervenção de interesse? | S | S | NA | N | N | S | S | N |
| Houve um grupo controle? | S | S | S | S | N | S | S | S |
| Houve múltiplas medições dos desfechos pré e pós‐intervenção/exposição? | S | S | S | N | N | N | S | S |
| O seguimento foi completo e, caso contrário, as diferenças entre os grupos em termos de seguimento foram adequadamente descritas e analisadas? | S | S | S | S | S | S | S | S |
| Os desfechos dos participantes foram incluídos em quaisquer comparações medidas da mesma maneira? | S | S | S | S | NA | S | S | S |
| Os desfechos foram medidos de maneira confiável? | S | S | U | S | S | S | S | S |
| Foi usada uma análise estatística apropriada? | S | S | S | S | S | S | S | S |
| Risco de viés (%) | 100% | 100% | 87,5% | 77,77% | 62,5% | 88,88% | 100% | 88,8% |
I, incerto; N, não; NA, não aplicável; S, sim.
JBI critical appraisal checklist para relatos de caso
| Guyot et al.30 | Golub et al.10 | |
|---|---|---|
| As características demográficas do paciente foram claramente descritas? | S | S |
| A história do paciente foi claramente descrita e apresentada como linha do tempo? | N | S |
| A condição clínica atual do paciente na apresentação foi claramente descrita? | S | S |
| Os testes de diagnóstico ou métodos de avaliação e os resultados foram claramente descritos? | S | S |
| A(s) intervenção(ões) ou procedimento(s) de tratamento foram claramente descritos? | S | S |
| A condição clínica pós‐intervenção foi claramente descrita? | S | S |
| Os eventos adversos (danos) ou eventos imprevistos foram identificados e descritos? | S | S |
| O relato do caso fornece lições para o aprendizado? | S | S |
| Risco de viés (%) | 87,5% | 100% |
N, não; S, sim.
Não foi possível fazer uma metanálise nesta RS porque os artigos incluídos apresentavam metodologias e medidas muito diferentes resultantes dos testes.
Guyot et al.30 conduziram um estudo de caso em que avaliaram um paciente com surdez bilateral idiopática e perda vestibular, com agendamento para implante coclear e que recebeu um IV. Eles avaliaram se o paciente poderia se adaptar à estimulação elétrica contínua do sistema vestibular e se era possível provocar movimentos oculares artificiais através da modulação da estimulação. Sucessivos ciclos on‐off de estimulação elétrica contínua nos eletrodos vestibulares resultaram em resposta nistagmática com duração progressivamente menor. Uma vez atingido o estado adaptado mediante estimulação constante, as modulações de amplitude ou frequência da estimulação elétrica produziram movimentos oculares oscilatórios suaves e conjugados.
Phillips et al.31 fizeram o IV em quatro pacientes com doença de Ménière unilateral intratável na orelha direita. Todos os indivíduos receberam um implante IV (UW/Nucleus), baseado no implante coclear Nucleus Freedom (Cochlear, Ltd.). Durante a cirurgia, um arranjo de eletrodos foi inserido no espaço perilinfático adjacente à ampola de cada um dos três canais semicirculares por meio de uma pequena fenestração no labirinto ósseo adjacente às ampolas. As fenestrações foram fechadas com fáscia enquanto se tentava não ocluir os lúmens do canal e os eletrodos externos às fenestrações foram fixados com sutura. Durante o posicionamento do arranjo, foram obtidos registros do potencial de ação composto evocado eletricamente (PACEE) para aprimorar a colocação dos eletrodos para ativação aferente. Quando PACEE de grande amplitude não eram obtidos em níveis baixos de corrente, a fenestração era ampliada e o conjunto de eletrodos movido para mais perto da ampola. Um eletrodo terra redondo remoto foi colocado sob o músculo temporal. Em três indivíduos, a cirurgia foi feita com arranjos de eletrodos estimuladores em três canais semicirculares da orelha direita afetada e um indivíduo foi implantado com arranjos apenas nos canais lateral e posterior. Antes dos estudos de estimulação elétrica, antes e depois do implante do dispositivo, os pacientes foram submetidos a uma bateria de testes vestibulares clínicos para avaliar sua função vestibular subjacente, inclusive prova calórica, cadeira rotatória, acuidade visual dinâmica, avaliação da vertical visual subjetiva e posturografia. Os testes foram feitos em duas sessões, de 17 a 136 semanas após o implante cirúrgico. A análise dos dados feita com o sistema offline mostrou que todos os indivíduos apresentaram diminuição significativa das respostas calóricas na orelha implantada no período pós‐operatório e apresentaram redução dos níveis pré‐operatórios no ganho da cadeira rotatória, um avanço de fase e uma assimetria na orelha implantada no pós‐operatório.
Golub et al.10 descreveram o caso de um paciente com doença de Ménière não controlada submetido a IV. Seis semanas após o implante, a prótese foi programada com um mapeamento para uso domiciliar (take‐home map). Nove configurações de nível foram fornecidas em incrementos de 25μA, variaram de 150μA a 350μA. O paciente foi instruído a progredir através das configurações do mapa durante uma crise aguda até que os sintomas fossem minimizados ou eliminados. Mais ou menos na época em que seu processador de uso domiciliar (take‐home processor) foi fornecido, as crises cessaram. Ele teve apenas uma crise subsequente, que ocorreu seis meses após a cirurgia. O desligamento do implante também resultou em um aumento dos sintomas. Comparativamente aos valores pré‐operatórios, o teste de velocidade da cadeira rotatória revelou um decréscimo de ganho em seis semanas pós‐implante. Sessenta e três semanas pós‐implante, o ganho foi recuperado, mas houve uma assimetria persistente. O teste calórico indicou uma fraqueza unilateral de 26% no pré‐operatório, que aumentou para 95% em seis semanas de pós‐operatório com ligeira recuperação para 71% em 87 semanas. A estimulação elétrica resultou em movimentos oculares específicos do canal, embora os limiares tenham aumentado ao longo do tempo.
Fornos et al.8 investigaram se era possível que o IV restaurasse artificialmente o RVO em três pacientes com Perda Vestibular Bilateral (PVB). A etiologia desses pacientes foi meningite (F‐58), DFNA9 (M‐66) e traumática (F‐67) e eles foram recrutados no Serviço de Otorrinolaringologia e Cirurgia de Cabeça e Pescoço dos Hospitais Universitários de Genebra e na Divisão de Distúrbios do Equilíbrio no Maastricht University Medical Center. Esses indivíduos receberam um protótipo de neuroprótese vestibular que consistiu em um implante coclear modificado (MED‐EL, Innsbruck, Áustria) e o implante foi feito com uma abordagem cirúrgica intralabiríntica. Esse dispositivo, além do conjunto de eletrodos cocleares, forneceu eletrodos extracocleares, os quais foram implantados próximo ao ramo ampular do nervo vestibular. Os pacientes foram submetidos a rotações horizontais de corpo inteiro (ou seja, ao redor do eixo vertical) em completa escuridão (sem estabilização da cabeça). As velocidades de rotação tinham um perfil sinusoidal com uma amplitude de pico de 30°/s, com base no perfil de movimento típico da locomoção humana. Cinco frequências de rotação diferentes (0,1, 0,25, 0,5, 1 e 2Hz) foram testadas. As rotações foram alcançadas com uma cadeira rotatória com velocidade controlada e personalizada. Os testes foram feitos sem qualquer estimulação elétrica (sistema off) e mediante estimulação elétrica do canal semicircular lateral (sistema on). Na condição com o sistema on, a amplitude da estimulação elétrica foi modulada através do sinal de movimento captado por um sensor inercial (giroscópio). Respostas do RVO significativamente mais altas foram observadas quando o protótipo estava ligado. Além disso, as respostas do RVO aumentaram significativamente à medida que a intensidade da estimulação aumentava, alcançaram em média 79% daquelas medidas em voluntários saudáveis nas mesmas condições experimentais.
Pelizzone et al.3 fizeram o IV em três pacientes com surdez bilateral profunda e perda vestibular. Primeiro, o paciente recebeu estimulação elétrica em estado estacionário para restaurar uma taxa de disparo “espontâneo” artificial em seu nervo vestibular em estado desaferentado até que as respostas nistagmáticas desaparecessem. Com o paciente nesse “estado adaptado”, um giroscópio para codificar movimentos rotacionais foi usado para modular a amplitude do trem de pulsos fornecido ao eletrodo vestibular. Os movimentos oculares do paciente foram registrados enquanto o paciente era submetido a rotações de corpo inteiro no plano horizontal e escuridão total. Os resultados mostraram que no pico de velocidade angular a 1Hz o ganho de RVO dos três pacientes testados era muito baixo no sistema offline (ganhos <0,2). No sistema na condição on, os ganhos nos três pacientes melhoraram significativamente, alcançaram até 75%–98% do ganho mediano do RVO de voluntários saudáveis. Além disso, o ganho aumentou significativamente à medida que aumentavam a intensidade da estimulação. O ganho de RVO no sistema offline foi muito baixo, enquanto aumentou significativamente no sistema na condição on, alcançou 51%–69% do observado em voluntários saudáveis.
Guinand et al.32 descreveram 11 pacientes com perda vestibular bilateral (PVB), com surdez severa bilateral ou unilateral, todos implantados com um IV desenvolvido por meio de um IC modificado, forneceram de um a três eletrodos extracocleares. Durante a cirurgia, a matriz coclear foi inserida e cada ramo extracoclear foi colocado na proximidade dos ramos ampulares posterior (PAN), lateral (LAN) e superior (SAN) do nervo vestibular. No total, 24 eletrodos vestibulares foram implantados nesses pacientes. Uma abordagem cirúrgica extralabiríntica foi feita em cinco pacientes e uma abordagem intralabiríntica foi usada em seis pacientes. A ativação do dispositivo não ocorreu antes de quatro semanas após a cirurgia, quando a cicatrização do local da cirurgia foi considerada completa. A videonistagmografia (VNG) e a eletronistagmografia (ENG) foram usadas para os testes vestibulares. O teste do impulso cefálico (HIT, sigla do inglês, Head Impulse Test) foi feito com o sistema Ulmer (Synapsis©; Marselha, França), o EyeSeeCam (EyeSeeCam VOG©; Munique, Alemanha) e/ou o ICS Impulse (Otometrics, Dinamarca). Os eletrodos cocleares sempre foram desligados durante o procedimento experimental. A posição angular bidimensional eye‐in‐head foi registrada com um sistema de vídeo‐óculo‐grafia 2D rápido monocular (EyeSeeCam VOG; Munique, Alemanha). Todas as gravações do movimento ocular foram feitas no escuro com os pacientes sentados em posição ereta. Não foram relatadas complicações relacionadas à cirurgia ou ao procedimento experimental. Apesar de diferentes etiologias (idiopática, Ménière, traumática, meningite e DFNA9) e diferentes durações da doença, foi possível obter movimentos oculares controlados de amplitudes e direções variáveis em todos os 11 pacientes com PVB até aproximadamente oito anos após o implante. Esses resultados indicam que a estimulação elétrica do nervo vestibular tem um impacto funcional significativo; movimentos oculares gerados dessa maneira poderiam ser suficientes para restaurar a estabilização do olhar durante as tarefas diárias essenciais, como caminhar. No entanto, os resultados também demonstram que os movimentos oculares evocados eletricamente resultam em perda significativa da acuidade visual. É importante ressaltar que o objetivo do implante vestibular não é prejudicar a acuidade visual, mas o contrário. A partir do momento em que um ajuste fino e uma combinação apropriada entre estimulação e movimento do paciente foram executados, a possibilidade de melhoria na acuidade visual é real e isso melhoraria a estabilização das imagens na retina.
Em um estudo posterior dos mesmos 11 pacientes, Guinand et al.1 não avaliaram a acuidade visual conforme feito por Guinand et al.,32 os quais1 apresentaram 24 eletrodos vestibulares disponíveis para estimulação elétrica nesses 11 pacientes. Desses, três eletrodos não respondiam e, portanto, um limiar vestibular foi determinado em apenas 21 dos 24 eletrodos disponíveis. Em 19 desses eletrodos, o nível de conforto superior correspondeu à estimulação do nervo facial. Em dois eletrodos, nenhum nível de conforto superior foi determinado, mesmo na maior amplitude de corrente testada (550mA). A posição eye‐in‐head bidimensional foi registrada com um sistema de vídeo‐óculo‐grafia 2D rápido monocular (EyeSeeCam VOG) para avaliar os efeitos da estimulação elétrica. Todas as gravações dos movimentos oculares foram feitas no escuro com os pacientes sentados em posição ereta com estimulação elétrica no labirinto para capturar o eRVO. Consistente com os intervalos dinâmicos bastante variáveis ??medidos, o intervalo das velocidades oculares também foi muito variável. A média das velocidades de pico por eletrodo entre pacientes foi de 8,7–7,6°/s para PAN (n=11), 13–12,5°/s para LAN (n=6) e de 11,9–6,6°/s para SAN (n=5). Os pacientes diagnosticados com DFNA9 apresentaram as menores respostas. Um dos resultados deste estudo é que os movimentos oculares podem ser evocados com sucesso em um grupo heterogêneo de pacientes em relação à etiologia do déficit ou à duração da doença.
Van de Berg et al.16 investigaram como as características do eRVO se modificaram em função da frequência de modulação em pacientes com IV e compararam esses resultados com as respostas “naturais” do RVO obtidas em voluntários saudáveis pareados por idade submetidos a rotações horizontais de corpo inteiro, com perfis de velocidade sinusoidal equivalentes nas mesmas frequências. Sete pacientes com PVB receberam um protótipo de IV que consistia em um implante coclear modificado (MED‐EL, Innsbruck, Áustria) com ramos extracocleares para estimulação vestibular. Foram testados 12 eletrodos vestibulares implantados em diferentes locais anatômicos: quatro na vizinhança do nervo ampular superior, três na vizinhança do nervo ampular lateral e cinco nas proximidades do nervo ampular posterior. A intensidade de modulação foi mantida constante durante os ensaios experimentais, foram testadas três frequências de modulação (0,5, 1 e 2Hz). Os experimentos com o eRVO foram conduzidos sob condições estacionárias e a estimulação elétrica foi feita exclusivamente em um eletrodo vestibular de cada vez. Resultados individuais e agrupados revelaram claramente um comportamento dependente da frequência para os três locais de estimulação. Eles observaram um efeito forte e significativo da frequência no pico da velocidade total do olho no eRVO: o pico total de velocidade ocular aumentou com o aumento da frequência para ambos os grupos, sem qualquer efeito significante entre os grupos. Outras características do eRVO (ângulo, índice de habituação e assimetria) não mostraram efeito significativo dependente da frequência. Esse efeito foi semelhante ao observado no RVO “natural”. O ângulo do eRVO foi muito variável em todo o grupo com PVB para toda a faixa de frequência testada. Esses resultados demonstraram que, pelo menos na faixa de frequência específica (limitada) testada, o IV é muito semelhante à dependência natural do sistema vestibular à frequência.
Phillips et al.13 implantaram quatro indivíduos com doença de Ménière unilateral intratável. Embora os indivíduos apresentassem função vestibular limitada e audição relativamente ruim no período pré‐cirúrgico, após o implante do IV os indivíduos perderam função auditiva e vestibular na orelha implantada em relação aos níveis pré‐operatórios, sem recuperação da função vestibular. Além disso, a estimulação elétrica do IV pareceu ser bem tolerada pelos pacientes, sem dor significativa, náusea ou percepção auditiva evocada eletricamente em associação com a estimulação elétrica. No geral, os resultados dos registros do PACEE mostraram um aumento na velocidade horizontal da fase lenta com uma taxa de estímulo crescente. Os autores também observaram uma diminuição geral ao longo do tempo na velocidade de fase lenta provocada pela estimulação elétrica na maioria dos canais nesses quatro indivíduos com doença de Ménière.
Guinand et al.33 avaliaram três pacientes com PVB grave e implantados com IV. O RVO de alta frequência foi avaliado com o vHIT, enquanto a estimulação elétrica modulada por movimento foi feita através de um dos eletrodos vestibulares implantados um de cada vez. Em três dos cinco eletrodos testados, o ganho de RVO aumentou monotonicamente com o aumento da força de estimulação quando os impulsos cefálicos foram entregues no plano do canal implantado. Nos três casos apresentados, as respostas de RVO medidas sem ativação do IV foram deficientes em ambas as direções do plano testado.
DiscussãoA presente RS foi concebida para identificar evidências na literatura científica de que o IV melhora a função vestibular em indivíduos com PVB.
Observamos que a abordagem intralabiríntica foi mais frequentemente usada, provavelmente porque a abordagem extralabiríntica é cirurgicamente mais desafiadora em relação à extensão do local exato da estimulação. No entanto, a principal desvantagem da abordagem intralabiríntica é o risco de comprometimento auditivo quando o labirinto é aberto e os eletrodos são inseridos nos canais semicirculares.1 Por esse motivo, o grupo de Genebra‐Maastricht optou por fazer a cirurgia apenas em pacientes surdos na orelha implantada. O grupo de Washington submeteu a implante cirúrgico10,13,31 quatro pacientes com doença de Ménière com audição residual e todos perderam a audição. No entanto, esses resultados negativos não implicam necessariamente que a audição sempre será afetada pela implantação de eletrodos nos canais semicirculares. Pesquisas em macacos rhesus mostraram que a preservação auditiva é possível com a abordagem intralabiríntica.9,14,34,35 Portanto, o principal desafio de estudos futuros é aprimorar a técnica cirúrgica e desenvolver eletrodos que possam provocar uma estimulação efetiva para a ativação da função vestibular e, simultaneamente, preservar a audição em pacientes.
A equipe de Genebra‐Maastricht mostrou que, com um perfil de movimento virtual para modular a estimulação elétrica basal dos ramos ampulares do nervo vestibular, foi possível gerar artificialmente movimentos oculares em todos os pacientes com PVB em seu grupo, independentemente da etiologia da doença, duração da implantação e modelo do protótipo do implante vestibular usado. Seus resultados também demonstram que movimentos oculares evocados eletricamente resultaram em perda significativa da acuidade visual.
O grupo da Universidade de Washington mostrou que a implantação do dispositivo em quatro pacientes com doença de Ménière produziu perda auditiva e vestibular na orelha implantada. Esses resultados sugerem que a estimulação elétrica do órgão terminal vestibular em indivíduos humanos forneceu entradas vestibulares controladas ao longo do tempo, mas nos pacientes com doença de Ménière esse resultado foi aparentemente obtido à custa da audição e da função vestibular na orelha implantada.
Observamos também melhores respostas artificiais do RVO em frequências de rotação mais altas. Nas frequências de rotação de 0,1 e 0,25Hz, o RVO artificialmente evocado estava praticamente ausente. A resposta do RVO começou a aumentar em 0,5Hz, atingiu um desempenho máximo nas frequências de rotação de 1 e 2Hz. Esse fenômeno lembra as características dinâmicas bem conhecidas e documentadas do RVO normal. Atividades cotidianas importantes, como caminhar, induzem movimentos cefálicos predominantemente na faixa de frequência de 1 a 2Hz. Essa restauração artificial do RVO nesses pacientes implantados pode, portanto, ser considerada uma recuperação funcional substancial. Além disso, essa conquista foi possível para pacientes com durações de déficits substancialmente diferentes e com diferentes etiologias de PVB.
Essa RS mostrou que seres humanos podem se adaptar à estimulação elétrica do sistema vestibular sem muito desconforto e que 77% dos 18 pacientes implantados apresentaram melhoria na função vestibular.
ConclusãoDiversos estudos demonstraram a viabilidade do IV de restaurar o RVO em uma ampla faixa de frequência e mostraram novos desafios para o desenvolvimento dessa tecnologia para garantir uma melhoria na função vestibular sem perda da audição.
Em conjunto, essas evidências são promissoras no alcance da primeira opção real para a reabilitação de pacientes com PVB, garantiram mais esforços de pesquisa e maior interesse no campo.
Conflitos de interesseOs autores declaram não haver conflitos de interesse.
Como citar este artigo: Azevedo YJ, Ledesma AL, Pereira LV, Oliveira CA, Bahmad Junior F. Vestibular implant: does it really work? A systematic review. Braz J Otorhinolaryngol. 2019;85:788–98.
A revisão por pares é da responsabilidade da Associação Brasileira de Otorrinolaringologia e Cirurgia Cérvico-Facial