The use of surgical decompression of facial hemispasm due to the loop in the internal auditory canal is not always accepted due to the risk related to the surgical procedure. Currently a new surgical technique allows surgeons to work in safer conditions.
ObjectiveTo report the results with endoscope‐assisted retrosigmoid approach for facial nerve microvascular decompression in hemifacial spasm due to neurovascular conflict. The surgical technique is described.
MethodsWe carried out a prospective study in a tertiary referral center observing 12 (5 male, 7 female) patients, mean age 57.5 years (range 49–71) affected by hemifacial spasm, that underwent to an endoscope assisted retrosigmoid approach for microvascular decompression. We evaluated intra‐operative findings, postoperative HFS resolution and complication rates.
ResultsHemifacial spasm resolution was noticed in 9/12 (75%) cases within 24h after surgery and in 12/12 (100%) subjects within 45 days. A significant (p<0.001) correlation between preoperative historical duration of hemifacial spasm and postoperative recovery timing was recorded. Only 1 patient had a complication (meningitis), which resolved after intravenous antibiotics with no sequelae. No cases of cerebrospinal fluid leak, facial palsy or hearing impairment were recorded. Hemifacial spasm recurrence was noticed in the only subject where the neurovascular conflict was due to a vein within the internal auditory canal.
ConclusionsThe endoscope assisted retrosigmoid approach technique offers an optimal visualization of the neurovascular conflict thorough a minimally invasive approach, thus allowing an accurate decompression of the facial nerve with low complication rates. Due to the less invasive nature, the procedure should be considered in functional surgery of the cerebellar pontine angle as hemifacial spasm treatment, specially when the procedure is performed by an otolaryngologist.
O uso de descompressão cirúrgica do espasmo hemifacial devido ao loop no canal auditivo interno nem sempre é aceito devido ao risco relacionado ao procedimento cirúrgico. Atualmente, uma nova técnica cirúrgica permite trabalhar em condições seguras.
ObjetivoRelatar os resultados que obtivemos com a abordagem retrosigmóidea assistida por endoscopia para a descompressão microvascular do nervo facial em casos de espasmo hemifacial devido a conflito neurovascular. A técnica cirúrgica é descrita.
MétodoRealizamos um estudo prospectivo em um centro de referência terciária observando 12 pacientes (5M, 7F), com média de idade de 57,5 (intervalo 49-71) anos com espasmo hemifacial submetidos a uma abordagem retrosigmóide assistida por endoscopia para descompressão microvascular. Foram avaliados os achados intraoperatórios, a resolução pós-operatória do espasmo hemifacial e as taxas de complicações.
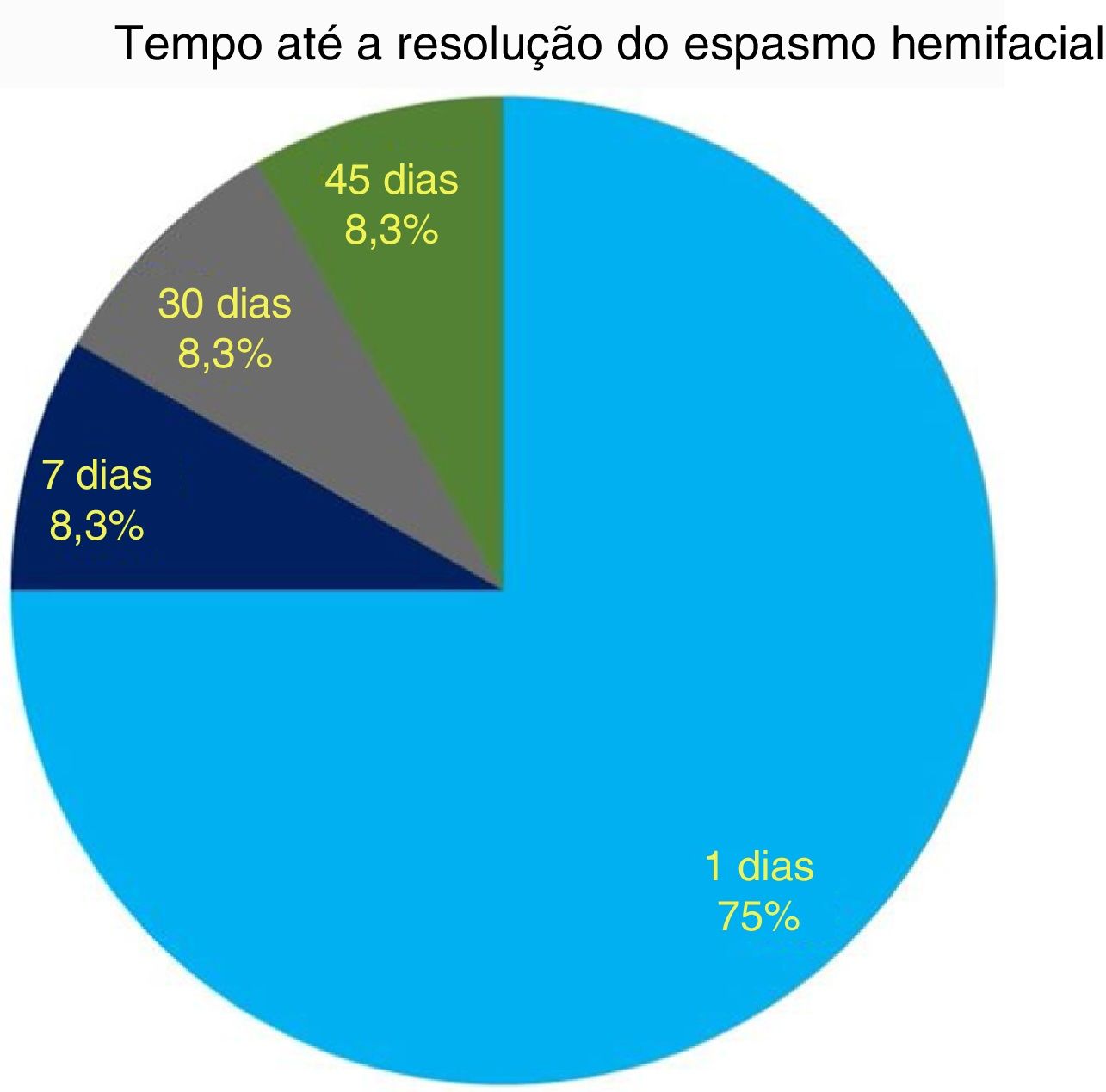
ResultadosA resolução do espasmo hemifacial foi observada em 9/12 (75%) dos casos nas 24 horas após a cirurgia e em 12/12 (100%) dos indivíduos até 45 dias. Uma correlação significativa (p<0,001) entre a duração do histórico pré‐operatório de espasmo hemifacial e o tempo de recuperação pós‐operatório foi registrado. Apenas um paciente apresentou uma complicação (meningite), que foi resolvida após administração de antibióticos por via intravenosa sem sequelas. Nenhum caso fístula liquórica, paralisia facial ou deficiência auditiva foi registrado. A recorrência do espasmo hemifacial foi observada em único indivíduo em quem o conflito neurovascular foi causado por um vaso no interior do canal auditivo interno.
ConclusõesA técnica da abordagem retrosigmóidea assistida por endoscopia oferece uma ótima visualização do conflito neurovascular através de uma abordagem minimamente invasiva, permite assim uma descompressão precisa do nervo facial com baixas taxas de complicações. Por ser menos invasivo, o procedimento deve ser considerado na cirurgia funcional do ângulo pontocerebelar como tratamento de espasmo hemifacial, especialmente quando o procedimento é feito por um otorrinolaringologista.
O espasmo hemifacial (EHF) é uma série unilateral, involuntária e paroxística de movimentos tônico‐clônicos dos músculos faciais. O EHF primário é causado por uma compressão vascular arterial ou venosa do nervo facial.1–4 A compressão de vasos supostamente causa desmielinização nervosa, com consequente alteração na transmissão de sinais, resulta em espasmo muscular no território inervado pelo nervo facial.1–4 Duas possíveis teorias sobre a fisiopatologia do EFH têm sido relatadas na literatura: as hipóteses “central” e “periférica”. De acordo com a primeira, a lesão do nervo facial, devido ao impacto neurovascular, teria uma ação regressiva no núcleo facial, causaria hiperexcitabilidade neural. Ao contrário, de acordo com a hipótese “periférica”, os sintomas clínicos resultariam da geração de impulsos ectópicos e alteração de transmissão devido à desmielinização do nervo facial.4 Muito embora nenhuma evidência definitiva tenha sido relatada sobre qual teoria é a mais relevante, ambos os mecanismos provavelmente contribuem juntos para o início da EHF.
O tratamento médico para o EHFS é a injeção de neurotoxina botulínica (BoNT). A BoNT bloqueia a liberação de acetilcolina mediada pelo íon cálcio na junção sináptica e dá alívio transitório do EHF em 85% dos casos. As limitações desse tratamento são a curta duração do alívio dos sintomas, os altos custos e o risco de não responsividade secundária devido à produção de anticorpos neutralizantes. Outras limitações estão relacionadas a doenças neurológicas preexistentes que contraindicam injeções de neurotoxina ou possíveis interações de BoNT com outros fármacos.5 Nessas condições, a descompressão microvascular (DMV) representa a única opção para obter a resolução do EHF e uma melhoria na qualidade de vida do paciente.6–12
Esse tratamento curativo consiste na descompressão cirúrgica do nervo facial e na separação do vaso agressor do nervo pela interposição de uma lâmina de teflon. As taxas de sucesso em longo prazo da DMV variam entre 83% e 97%.2,3,8 Muito embora a DMV seja descrita como um procedimento seguro, a frequência de complicações cirúrgicas relatadas na literatura não é negligenciável.7–14 A fim de maximizar a taxa de sucesso e reduzir a frequência de complicações cirúrgicas, vários autores propuseram a associação entre a abordagem microscópica tradicional e a endoscópica.15–23 De acordo com essa técnica “combinada”, o procedimento é feito microscopicamente, enquanto o endoscópio é usado para visualizar melhor o vaso agressor antes da descompressão e para confirmar a separação do vaso do nervo no fim da cirurgia. Apesar da melhoria dos resultados positivos obtidos com a técnica “combinada”, algumas complicações pós‐operatórias, especialmente fístula liquórica (LCR), foram relatadas.15–23 Na tentativa de reduzir ainda mais a taxa de complicações e confirmar a redução da morbidade, investigamos os resultados obtidos com uma abordagem retrosigmóidea minimamente invasiva ou “em buraco de fechadura” assistida por endoscopia para a DMV no EHF. A técnica cirúrgica e os resultados são relatados.
MétodoO protocolo foi autorizado pelo Comitê de Ética do Hospital Silvestrini, embora nenhum número tenha sido liberado de acordo com a legislação da área da saúde italiana, uma vez que este não foi considerado um estudo experimental. O estudo foi feito de acordo com a declaração de Helsinque.
Entre dezembro de 2012 e dezembro de 2014, 12 pacientes (cinco homens/sete mulheres), com média de 57,5 anos (variação de 49 a 71) com EHF foram submetidos à abordagem retrosigmóidea minimamente invasiva assistida por endoscopia para DMV no departamento de otorrinolaringologia de um centro de referência terciário.
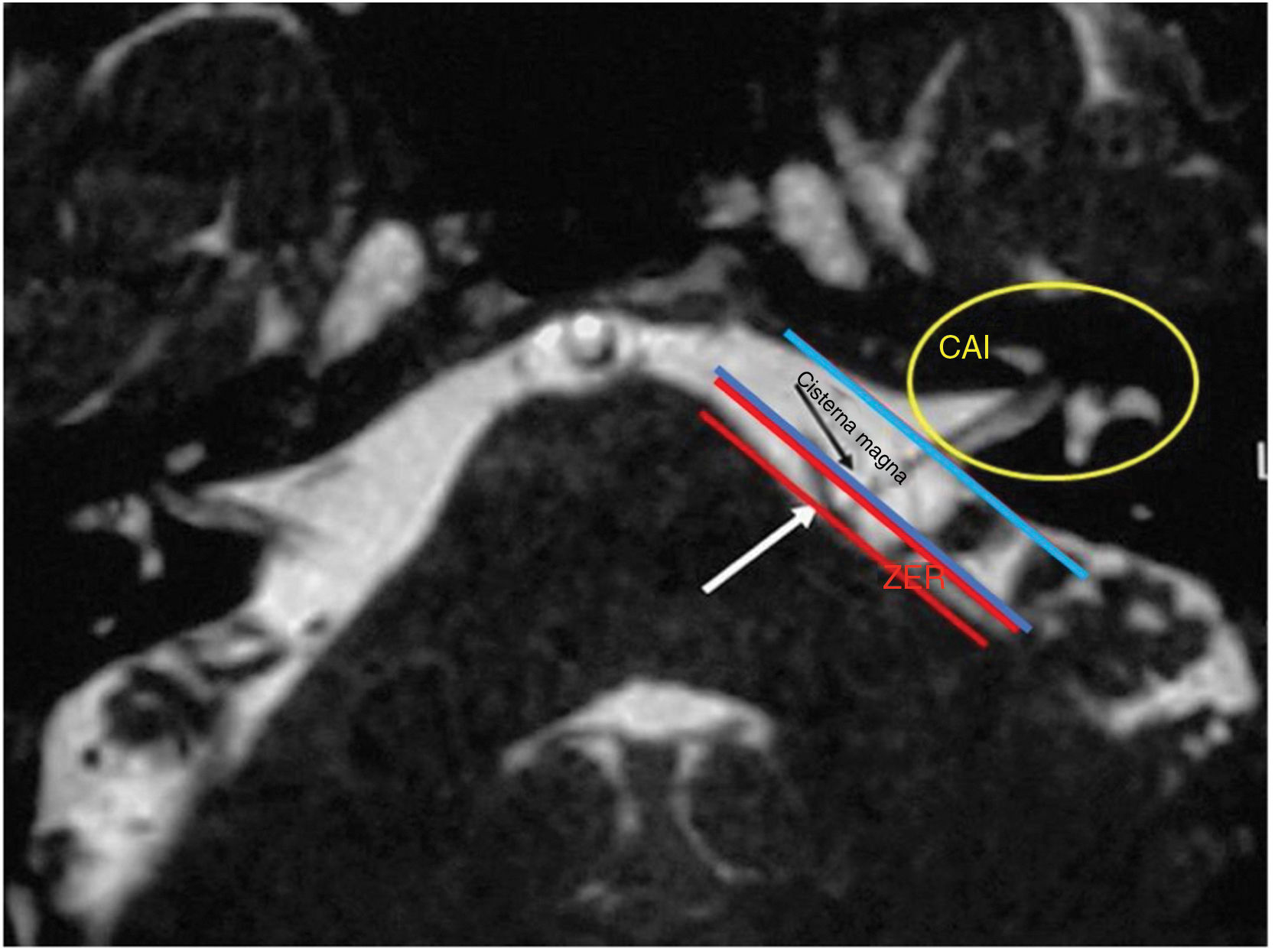
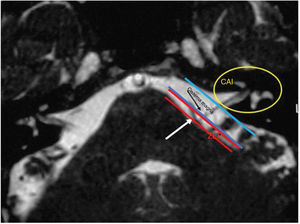
O diagnóstico de EHF foi feito com base na história clínica dos indivíduos e imagens radiológicas. Em todos os pacientes, imagens por ressonância magnética (RM) e/ou angiografia por ressonância magnética (Angio‐RM)8–11 com sequências T1 e T2 foram feitas para descartar outras neuropatias cranianas do ângulo pontocerebelar (APC). A sequência T2da RM é a mais sensível para identificar os vasos que impactam o nervo facial8–24 na zona de entrada da raiz (ZER) do APC e, mais raramente, na entrada do poro. Todos os pacientes assinaram o termo de consentimento informado.
Todos os procedimentos foram feitos pela mesma equipe cirúrgica. Sob anestesia geral, o paciente foi colocado em decúbito dorsal e a cabeça elevada em cerca de 15 graus, colocada sobre um “donut de borracha”. Se necessário (pacientes com excesso de peso com pescoço curto e/ou ombros grandes), uma elevação adicional da cabeça de até 30 graus pode ser obtida com lençóis adicionais sob o “donut”. A cabeça foi virada contralateralmente ao lado cirúrgico para deixar o local operatório voltado para cima e ligeiramente flexionado sobre o ombro oposto. A testa foi presa com fita adesiva; não foi usada fixação por pino no crânio. Durante a cirurgia, a função do nervo facial foi monitorada através de um sistema de monitoramento eletromiográfico24 (NIM 2.0 Medtronic Inc®, Minneapolis, MN, EUA).
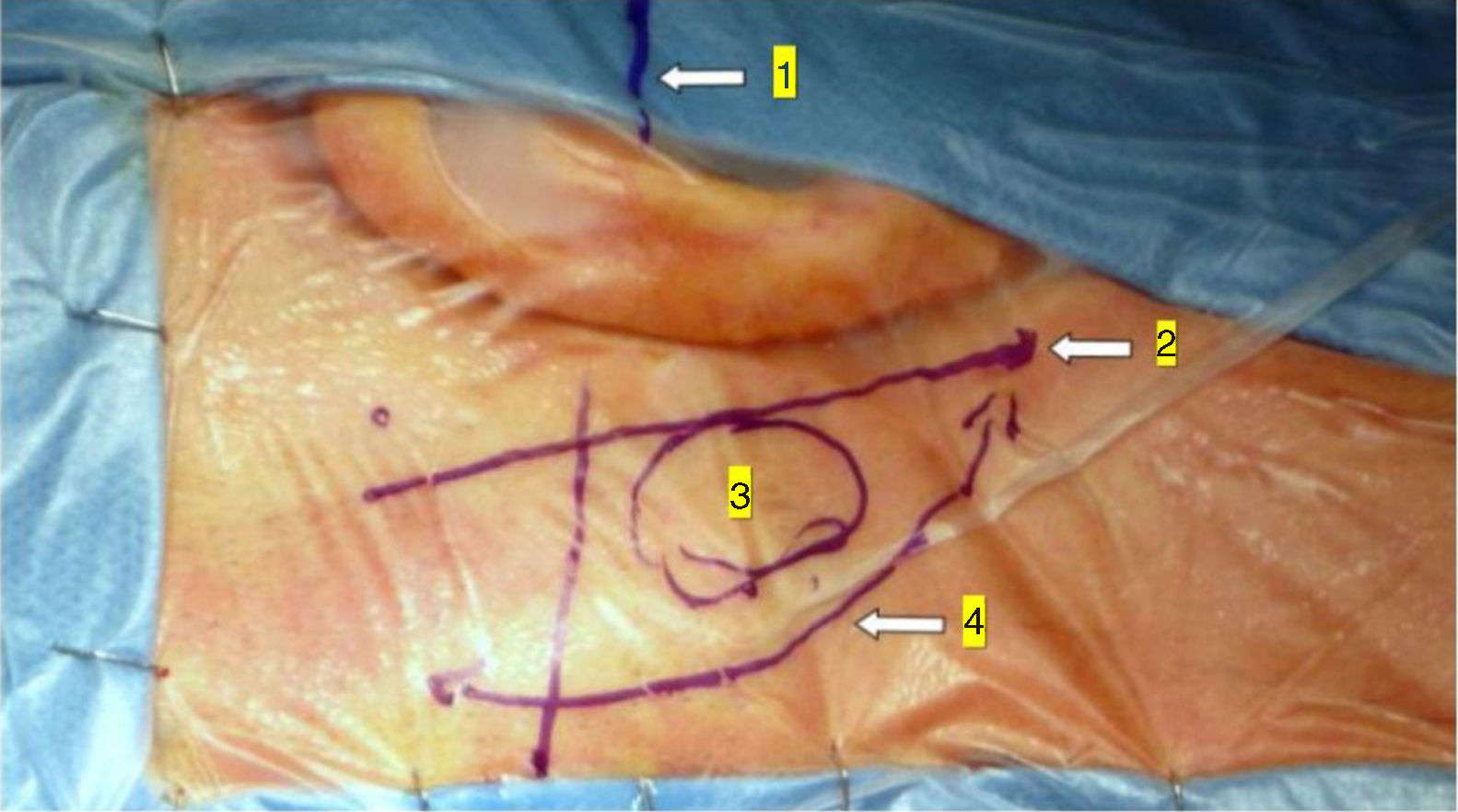
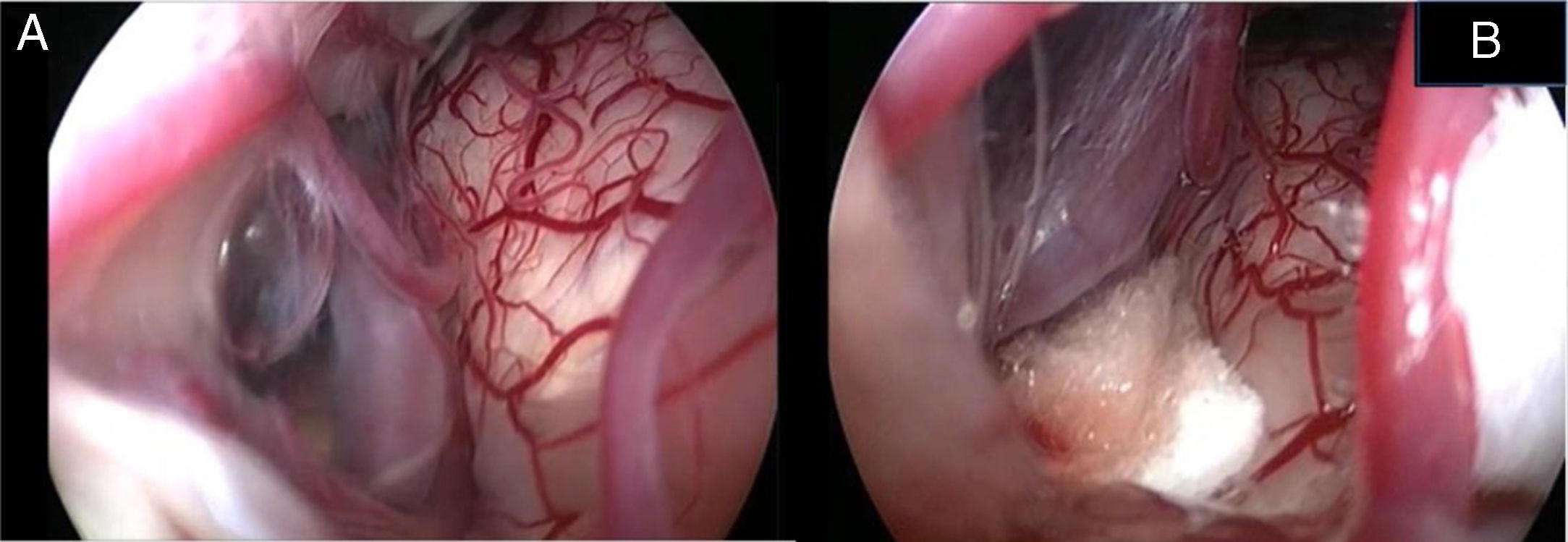
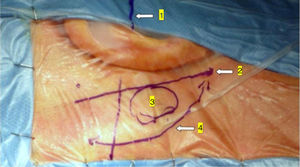
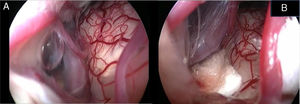
Na área retroauricular, ao longo das linhas de incisão propostas (fig. 1), foram injetados 5 a 7mL de lidocaína a 2% com epinefrina 1:100.000 para favorecer a hemostasia e dissecção dos tecidos moles. Uma incisão cutânea de 6 a 8cm em forma de arco foi feita com o lado convexo voltado para trás. Foi feita a cerca de 1cm da suposta borda posterior da craniotomia e a dois dedos até a projeção da hélice para a região retromastoide. A incisão em tal área pode evitar trauma a ambos, a artéria occipital e o nervo C2. Um retalho de pele é elevado anteriormente. Uma incisão musculoperiosteal foi feita com cauterização monopolar. A perfuração óssea para a craniotomia retrosigmoide iniciou‐se ao redor da veia emissária, manteve‐a no centro como um marco. Uma broca cortante grande foi usada no início, enquanto uma broca de diamante foi necessária ao aproximar‐se da dura e do seio sigmoide para preservar suas superfícies. Uma craniotomia circular de 1,5 a 2cm de diâmetro foi feita em volta ao seio sigmoide. A dura‐máter foi aberta em forma de V, iniciou‐se logo atrás dos seios sigmoides para reduzir a necessidade de retração mecânica do cerebelo durante o acesso ao CAI. Então, a incisão dural foi feita 1 a 2mm das bordas da craniotomia para facilitar a ressutura da dura‐máter no fim da cirurgia. A hiperventilação anestesiológica foi feita para reduzir a pressão liquórica intracraniana e retrair o cerebelo espontaneamente. Uma vez que o “relaxamento” cerebelar suficiente é alcançado, um cotonoide ou compressa neurocirúrgica fina do tipo Neuropatch (1,5cm de largura por 5cm de comprimento) é colocado sobre o cerebelo para protegê‐lo de possíveis lesões enquanto instrumentos são introduzidos. A cisterna magna é aberta para obter acesso ao APC. Com o microscópio, a membrana aracnoide que circunda os nervos cranianos VIII e os nervos cranianos inferiores é dissecada. O procedimento continua com o uso do endoscópio (Rígido 4mm, 30°, da KARL STORZ®, Tuttlingen, Alemanha). O feixe acusticofacial é o marco central do APC e a área de conflito neurovascular (CNV) é identificada abaixo, na ZER do nervo facial. O vaso agressor mais comum é a artéria cerebelar posteroinferior (PICA de posterior inferior cerebelar artery) (fig. 2A). Um vaso de impacto adicional (artéria cerebelar anteroinferior – AICA de anterior inferior cerebelar artery) está normalmente localizado ao longo da porção da cisterna do nervo facial e algumas vezes está parcialmente localizado no início do canal auditivo interno (CAI), é necessária uma perfuração parcial do poro, que é feita para permitir a descompressão do vaso.
Abordagem retrosigmóidea minimamente invasiva (lado direito). A imagem mostra os parâmetros anatômicos para o acesso cirúrgico:1) plano de Frankfurt entre a região cantal externa e a borda superior do tragus; 2) plano muscular do digástrico; 3) projeção do local da craniotomia; 4) incisão cirúrgica.
Mais uma vez, com o uso do microscópio cuidadosamente, o(s) vaso(s) arterial(ais) agressor(es) é(são) separado(s) do nervo facial. Às vezes, imediatamente após a separação do nervo facial, uma trilha de “liberação” de estímulos elétricos pode ser notada no monitoramento do nervo facial, o que confirma o sucesso da descompressão.17 Esponjas de teflon® são interpostas entre todos os vasos agressores, a fim de evitar um novo contato neurovascular e para isolar o nervo facial (fig. 2B). Se uma veia impactar o nervo facial, ela é cuidadosamente coagulada com uma pinça bipolar após o descolamento do vaso. No fim do procedimento de descompressão, o bom posicionamento do teflon é verificado com o endoscópio. Os cotonoides são removidos e o APC é preenchido com solução salina e, em seguida, a dura‐máter é suturada com pontos únicos reabsorvíveis; para garantir a resistência à água, tecido conjuntivo adicional é colocado e fixado por cola biológica. O patê de osso, obtido com pó de osso (coletado durante a perfuração craniana) misturado com cola de fibrina é usado para fechar o local da craniotomia. Os retalhos musculoperiosteal e cutâneos são suturados cuidadosamente em camadas com pontos reabsorvíveis únicos. Um curativo compressivo é aplicado e mantido por quatro dias. O paciente é acordado da anestesia geral, extubado, levado para a sala de pós‐operatório para uma observação de três horas e depois levado à enfermaria comum. O paciente deixa o hospital após uma semana. Os pacientes foram acompanhados periodicamente por dois anos após a cirurgia.
Coleta de dados e análise estatísticaOs dados relativos a idade e sexo dos pacientes, início do EHF, lado do EHF, lado do loop, vaso envolvido no CNV, tratamentos feitos antes da cirurgia, comorbidades, desfechos e complicações cirúrgicas e tempo entre a cirurgia e a resolução do EHF foram coletados. Os dados foram representados como frequências e porcentagens. A análise estatística foi feita com o programa SPSS 10.0 for Windows (SPSS, Chicago, Illinois). O teste t de Student (t), o coeficiente de correlação de Pearson e Spearman (r) e o teste qui‐quadrado (QQ) foram usados quando apropriado. Um valor de p <0,05 foi considerado estatisticamente significante.
ResultadosA tabela 1 resume os principais achados de nossa amostra.
Descrição dos pacientes incluídos no estudo, o vaso envolvido no CNV e os resultados pós‐operatórios
| Paciente (sexo/idade) | Lado | Vaso responsável (S) | Resultado |
|---|---|---|---|
| M/60 | Esquerdo | Veia intracanalicular em contato com a ponte | Recorrência após 1 ano |
| W/57 | Direito | PICA+vertebral | Resolução |
| M/71 | Esquerdo | AICA | Resolução |
| W/54 | Esquerdo | Vertebral | Resolução atrasada |
| W/55 | Direito | PICA | Resolução |
| W/47 | Esquerdo | AICA | Resolução |
| W/53 | Esquerdo | PICA | Resolução atrasada |
| M/49 | Esquerdo | PICA | Resolução |
| W/59 | Esquerdo | AICA | Resolução atrasada |
| M/66 | Direito | Vertebral | Resolução |
| W/61 | Esquerdo | PICA | Resolução |
| M/58 | Esquerdo | PICA+vertebral | Resolução |
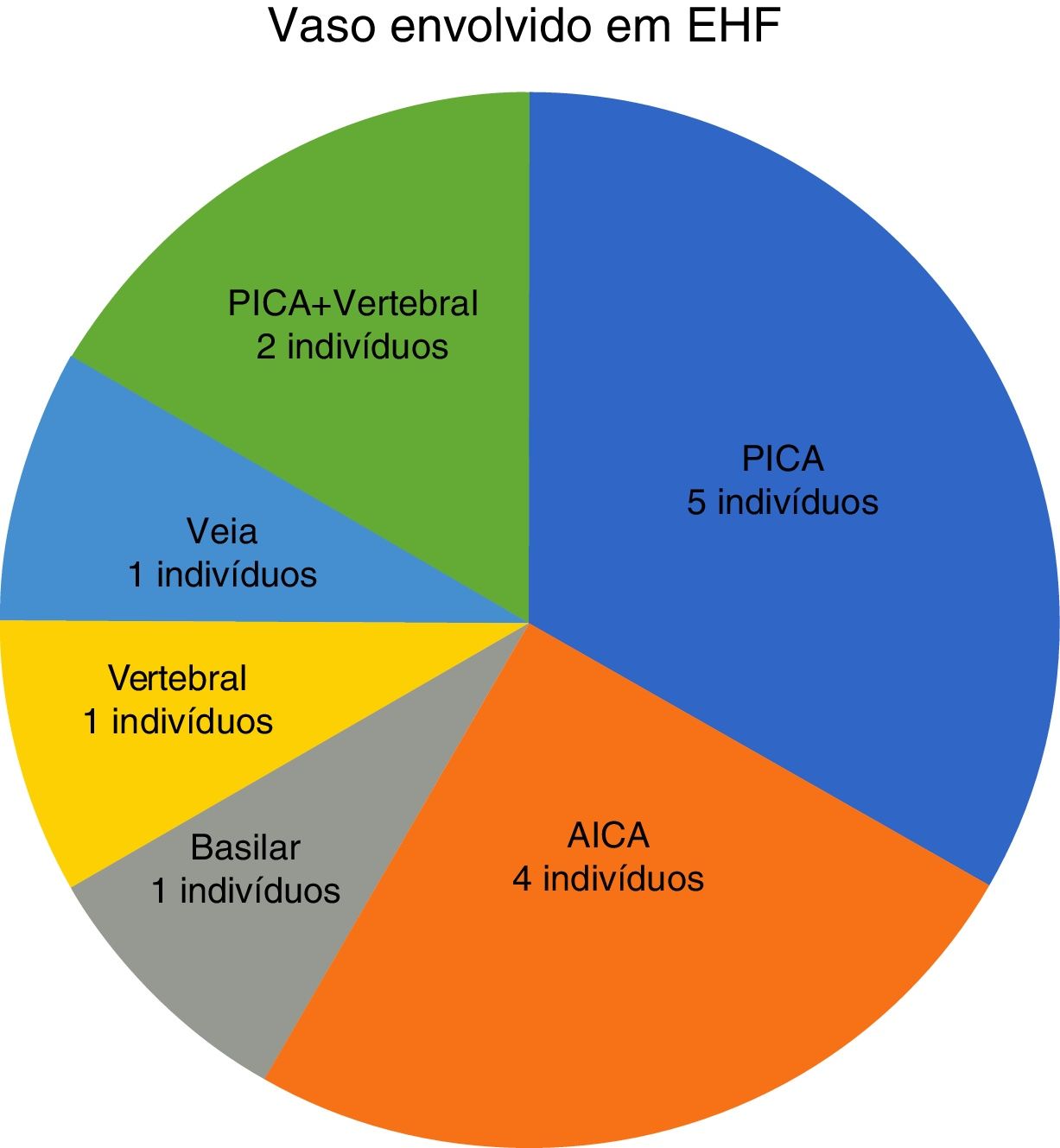
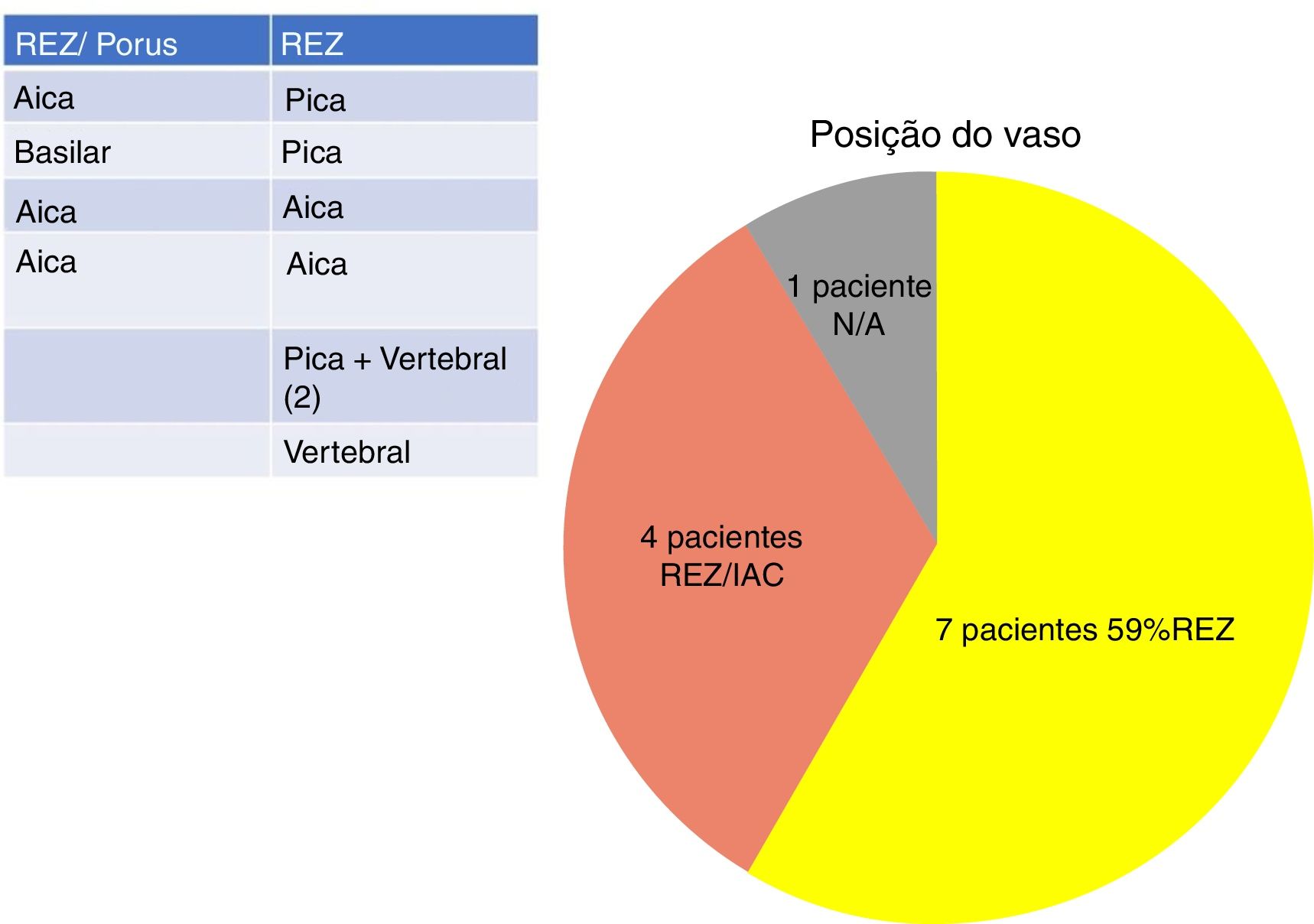
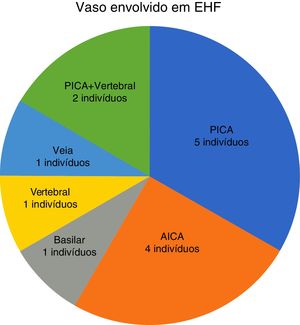
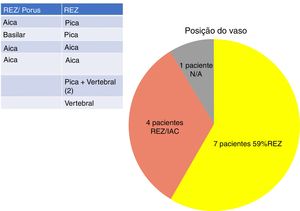
Em nosso estudo, todos os pacientes (100% dos casos) apresentaram uma correlação entre diagnóstico e achados cirúrgicos. Observamos uma predominância de CNVs do lado esquerdo (8/12 indivíduos) com envolvimento mais frequente (51% vs. 25%) da artéria cerebelar posteroinferior (PICA) em relação à artéria cerebelar anteroinferior (AICA). Em dois casos foi detectado um múltiplo impacto da artéria vertebral PICA no nervo facial. As artérias basilar e vertebral foram responsáveis pelo CNV em um caso cada (fig. 3). Um loop arterial que impactava o nervo facial foi encontrado, projetava‐se da entrada do poro acústico em 33% (4/12 pacientes) dos casos e envolvia apenas a área ZER em 69% (7/12) dos indivíduos (fig. 4), com resultado estatisticamente significante (p <0,05). No único paciente com EHS e RM negativa para CNV, foi identificado um vaso que cruzava o nervo facial; o vaso era intracanalicular e em contato com a ponte. Nossos pacientes relataram uma história clínica prévia de presença de EHF com uma média de 10 anos (DP=7,1; IC95% 2‐29) no momento da cirurgia e 66% deles haviam sido submetidos a tratamento prévio com BoNT.
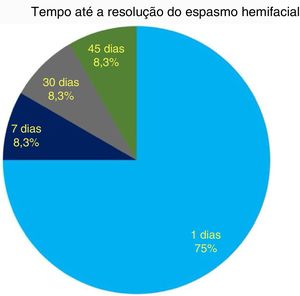
Quanto ao resultado funcional, observamos a resolução do EHF em 24 horas após a cirurgia em 9/12 (75%) casos, enquanto todos os pacientes apresentaram resolução do EHF em 45 dias (fig. 5). Não foi encontrada correlação entre o tempo de resolução da EHF e o vaso agressor (PICA, AICA ou artéria vertebral) (QQ, p=0,7).
O teste de Spearman identificou uma correlação negativa significante (p <0,001) (Pearson) entre a duração do histórico pré‐operatório de EHF e o tempo de recuperação pós‐operatório; isso significa que um aumento dos anos de EHF corresponde a uma rápida recuperação pós‐operatória.
Complicações pós‐operatórias foram observadas em 2/12 (16%) dos casos: um paciente apresentou meningite e um apresentou infecção da incisão cirúrgica. O indivíduo que apresentou meningite era hipertenso; recebeu antibióticos por via IV com resolução da meningite e não apresentou sequelas em longo prazo. Entre nossos pacientes, 25% (3/12) tinham hipertensão e 16% tinham hipertrigliceridemia (2/12); nenhuma dessas condições influenciou o tempo de recuperação do EHF. Nenhum caso fístula liquórica, paralisia facial ou deficiência auditiva foi registrado. Durante o seguimento, a recorrência de EHF foi observada 12 meses após a cirurgia somente no indivíduo no qual a veia impactante foi identificada. Nenhuma correlação significativa foi observada entre os resultados funcionais e as diferentes artérias envolvidas no CNV.
DiscussãoEm nosso estudo, foi observada uma associação constante entre o lado do EHF e o local do CNV, o que confirma o conceito de que um contato entre o loop de um vaso e o nervo facial é responsável pelo espasmo facial (fig. 6). Apesar de não haver diferença significante em relação ao local de compressão do nervo (ZER vs. CAI) em nossos pacientes, em nossa casuística registramos uma maior frequência de envolvimento do poro (33%) em relação a outros autores;2,8–10 o uso da abordagem combinada oferece uma visão melhor da trajetória do vaso agressor graças ao endoscópio que permite ver a posição do vaso a 360°. O uso de um endoscópio de 30° permitiu uma melhor visualização abrangente do CAI com relação à visão linear reta do microscópio.
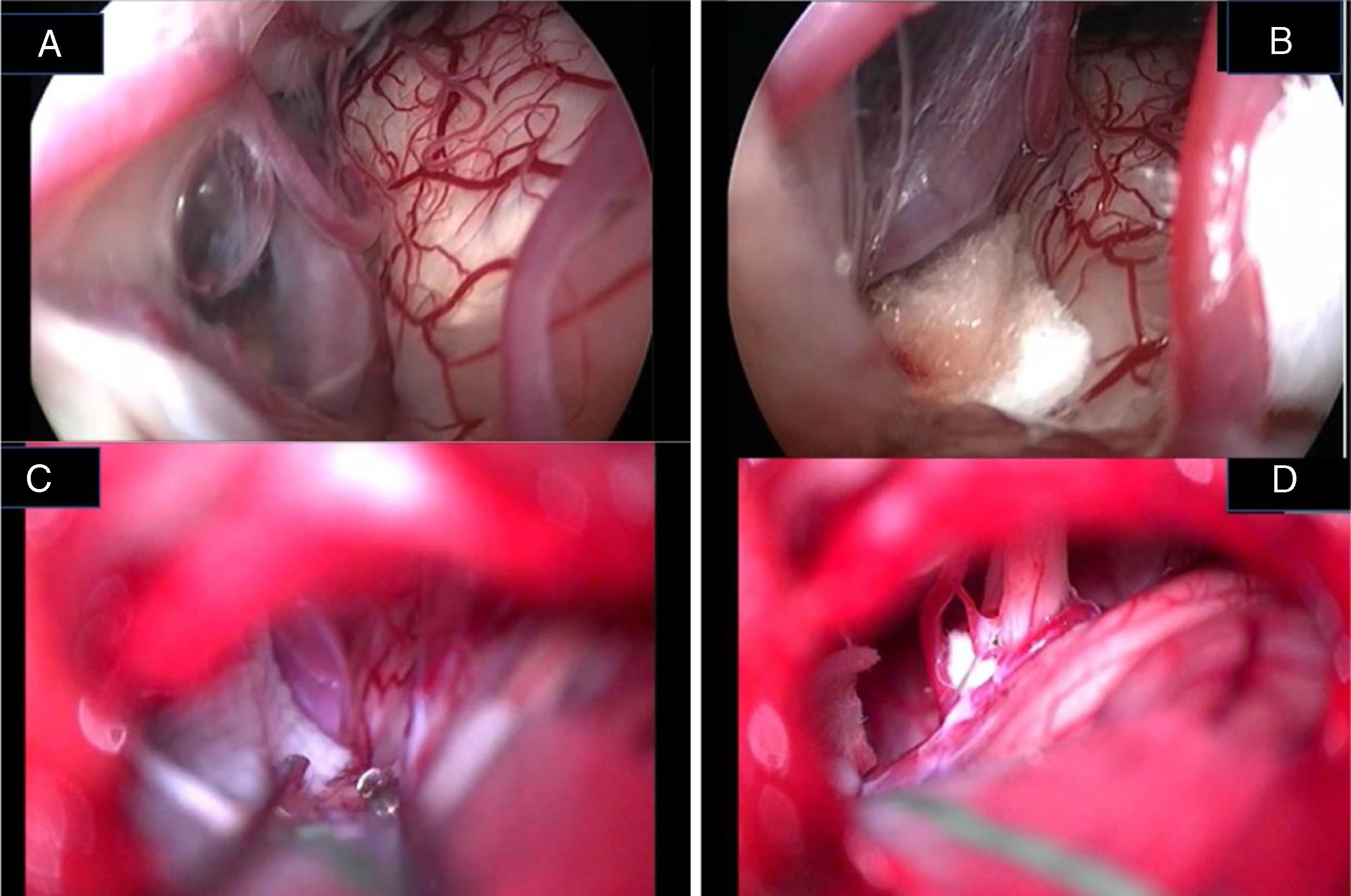
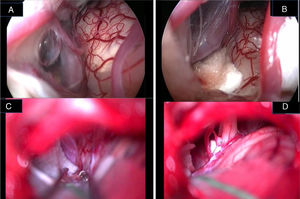
Desde que Jannetta em 197712 descreveu os princípios da DMV, que consistem em destacar o(s) loop(s) vascular(es) agressor(es) e fixá‐los(s) com uma esponja sintética não absorvente sem traumatismo intencional ou ruptura do nervo, uma melhoria importante nos resultados cirúrgicos tem sido relatada na literatura. No entanto, esse procedimento não está livre de limitações, uma vez que vários relatos documentaram insucessos, recorrências e complicações relacionadas à descompressão microscópica.7–14 Há relatos de uma taxa de mortalidade de 0,2% para descompressão vascular assistida por microscopia para EHF e uma taxa de complicações gerais de 5% a 25% para disfunção temporária e de 2% a 10% para comprometimento neurológico permanente.7–14 A maioria das complicações envolve a função do nervo auditivo ou facial. A taxa relatada de comprometimento do nervo auditivo é de 3% a 5% para disfunção temporária e de 2% a 3% para perda auditiva permanente.7–14,23 O comprometimento do nervo facial ocorre temporariamente em aproximadamente 4% dos pacientes, enquanto 1% a 2% apresentam déficit permanente do nervo facial.7–14 A chave para o sucesso da cirurgia de descompressão para EHF inclui uma visualização precisa de todos os conflitos neurovasculares e confirmação de descompressão completa do nervo no fim do procedimento (fig. 7A‐D). Como já relatado por Jannetta, a anatomia da fossa posterior e o tamanho limitado da craniotomia dificultam a visualização adequada de todo o trajeto do nervo facial e a porção do poro somente através do uso do microscópio.12–14
Imagem endoscópica (A, B) e microscópica (C, D) de um conflito neurovascular antes da descompressão (A, C) e após interposição de folha de Teflon® entre a alça vascular e o nervo facial (B, D). Observe a diferença na resolução dos detalhes e na definição das estruturas anatômicas entre a tecnologia endoscópica full‐HD e a visão microscópica. VII, nervo facial; VIII, nervo estatoacústico; XII, nervo hipoglosso; T, esponja de Teflon®; v, veia.
A fim de superar tais limitações, alguns autores propuseram o uso da combinação de endoscópio‐microscópio para identificar o local real do CNV e reduzir as taxas de complicações.15–23 Particularmente, o autor principal deste estudo já relatou o uso do endoscópio para auxiliar a DMV do nervo facial e demonstrou uma taxa adicional de precisão de 72% na identificação de conflitos neurovasculares sem necessidade de deslocamento do feixe acústico‐facial e retração do cerebelo,15–17,21,22 o que permitiu uma diminuição nas taxas de complicações neurológicas.
Nossa experiência confirma as vantagens da abordagem minimamente invasiva assistida por endoscopia em termos de resolução do EHF e taxas de complicações em relação à abordagem microscópica tradicional.7–14 Em particular, 75% dos nossos pacientes apresentaram resolução completa do EHF 24 horas após a cirurgia, enquanto os demais pacientes apresentaram uma recuperação “tardia”. A recuperação tardia pode ser causada pela distorção neural e hiperatividade do núcleo do nervo facial ou por fenômenos inflamatórios pós‐operatórios,24 mesmo que nenhuma explicação definitiva desse evento esteja disponível. Quanto ao único caso que apresentou recorrência de EHF após a cirurgia, o paciente apresentava uma veia que impactava o nervo facial. Nesse caso, o cautério bipolar foi usado para coagular o vaso; os autores são de opinião que uma cicatriz (evento pós‐inflamatório) ou repermeação da veia foi a causa da recorrência.
Nossos resultados positivos são possibilitados pela visão operatória “panorâmica” e pela visualização abrangente oferecida pelo endoscópio, além da alta resolução da moderna tecnologia full‐HD (fig. 7A‐D). Recomendamos o endoscópio com ângulo de 30° como a ferramenta mais apropriada para a descompressão vascular. A abordagem minimamente invasiva abre uma pequena janela na área sigmoide, preserva melhor a queda da pressão craniana e reduz a dor de cabeça e o risco de fístula liquórica. Nossa alta taxa de sucesso não é devida apenas ao uso do endoscópio, mas à minimização de abordagens e manobras. O procedimento feito com auxílio do endoscópio permite ao cirurgião identificar com precisão a estrutura e minimizar os movimentos da mão durante a cirurgia, devido à visão completa da área cirúrgica. Os movimentos seguros devido à ampla compreensão da área de conflito eliminam a pressão no cerebelo e o risco de complicações neurológicas centrais. A importância da visão angulada é da maior significância no caso de CNV no interior do CAI, a fim de fazer as manobras de descompressão com segurança. No caso do CNV se projetar parcialmente no CAI, é necessária uma perfuração parcial do canal antes da separação vascular e da inserção de um pequeno pedaço de esponja fina de poliuretano (Neuropatch® ‐ B/Braun‐Aesculap®, Tuttlingen, Alemanha) entre a AICA e o nervo facial. No entanto, a descompressão não é a ideal por causa da artéria labiríntica, que não permite mover o vaso impactado de seu contato com os nervos VIII e VII. Nossa abordagem minimamente invasiva permitiu cirurgias mesmo em pacientes idosos (nosso paciente mais idoso tinha 71 anos) sem aumento de sequelas pós‐operatórias.
ConclusãoOs resultados deste estudo confirmam que a abordagem retrosigmóidea minimamente invasiva assistida por endoscopia é um procedimento seguro para visualizar conflitos neurovasculares que levam ao EHF, permite uma eficiente descompressão do nervo facial com um risco muito baixo de morbidade. Graças às reduzidas taxas de complicações pós‐operatórias, essa abordagem deve ser considerada o padrão‐ouro em pacientes com espasmo hemifacial, qualquer que seja sua idade.
Conflitos de interesseOs autores declaram não haver conflitos de interesse.
Como citar este artigo: Ricci G, Di Stadio A, D’Ascanio L, La Penna R, Trabalzini F, della Volpe A, et al. Endoscope‐assisted retrosigmoid approach in hemifacial spasm: our experience. Braz J Otorhinolaryngol. 2019;85:465–72.
A revisão por pares é da responsabilidade da Associação Brasileira de Otorrinolaringologia e Cirurgia Cérvico‐Facial.