A desnutrição é um problema comum em pacientes com carcinoma de células escamosas de cabeça e pescoço e tem um efeito negativo nos resultados cirúrgicos.
ObjetivoTentamos determinar quais variáveis diagnósticas de desnutrição podem ser usadas como preditivos de complicações pós‐operatórias em pacientes com carcinoma de células escamosas de cabeça e pescoço.
MétodoQuarenta e um pacientes submetidos à cirurgia de carcinoma de células escamosas de cabeça e pescoço foram submetidos a uma avaliação prospectiva. Dados bioquímicos, medidas antropométricas e avaliação da composição corporal foram usados na análise nutricional.
ResultadosVinte e dois pacientes (53,6%) desenvolveram complicações. A dosagem de albumina sérica no primeiro dia pós‐operatório foi a única variável que diferiu significantemente entre os grupos. Um valor de corte de 2,8g/dL distinguiu os pacientes com uma evolução pós‐operatória complicada e não complicada. A normalização dos níveis de albumina ocorreu mais frequentemente e mais rapidamente no grupo sem complicação pós‐operatória.
ConclusãoA albumina sérica medida no primeiro dia pós‐operatório foi a única variável capaz de predizer complicações pós‐operatórias após cirurgia de carcinoma de células escamosas de cabeça e pescoço de grande porte.
A desnutrição é um problema frequente em pacientes com carcinoma de células escamosas de cabeça e pescoço (CCECP), ocorre em 20% a 67% dos casos.1–3 Abuso de álcool, tabagismo, higiene bucal inadequada e hábitos alimentares pouco saudáveis contribuem para que esses pacientes tenham um certo grau de desnutrição antes do início da doença.3 O CCECP aumenta o risco de desnutrição por perturbar diretamente a fisiologia da alimentação, leva a sintomas que afetam a mastigação, prejudicam a ingestão de alimentos e impedem a deglutição.1–3
A desnutrição, por sua vez, afeta diretamente os resultados cirúrgicos, retarda a cicatrização da ferida e, consequentemente, aumenta o risco de infecção, deiscência da ferida, formação de fístula e até ruptura de artéria carótida.4 Os pacientes desnutridos, portanto, têm mortalidade e morbidade aumentadas e permanências hospitalares mais longas, o que leva diretamente ao aumento dos custos de saúde.5
Como não há consenso quanto à avaliação da desnutrição, múltiplas variáveis são usadas para detectá‐la, muitas das quais, no entanto, não refletem adequadamente o estado nutricional do paciente. Além disso, apesar de haver muitas ferramentas diagnósticas de desnutrição em pacientes hospitalizados, não sabemos quais parâmetros nutricionais podem predizer resultados cirúrgicos em pacientes com CCECP.
Embora a ocorrência de desnutrição seja com frequência relatada em pacientes com CCECP, pouca atenção tem sido dada ao seu efeito nos resultados cirúrgicos nessa população específica de pacientes. Considerando a forte associação entre desnutrição e complicações pós‐operatórias,4 o objetivo deste estudo é determinar quais variáveis diagnósticas de desnutrição podem ser usadas como preditivos de complicações pós‐operatórias em pacientes com CCECP.
MétodoO protocolo do estudo foi aprovado pelo comitê de ética em pesquisa e todos os pacientes assinaram o termo de consentimento livre e esclarecido, de acordo com os preceitos do comitê de ética local (protocolo número 0105/07).
Este é um estudo de coorte prospectivo que envolveu pacientes internados no Serviço de Otorrinolaringologia/Cirurgia de Cabeça e Pescoço do Hospital do Servidor Público Estadual de São Paulo Francisco Morato de Oliveira, de janeiro de 2008 a janeiro de 2009. Os pacientes maiores de 18 anos, elegíveis para a cirurgia em bloco (remoção do tumor primário e dissecção do pescoço) para o tratamento de CCECP T2‐T46 foram incluídos no estudo. Os pacientes foram excluídos caso recusassem a participar do estudo ou preenchessem um dos seguintes critérios: menores de 18 anos, uso pré‐operatório de suplementos nutricionais, uso prolongado de corticosteroides, dislipidemia, síndrome nefrótica, insuficiência cardíaca congestiva, insuficiência hepática ou qualquer outra doença que afetasse o metabolismo normal das proteínas hepáticas.
Avaliação pré‐operatóriaOs pacientes foram internados no hospital 72 horas antes da cirurgia e os seguintes dados foram incluídos no formulário de protocolo do estudo: idade, sexo, renda familiar mensal,7 nível de escolaridade,8 subsítio do tumor primário, estágio clínico,6 comorbidades, cirurgia prévia de cabeça e pescoço ou radioterapia.
A análise nutricional foi feita 24 horas antes da cirurgia por nutricionista e consistiu em medidas antropométricas e avaliação da composição corporal por análise de impedância bioelétrica (bioelectricalimpedance analysis – BIA).
Avaliação antropométricaUma fita métrica e uma balança (Welmy®) foram usadas para medir a altura e o peso. O índice de massa corporal (IMC) foi obtido dividindo‐se o peso em quilogramas pelo quadrado da altura em metros.9
Um paquímetro de pregas cutâneas (Lange®) foi usado para medir a prega cutânea tricipital (PCT) no braço não dominante e uma fita métrica foi usada para determinar a circunferência do braço (CB) e a circunferência da panturrilha (CP). As medições foram feitas em triplicata com aproximação de 1‐mm.10,11
A seguinte fórmula foi usada para calcular a porcentagem do peso corporal ideal (%PCI): (PA/P)×100, PA o peso atual e PI o peso ideal. As tabelas da Metropolitan Life Insurance Company de 1983 foram usadas para calcular o PI com base no sexo, altura, idade e tamanho estrutural do corpo. A %PCI foi usada para classificar os pacientes como portadores de desnutrição leve (80%–90%), moderada (70%–79%) ou grave (< 69%).12
A seguinte fórmula foi usada para calcular a porcentagem de variação do peso (%VP): (PA‐PU)/PU×100, onde PA é o peso atual e PU o peso usual. Uma %VP de <5% indica uma pequena perda de peso, enquanto 5%–10% sugere uma perda de peso potencialmente significativa e>10% uma perda de peso definitivamente significativa.13 Dados adicionais que especificam se a perda de peso foi contínua ou intermitente com os períodos de recuperação de peso também foram obtidos.
Análise de composição corporalTodos os pacientes foram submetidos à análise de bioimpedância elétrica, de acordo com os padrões do National Institute of Health.14 Um analisador de impedância bioelétrica (Biodynamics®, 310e, versão 8.0) foi usado para determinar a resistência e a reatância, que foram então usadas para estimar a água corporal total (ACT), gordura corporal (GC) e massa corporal magra (MCM).
Suporte nutricionalOs pacientes não receberam suporte nutricional no período pré‐operatório. A equação de Harris‐Benedict15 (66.437+(5.0033×altura [cm])+(13,7516×peso[Kg])‐(6.7550×idade para homens e 655.0955+(1.8496×altura [cm])+(9.5634×peso[Kg])‐(4.6756×idade para mulheres) foi usada para estimar individualmente o gasto energético basal (GEB) e o gasto energético total (GET). Todos os pacientes receberam suporte nutricional pós‐operatório, administrado por via enteral.
Avaliação bioquímicaOs seguintes exames laboratoriais foram feitos: hemograma completo, proteína sérica total e suas frações (ensaio colorimétrico), colesterol total e suas frações (ensaio colorimétrico enzimático) e contagem absoluta de linfócitos (CAL), conforme determinado pela seguinte fórmula: (% linfócitos×leucócitos)/100. Uma CAL de 1.200–2.000 células/mm3 sugere depleção leve, enquanto um resultado de 800–1.200 células/mm3 indica depleção moderada e <800 células/mm3 indica depleção grave.16
CirurgiaDados referentes ao tipo de cirurgia e esvaziamento cervical, necessidade de reconstrução do retalho, ocorrência de complicações intraoperatórias e transfusão de hemoderivados foram coletados.
Iodopovidona (PVP‐I) foi usado para o preparo da pele antes da cirurgia e a irrigação com solução salina normal a 0,9% aquecida foi feita antes do fechamento da ferida cirúrgica.
A profilaxia antibiótica consistiu em ceftriaxona e clindamicina administrados por via intravenosa na indução da anestesia e continuados nas 48 horas seguintes.
Curso pós‐operatórioOs pacientes foram transferidos para a unidade de terapia intensiva no pós‐operatório imediato. A alimentação enteral foi iniciada 12‐48 horas após a cirurgia. Albumina sérica foi medida no primeiro, terceiro, quinto e sétimo dia pós‐operatório (DPO). Alguns pacientes precisaram de transfusão de sangue para manter os níveis de hemoglobina (Hb) acima de 10g/dL.
Características clínicas, bioquímicas e radiográficas foram usadas para diagnosticar complicações pós‐operatórias. Foram pesquisadas as seguintes “complicações maiores”, definidas por Van Bokhorst‐de van der Schueren et al.: infecção da ferida operatória (drenagem purulenta espontânea ou cirúrgica); necrose do retalho (lesão isquêmica); fístula salivar orocutânea ou faringocutânea; fístula anastomótico; choque séptico; insuficiência respiratória com necessidade de assistência ventilatória por mais de 12 horas ou retorno à ventilação mecânica após a extubação; e morte.17 O diagnóstico de pneumonia foi baseado nas diretrizes brasileiras para o tratamento de pneumonia hospitalar e associada à ventilação mecânica.18
Os pacientes submetidos à laringectomia total foram submetidos à avaliação videofluoroscópica da deglutição entre o sétimo e o décimo DPO; em todos os outros casos, para o diagnóstico de fístula foi usado o teste de administração oral de azul de metileno diluído em água.
Todos os pacientes incluídos no estudo foram acompanhados até a alta hospitalar.
Análise estatísticaOs dados foram expressos em médias± desvio‐padrão (DP), medianas e intervalos interquartílicos ou valores absolutos e frações. O teste t de Student ou o teste de Mann‐Whitney foram usados para comparar as variáveis contínuas, enquanto o teste qui‐quadrado foi usado para comparar as variáveis categóricas.
Curvas características de operação do receptor (receiver operating characteristic – ROC) foram usadas para avaliar as propriedades preditivas das variáveis em análise. A área sob a curva ROC determinou o poder discriminante geral das variáveis nutricionais para prever complicações pós‐operatórias; além disso, foram identificados os valores de corte com melhor poder preditivo.
O teste log‐rank (teste de Mantel‐Cox) foi usado para comparar as curvas de normalização da albumina, enquanto a razão de riscos (hazard ratios – HR) e seus respectivos intervalos de confiança (IC) foram usados para estimar a magnitude das potenciais diferenças.
A regressão logística será usada para analisar a relação entre as variáveis categóricas dependentes e as variáveis independentes.
Todos os testes foram bicaudais, com valores de p <0,05 considerados estatisticamente significativos. O software de estatística disponível comercialmente GraphPad Prism (versão 6.02 para Windows, San Diego, CA, EUA) foi usado para fazer a análise estatística.
ResultadosForam incluídos no estudo 41 pacientes, 36 homens (87,8%) e cinco mulheres (12,2%), com média de 61,4 anos. Dados sociodemográficos adicionais da população do estudo são apresentados na tabela 1.
Correlação entre dados sociodemográficos, dados clínicos pré e pós‐operatórios e o risco de complicações pós‐operatórias
| Com complicações (n=22) | Sem complicações (n=19) | p‐valor | |
|---|---|---|---|
| Idade | 61,32±10,77 | 61,57±10,42 | 0,941 |
| Sexo | |||
| Masculino | 18 (82%) | 18 (95%) | 0,707 |
| Feminino | 4 (18%) | 1 (5%) | |
| Renda mensala | |||
| Até 3 salários mínimos | 9 (41%) | 8 (42%) | 0,969 |
| Entre 3 e 7 salários mínimos | 10 (45,4%) | 8 (42%) | |
| Acima de 7 salários mínimos | 3 (13,6%) | 3 (16%) | |
| Nível de escolaridadeb | |||
| Analfabetos | 1 (4,5%) | 0 | 0,531 |
| Ensino fundamental incompleto | 10 (45,5%) | 8 (42,1%) | |
| Ensino fundamental completo | 4 (18,2%) | 6 (31,6%) | |
| Ensino médio incompleto | 1 (4,5%) | 3 (15,8%) | |
| Ensino médio completo | 2 (9,1%) | 0 | |
| Ensino superior | 4 (18,2%) | 2 (10,5%) | |
| Subsítio do tumor primário | |||
| Cavidade oral | 9 (40%) | 6 (31,6%) | 0,083 |
| Orofaringe | 6 (27,3%) | 1 (5,2%) | |
| Hipofaringe | 3 (13,6%) | 2 (10,5%) | |
| Laringe | 4 (18,2%) | 10 (52,7%) | |
| Estágio clínico | |||
| II | 2 (9,1%) | 4 (10,5%) | 0,533 |
| III | 7 (31,8%) | 6 (31,6%) | |
| IV | 13 (59,1%) | 9 (47,4%) | |
| T (tamanho do tumor) | |||
| T2 | 4 (18,2%) | 7 (36,8%) | 0,339 |
| T3 | 11 (50%) | 6 (31,6%) | |
| T4 | 7 (31,8%) | 6 (31,6%) | |
| Reconstrução de retalho | |||
| Sim | 7 (31,8%) | 4 (21,1%) | 0,437 |
| Não | 15 (68,2%) | 15 (78,9%) | |
| Transfusão de sangue | |||
| Não | 11 (50%) | 13 (68,4%) | 0,232 |
| Sim | 11 (50%) | 6 (31,6%) | |
| Início da alimentação | |||
| Até 12 horas após a cirurgia | 4 (18,2%) | 8 (42,1%) | 0,247 |
| 12 a 24 horas após a cirurgia | 14 (63,6%) | 10 (52,6%) | |
| 24 a 48 horas após a cirurgia | 2 (9,1%) | 0 (0) | |
| Sem dados | 2 (9,1%) | 1 (5,3%) | |
| Comorbidades | |||
| Sim | 13 (59,1%) | 13 (68,4%) | 0,536 |
| Não | 9 (40,9%) | 6 (31,6%) | |
| Radioterapia anterior | |||
| Sim | 3 (13,6%) | 1 (5,3%) | 0,367 |
| Não | 19 (86,4%) | 18 (94,7%) | |
| Cirurgia anterior | |||
| Sim | 5 (22,7%) | 1 (5,3%) | 0,114 |
| vNão | 17 (77,3%) | 18 (94,7%) | |
Todos os pacientes tinham diagnóstico histopatológico de CCECP: 15da cavidade oral (36,6%), sete da orofaringe (17%), cinco da hipofaringe (12,2%) e 14da laringe (34,2%). Em relação ao estadiamento clínico, a maioria dos pacientes (22) apresentava CCECP de estágio IV (53,7%).
Vinte e quatro pacientes (58,5%) foram submetidos a esvaziamento cervical unilateral, enquanto 17 (41,5%) foram submetidos a procedimento bilateral. Todos os indivíduos precisaram de traqueostomia pós‐operatória. Apenas 26,8% dos pacientes precisaram de reconstrução com retalho: quatro deles com retalho microcirúrgico e sete com retalho miocutâneo de peitoral maior (tabela 1).
De todos os casos incluídos, 22 pacientes (53,6%; IC 95% 38,74% a 67,95%) apresentaram complicações pós‐operatórias, mas nenhum paciente morreu durante o acompanhamento.
Nenhuma variável demográfica apresentou correlação significante com a ocorrência de complicações pós‐operatórias (tabela 1). Em relação às características clínicas, não houve diferença estatisticamente significativa entre os grupos para estadiamento clínico, presença de comorbidades, subsítio do tumor primário, cirurgia ou radioterapia prévia, transfusão de hemoderivados ou necessidade de reconstrução de retalho (tabela 1).
Dos 41 pacientes do estudo, 35 foram submetidos à avaliação da composição corporal por bioimpedância elétrica. Não houve diferença estatisticamente significativa entre os grupos para água corporal total (p=0,1341), gordura corporal (p=0,2051) ou massa corporal magra (p=0,2167) (tabela 2).
Correlação entre dados antropométricos pré‐operatórios, análise de impedância bioelétrica pré‐operatória, dados bioquímicos e hematológicos pré‐operatórios e risco de complicações pós‐operatórias
| Com complicações (n=22) | Sem complicações (n=19) | p‐valor | |
|---|---|---|---|
| %PCIa | |||
| > 90% | 17 (77,3%) | 12 (63,2%) | 0,517 |
| 80%–89% | 2 (9,1%) | 4 (21,1%) | |
| No data | 3 (13,6%) | 3 (15,7%) | |
| %VPb | |||
| Nenhum | 6 (27,3%) | 5 (26,3%) | 0,316 |
| ≤5% | 2 (9,1%) | 6 (31,6%) | |
| 5%–10% | 9 (40,9%) | 5 (26,3%) | |
| ≥10% | 5 (22,7%) | 3 (15,8%) | |
| Tipo de perda de peso | |||
| Nenhum | 6 (27,3%) | 5 (26,3%) | 0,547 |
| Contínuo | 11 (50%) | 12 (63,1%) | |
| Intercalado com períodos de recuperação de peso | 5 (22,7%) | 2 (10,6%) | |
| Dados antropométricos (cm) | |||
| Prega cutânea tricipital | 1,158±0,48 | 1,200±0,63 | 0,811 |
| Circunferência do braço | 26,93±2,73 | 28,08±3,82 | 0,269 |
| Circunferência da panturrilha | 29,49±5,70 | 32,59±5,07 | 0,341 |
| Índice de massa corporal (kg/m2) | 23,19±3,74 | 23,09±3,96 | 0,934 |
| Impedância bioelétrica | |||
| % água corporal total | 51,71±7,85 | 54,94±3,78 | 0,1341 |
| % massa corporal magra | 67,38±8,44 | 70,69±7,02 | 0,2167 |
| % gordura corporal | 31,44±7,89 | 28,19±6,92 | 0,2051 |
| Contagem absoluta de linfócitosc | |||
| Normal | 11 (50%) | 6 (31,6%) | 0,339 |
| 1,200–2,000mm3 | 7 (31,8%) | 11 (57,9%) | |
| 800–1,199mm3 | 3 (13,6%) | 2 (10,5%) | |
| <800mm3 | 1 (4,6%) | 0 (0) | |
| Dados hematológicos | |||
| Hemoglobina | 13,88±1,58 | 13,95±1,66 | 0,891 |
| Hematócrito | 41,28±4,62 | 41,38±4,8 | 0,946 |
| Dados bioquímicos | |||
| Colesterol total | 191,9±44,4 | 182,9±9,613 | 0,526 |
| HDL | 48,15±14,9 | 48,45±15,23 | 0,949 |
| vLDL | 114,15±39,57 | 112,31±34,57 | 0,875 |
| Proteína total | 6,98±0,63 | 7,04±0,61 | 0,759 |
Todos os pacientes tiveram suas medidas antropométricas mensuradas, exceto o percentual do peso corporal ideal, que não foi calculado para seis sujeitos (35/41). Nenhuma dessas variáveis atingiu significância estatística (tabela 2).
Nenhuma variável bioquímica pré‐operatória, inclusive albumina sérica, atingiu significância estatística (tabela 2). Ao analisar a albumina no pós‐operatório, ou seja, agora influenciada pela resposta inflamatória, os níveis séricos medidos no primeiro (p=0,021) e no sétimo DPO (p=0,027) foram as únicas variáveis que diferiram significantemente entre os dois grupos (tabela 3).
Níveis de albumina sérica medidos no pré‐operatório e no primeiro, terceiro, quinto e sétimo dias após a cirurgia em ambos os grupos de estudo
| Com complicações (n=22) | Sem complicações (n=19) | p‐valor | |
|---|---|---|---|
| Albumina pré‐operatória | 4,11±0,38 | 4,24±0,42 | 0,218 |
| Albumina primeiro DPO | 2,65±0,49 | 3,04±0,56 | 0,021 |
| Albumina terceiro DPO | 2,85±0,52 | 3,14±0,51 | 0,07 |
| Albumina quinto DPO | 3,17±0,58 | 3,40±0,54 | 0,123 |
| Albumina sétimo DPO | 3,21±0,63 | 3,64±0,57 | 0,027 |
Dados expressos em média±desvio padrão.
Em um modelo de regressão logística após o ajuste para fatores de confusão (idade, estágio T, estágio clínico, radioterapia anterior e presença de comorbidades), a albumina sérica do primeiro DPO permaneceu correlacionada com complicações (OR=0,228; IC 95% [0,057–0,882]).
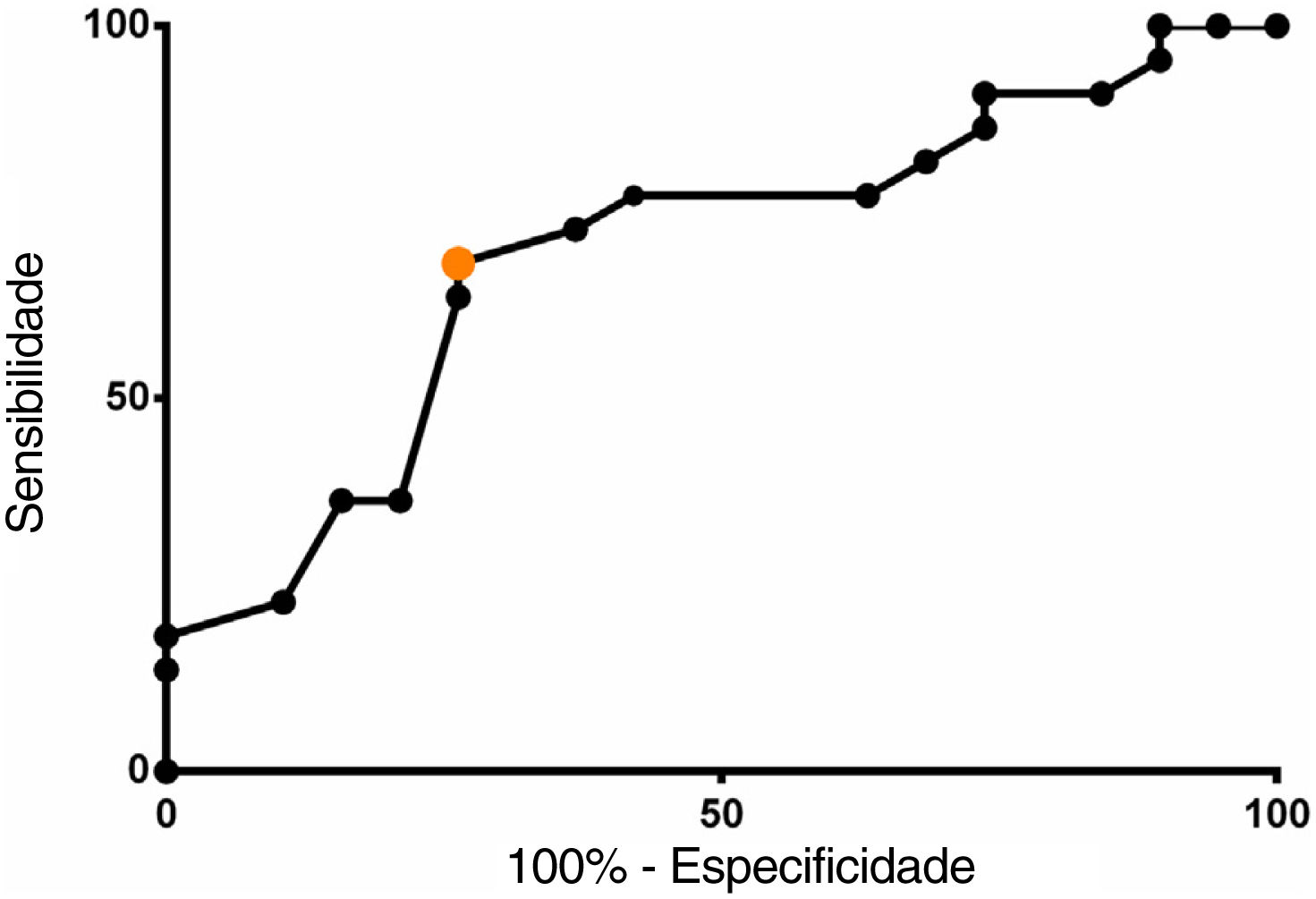
A curva ROC foi usada para determinar a precisão e as propriedades diagnósticas adicionais da albumina sérica medida no primeiro DPO como um preditivo de complicações pós‐operatórias (fig. 1). O poder discriminante global (precisão), calculado a partir da área sob a curva ROC, foi de 69,52% (IC 95% 53,12% a 89,64%; p <0,001).
As propriedades diagnósticas da albumina sérica no primeiro DPO são apresentadas na tabela 4.
Sensibilidade e especificidade dos diferentes níveis séricos de albumina medidos no primeiro dia de pós‐operatório no diagnóstico de complicações pós‐operatórias
| Sensibilidade | Especificidade | LR+a | |
|---|---|---|---|
| <2.3 g/dL | 22,73 | 89,47 | 2,15 |
| <2.5 g/dL | 36,36 | 84,21 | 2,30 |
| <2.8 g/dL | 68,18 | 73,68 | 2,59 |
| <3.0 g/dL | 77,27 | 57,89 | 1,83 |
| <3.5 g/dL | 90,91 | 15,79 | 1,08 |
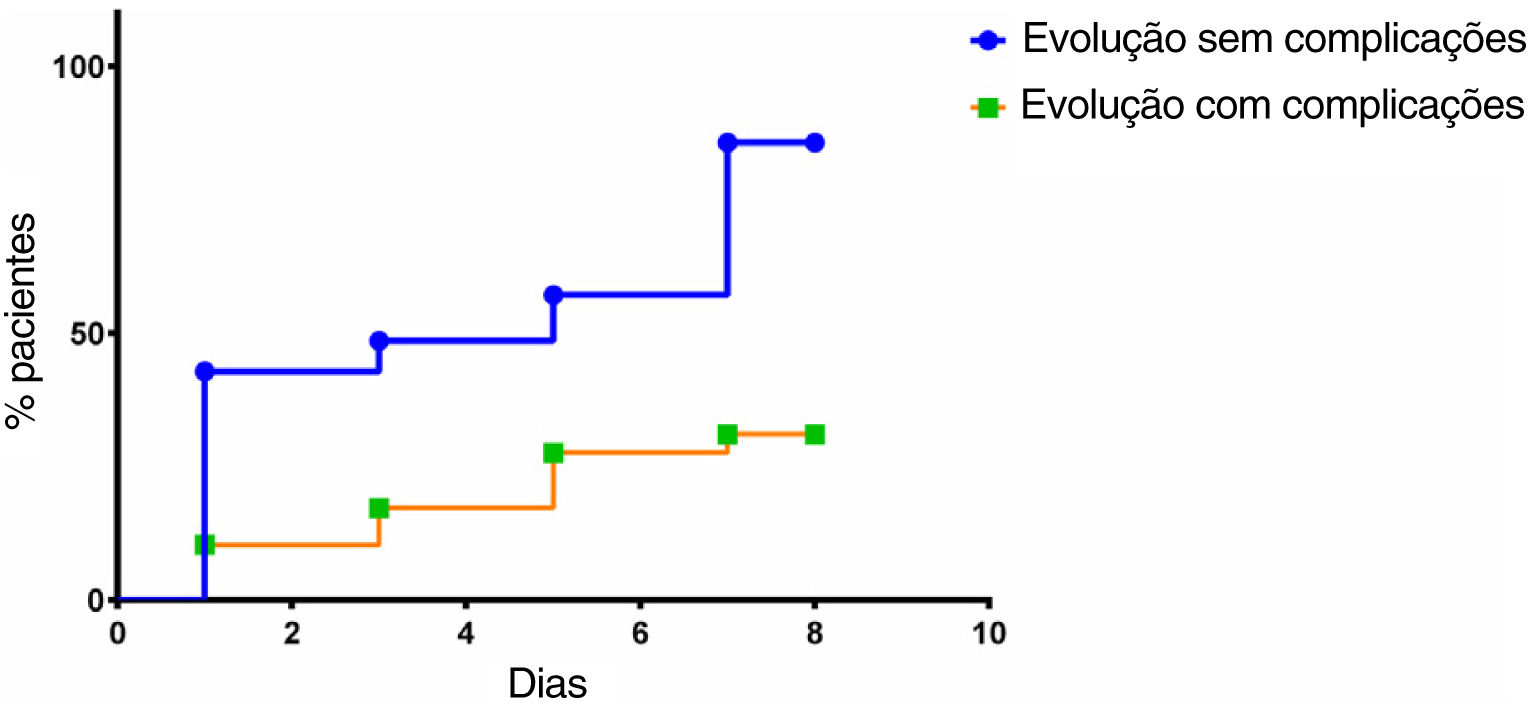
A normalização dos níveis séricos de albumina ocorreu com mais frequência e significativamente mais rápido no grupo sem complicações, comparado ao grupo com complicações (HR=5,096; IC 95%: 1,973 a 13,16; p=0,001) (fig. 2).
DiscussãoA desnutrição é reconhecida como um problema comum entre os pacientes com câncer de cabeça e pescoço, com prevalência nessa população de 20% a 67%.1–3 Os métodos de avaliação nutricional devem ser confiáveis, práticos, de fácil interpretação e baratos.2 Porém, todos têm limitações, razão pela qual uma combinação de variáveis é usada na maioria dos casos. A falta de padronização dos métodos para diagnóstico da desnutrição leva a resultados heterogêneos dos estudos, dificulta o estabelecimento de comparações. A maioria desses estudos se concentra apenas em variáveis como perda de peso, IMC, perda de massa corporal magra ou níveis de proteínas séricas.1 No presente estudo, sete variáveis antropométricas e cinco bioquímicas, além da impedância bioelétrica, foram usadas para determinar quais seriam capazes de predizer complicações pós‐operatórias em pacientes com CCECP.
O valor absoluto do peso e sua taxa de variação têm propriedades prognósticas.12 A porcentagem de variação do peso (%VP), calculada a partir da fórmula (PA‐PU)/PU×100),13 reflete a velocidade com que ocorrem as mudanças na composição corporal. Ao considerar a %VP e o tempo de fatoração na avaliação, a gravidade da perda de peso pode ser avaliada.12 A porcentagem do peso corporal ideal (%PCI), por outro lado, é calculada a partir da fórmula (PA/PI)×100 e é usada para classificar os pacientes como portadores de desnutrição leve (80%–90%), moderada (70%–79%) ou grave (< 69%).12 Deve‐se ter cautela ao usar essa variável, pois alguns indivíduos saudáveis têm peso inferior ao ideal e em pacientes obesos a desnutrição pode passar despercebida.
O estudo prospectivo conduzido por Van Bokhorst‐de van der Schueren et al. mostrou que uma %VP superior a 10% nos últimos seis meses foi a única variável nutricional associada ao risco aumentado de complicações pós‐operatórias.17 Porém, um estudo subsequente do mesmo autor que avaliou as taxas de sobrevivência não encontrou correlação significante.19 Embora alguns autores tenham constatado que pacientes com complicações pós‐operatórias apresentam uma redução maior do peso corporal antes20 ou após a cirurgia,21 outros não encontraram correlação entre essas variáveis e morbimortalidade pós‐operatória.3,22 No presente estudo, os pacientes que apresentaram diminuição da %VP não apresentaram risco aumentado de complicações pós‐operatórias (p=0,316), o que também ocorreu com a %PCI (p=0,517), mostrando que essas variáveis não foram capazes de prever complicações pós‐operatórias nessa população de pacientes.
Os estudos que avaliaram o IMC em pacientes com CCECP produziram resultados conflitantes. Um estudo de caso‐controle mostrou que esses pacientes tinham IMC mais baixo que os controles, mesmo antes do tratamento.23 Alguns estudos encontraram associação entre IMC baixo e aumento da morbimortalidade pós‐operatória.24,25 Por outro lado, outros estudos não encontraram tal correlação.21,23,26 No presente estudo, o IMC médio foi de 23,14±3,73kg/m2 e não houve correlação significativa entre IMC baixo e risco de complicações pós‐operatórias (p=0,934). Uma possível explicação para esse achado é que a maioria dos sujeitos do estudo tinha idade avançada, nos quais a medida da estatura é afetada por compressão vertebral, perda de tônus muscular e alterações posturais.27 Apesar disso, a facilidade de mensuração da estatura e sua correlação com a morbimortalidade encontrada em alguns estudos ainda justificam seu uso em combinação com outros métodos de avaliação do estado nutricional.
Poucos estudos avaliaram o papel das dobras cutâneas e circunferências dos membros na avaliação de pacientes cirúrgicos com CCECP. O presente estudo avaliou as principais variáveis de dobras cutâneas e circunferência de membros nessa população. Não houve diferença estatisticamente significante na PCT (p=0,811), CB (p=0,269) ou CP (p=0,341) entre os pacientes com e sem complicações pós‐operatórias. Algumas limitações da prega cutânea tricipital (PCT), como variação interindividual na distribuição da gordura corporal, mudança na composição corporal devido à idade e estado nutricional e variação da compressibilidade das dobras cutâneas dependente da idade,28 poderiam explicar parcialmente por que os presentes resultados diferem de outros achados da literatura. Um estudo mostrou que pacientes com complicações pós‐operatórias têm uma redução maior da PCT e da CB após a cirurgia,21 enquanto um estudo brasileiro mostrou que pacientes com CB e PCT pré‐operatórias mais baixas têm mais complicações pós‐operatórias.22
A circunferência da panturrilha (CP) é a medida mais sensível para avaliação de massa muscular em idosos,21 faixa etária à qual pertence a maioria dos pacientes com CCECP. No entanto, nenhum estudo avaliou o papel da CP no diagnóstico de desnutrição ou como preditivo de complicações pós‐operatórias em pacientes cirúrgicos com CCECP, o que tornao presente estudo um trabalho pioneiro nesse sentido.
A análise de impedância bioelétrica tem sido amplamente usada nas últimas décadas para avaliação nutricional. Poucos estudos avaliaram seu papel na avaliação de pacientes cirúrgicos com CCECP e nenhum deles encontrou correlação entre as variáveis da análise de impedância bioelétrica — MCM, GC e ACT — e o estado nutricional ou morbidade pós‐operatória nessa população.21,23,29 O presente estudo também não encontrou diferença pré‐operatória estatisticamente significante em ACT (p=0,1341), MCM (p=0,2167) ou GC (p=0,2051) entre os pacientes com e sem complicações pós‐operatórias.
Estudos que examinam os níveis de hemoglobina e transfusão de sangue em pacientes cirúrgicos com CCECT produziram resultados conflitantes. Estudos retrospectivos30,31 encontraram anemia, perda de sangue e transfusão de sangue perioperatória como fatores de risco para complicações pós‐operatórias (infecção e fístula). Estudos prospectivos, entretanto, não observaram tal correlação.21,22 Em concordância com outros estudos prospectivos, o presente estudo também não encontrou diferença quanto à necessidade de hemotransfusão entre os grupos com e sem complicações pós‐operatórias (p=0,232). Todos os pacientes apresentavam níveis normais de hemoglobina pré‐operatória e a menor diferença pós‐operatória encontrada entre os grupos não foi estatisticamente significante (p=0,891).
Contagem absoluta de linfócitos (CAL) fornece uma estimativa aproximada do estado imunológico.10 Diferentes estudos que envolveram pacientes cirúrgicos com CCECP estão de acordo com o presente estudo, pois observaram que a CAL pré‐operatória não tem correlação com complicações pós‐operatórias17,22 ou taxas de sobrevida.19
O colesterol sérico geralmente diminui nos estágios finais da desnutrição, limita o uso dessa variável como ferramenta de avaliação nutricional. Contudo, alguns estudos relacionaram essa redução nos níveis de colesterol com o aumento da morbidade e mortalidade32,33, bem como com internações hospitalares mais longas.33
No contexto da cirurgia de cabeça e pescoço, apenas um estudo investigou a potencial associação entre hipocolesterolemia pré‐operatória (colesterol sérico <100mg/dL) e o risco de fístula faringocutânea,34 mas não encontrou correlação. No presente estudo, nenhum paciente apresentou hipocolesterolemia pré‐operatória e não houve diferença estatisticamente significante (p=0,526) na média de colesterol total entre os grupos com (191,9±44,4mg/dL) e sem complicações (182,9±9,613mg/dL).
A proteína hepática mais comumente monitorada na prática clínica é a albumina.35 A inflamação provocada por trauma (cirúrgico ou não) ou doença aguda (sepse, pancreatite) é a condição mais importante que leva à diminuição dos níveis de albumina sérica.36 Essa diminuição é feita diretamente, estimula o extravasamento transcapilar de albumina do espaço intravascular para o extravascular35,36 e, indiretamente, promove aumento da perda líquida de proteína após o início de um estado catabólico induzido por inflamação e induzindo anorexia e, assim, reduzindo a ingestão de nutrientes — esse fenômeno é denominado “hipoalbuminemia induzida por estresse” (HIE) e não depende do estado nutricional do indivíduo.36
Muitos estudos investigaram a relação entre a albumina sérica e as taxas de morbidade e mortalidade entre pacientes com câncer de cabeça e pescoço tratados cirurgicamente, mas apenas no período pré‐operatório.17,20–22,26,29,31,34 A análise do fator mais importante que influencia o metabolismo das proteínas hepáticas, ou seja, a resposta inflamatória, foi, portanto, esquecida.
Um estudo mostrou que a diferença entre a albumina sérica pré‐operatória e o primeiro DPO foi capaz de prever as principais complicações não infecciosas em 59 pacientes com câncer (p <0,05).37 Apenas dois estudos de cirurgia de cabeça e pescoço também avaliaram os níveis de albumina no pós‐operatório, mas produziram resultados conflitantes. O estudo prospectivo conduzido por Liu et al.24 avaliou os níveis de albumina sérica no pré‐operatório e no terceiro DPO e mostraram que ambos estavam mais elevados no grupo sem complicações infecciosas O estudo prospectivo conduzido por Guo et al., por outro lado, não encontrou diferença estatisticamente significante nos níveis de albumina sérica no pré ou pós‐operatório entre os grupos (p> 0,80).21
No presente estudo, os níveis de albumina sérica foram avaliados tanto no pré‐operatório quanto no pós‐operatório, levaram em consideração sua estreita relação com a resposta inflamatória após o trauma cirúrgico. A associação entre o tempo de normalização dos níveis séricos de albumina (tempo de recuperação) e o risco de complicações pós‐operatórias também foi avaliada.
Os dados apresentados neste estudo mostraram que a albumina sérica do primeiro DPO diferiu significativamente entre os grupos, estabeleceu‐se como um preditivo de complicações após cirurgia de cabeça e pescoço de grande porte (p=0,021). Além disso, seu poder discriminante geral (precisão) foi calculado em 69,52% (IC 95%: 53,12 a 89,64%; p <0,001) e um valor de corte de 2,8g/dL foi considerado o melhor limite para distinguir pacientes com complicações pós‐operatórias de pacientes com uma evolução pós‐operatória não complicada, produziu uma sensibilidade de 68,1% (IC 95%: 45,13% a 86,14%; p=0,033) e uma especificidade de 73,68% (IC 95%: 48,8% a 90,85%; p=0,033).
A hipoalbuminemia (albumina sérica <2,8g/dL) no primeiro dia após uma grande cirurgia de cabeça e pescoço está associada ao risco aumentado de complicações pós‐operatórias. A capacidade de prever esse risco de forma precoce permitiria, por exemplo, estratégias de suplementação nutricional diferenciada para pacientes em risco ou monitorização mais apropriada, por exemplo, mantê‐los no hospital por períodos mais longos.
Além de ocorrer mais frequentemente em pacientes sem complicações, a normalização dos níveis séricos de albumina ocorreu mais cedo no grupo sem complicações, comparado ao grupo com complicações (HR=5,096; IC 95%: 1,973 a 13,16; p=0,001). Esse fenômeno representa um efeito fisiológico normal, indica a melhoria da resposta inflamatória ao trauma cirúrgico e está associado a um menor risco de complicações. A persistência de hipoalbuminemia pós‐operatória apesar de suporte nutricional adequado indica risco maior de complicações pós‐operatórias.
A curva de normalização da albumina sérica avaliou a duração da hipoalbuminemia induzida por estresse, que está diretamente associada ao estresse causado pelo trauma cirúrgico. Além de monitorar os níveis de albumina no pós‐operatório, é importante saber se os níveis séricos do paciente normalizaram e quanto tempo demorou para isso, já que os pacientes sem complicações não apenas normalizaram seus níveis de albumina sérica, mas o fizeram com mais frequência e cinco vezes mais rapidamente do que os pacientes que desenvolveram complicações. Aqueles que conseguiram normalizar seus níveis de albumina sérica e o fizeram precocemente tiveram, consequentemente, um risco menor de complicações, mesmo que inicialmente apresentassem hipoalbuminemia pós‐operatória.
A albumina sérica do sétimo DPO também foi significantemente diferente entre os grupos (p=0,027). No entanto, como a maioria das complicações após cirurgia de cabeça e pescoço ocorre na primeira semana de pós‐operatório, essa variável seria um marcador — e não um preditivo — de complicações pós‐operatórias. Além disso, todos os pacientes com hipoalbuminemia no sétimo DPO já a apresentavam no primeiro DPO.
A principal limitação deste estudo foi o tamanho da amostra, o que reduziu o poder estatístico de algumas comparações. O fato de este estudo ter sido feito em uma única instituição enfraquece sua validade externa, pois seus achados podem não refletir a realidade de outras instituições. Por fim, nem todos os pacientes da amostra tiveram sua composição corporal avaliada por BIA e %PCI.
ConclusãoEntre as variáveis nutricionais avaliadas (bioimpedância elétrica, antropometria e exames bioquímicos), a albumina sérica medida no primeiro dia de pós‐operatório foi significantemente diferente entre os dois grupos de estudo, o que a tornou um preditivo de complicações pós‐operatórias no contexto de câncer de cabeça e pescoço. Além disso, os pacientes que conseguiram normalizar seus níveis de albumina sérica e o fizeram precocemente, mesmo com hipoalbuminemia pós‐operatória inicial, tiveram um risco cinco vezes menor de complicações.
FinanciamentoEsta pesquisa não recebeu nenhum financiamento específico de agências de fomento nos setores público, comercial ou sem fins lucrativos.
Conflitos de interesseOs autores declaram não haver conflitos de interesse.
Como citar este artigo: Reis TG, Silva RA, Nascimento ES, Júnior JB, Oliveira MC, Fava AS, et al. Early postoperative serum albumin levels as predictors of surgical outcomes in head and neck squamous cell carcinoma. Braz J Otorhinolaryngol. 2022;88:48–56.
A revisão por pares é da responsabilidade da Associação Brasileira de Otorrinolaringologia e Cirurgia Cérvico‐Facial.